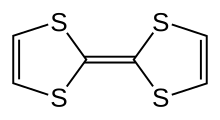
Тетратиафульвален
| |

| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
2,2'-Би(1,3-дитиолилиден) | |
| Другие имена
Δ2,2-би-1,3-дитиол
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 1282106 | |
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.045.979 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 6 Ч 4 С 4 | |
| Молярная масса | 204.34 g·mol −1 |
| Появление | Желтое твердое вещество |
| Температура плавления | От 116 до 119 ° C (от 241 до 246 ° F; от 389 до 392 К) |
| Точка кипения | Разлагается |
| нерастворимый | |
| Растворимость в органических растворителях | Растворимый [ нечеткий ] |
| Структура | |
| 0 Д | |
| Опасности [1] | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
горючий |
| СГС Маркировка : | |

| |
| Предупреждение | |
| H317 | |
| П261 , П280 , П302+П352 , П333+П313 , П363 , П501 | |
| Родственные соединения | |
Родственные соединения
|
|
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Тетратиафульвален ( ТТФ ) представляет собой соединение формулы сераорганическое ( С 3 Ч 2 С 2 ) 2 . Исследования этого гетероциклического соединения способствовали развитию молекулярной электроники . TTF связан с углеводородом фульваленом , (C 5 H 4 ) 2 , заменой четырех групп CH на атомы серы. Более 10 000 научных публикаций посвящены TTF и его производным. [2]
Подготовка
[ редактировать ]Высокий уровень интереса к ТТФ привел к разработке множества синтезов ТТФ и его аналогов. [2] Большинство препаратов предполагают связывание циклических C 3 S 2 строительные блоки, такие как 1,3-дитиол -2-тион или родственные 1,3-дитиол-2-оны. Синтез самого ТТФ начинается с циклического тритиокарбоната. H 2 C 2 S 2 C=S ( 1,3-дитиол-2-тион ), который S -метилируется , а затем восстанавливается с образованием H 2 C 2 S 2 CH(SCH 3 ) (1,3-дитиол-2-илметилтиоэфир), который обрабатывают следующим образом: [3]
- 2 [Ч 2 С 2 С 2 СН] + [БФ 4 ] − + 2 N(CH 2 CH 3 ) 3 → (H 2 C 2 S 2 C) 2 + 2 [NH(CH 2 CH 3 ) 3 ] + [БФ 4 ] −
Редокс-свойства
[ редактировать ]Сам объемный TTF обладает ничем не примечательными электрическими свойствами. Отличительные свойства, однако, связаны с солями его окисленных производных, например солями, полученными из ТТФ + .
Высокую электропроводность солей ТТФ можно объяснить следующими особенностями ТТФ:
- его планарность, которая обеспечивает π-π-укладку его окисленных производных,
- его высокая симметрия, которая способствует делокализации заряда , тем самым сводя к минимуму кулоновское отталкивание, и
- его способность подвергаться окислению при слабом потенциале с образованием стабильного катион-радикала . Электрохимические измерения показывают, что ТТФ может дважды обратимо окисляться:
- ТТФ → ТТФ + + и − ( Е = 0,34 В )
- ТТФ + → ТТФ 2+ + и − ( E = 0,78 В, относительно Ag / AgCl в CH 3 CN ) раствор
Каждое дитиолиденовое кольцо в TTF имеет 7π электронов: по 2 на каждый атом серы, по 1 на каждый sp. 2 атом углерода. Таким образом, окисление преобразует каждое кольцо в ароматическую конфигурацию из 6π-электронов, в результате чего центральная двойная связь остается по существу одинарной, поскольку все π-электроны занимают кольцевые орбитали.
История
[ редактировать ]
Соль [TTF +
]Cl −
В 1972 году сообщалось, что это полупроводник. [5] Впоследствии было показано, что соль переноса заряда [TTF] TCNQ представляет собой полупроводник с узкой запрещенной зоной . [6] Рентгеноструктурные исследования [TTF][TCNQ] выявили стопки частично окисленных молекул TTF, соседствующие с анионными стопками молекул TCNQ. Этот мотив «разделенной стопки» был неожиданным и отвечает за отличительные электрические свойства, то есть высокую и анизотропную электропроводность . Со времени этих ранних открытий было получено множество аналогов TTF. К хорошо изученным аналогам относятся тетраметилтетратиафульвален (Me 4 TTF), тетраметилселенафульвалены (TMTSF) и бис(этилендитио)тетратиафульвален (BEDT-TTF, CAS [66946-48-3]). [7] Некоторые соли тетраметилтетратиафульвалена (называемые солями Фабра ) имеют определенное значение в качестве органических сверхпроводников .
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Тетратиафульвален» . pubchem.ncbi.nlm.nih.gov .
- ^ Jump up to: а б Бендиков М; Вудль, Ф; Перепичка, Д.Ф. (2004). «Тетратиафульвалены, олигоаценены и их производные бакминстерфуллеренов: кирпич и раствор органической электроники». Химические обзоры . 104 (11): 4891–4945. дои : 10.1021/cr030666m . ПМИД 15535637 .
- ^ Вудл, Ф.; Каплан, М.Л. (1979). «2,2'-Би-L,3-дитиолиден (тетратиафульвален, ТТФ) и его катион-радикальные соли». Неорганические синтезы . Том. 19. С. 27–30. дои : 10.1002/9780470132500.ch7 . ISBN 978-0-470-13250-0 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Д. Шассо; Г. Комбертон; Ж. Готье; К. Хау (1978). «Повторное исследование структуры гексаметилентетратиафульвален-тетрацианохинодиметанового комплекса» . Acta Crystallographica Раздел B. 34 (2): 689. Бибкод : 1978AcCrB..34..689C . дои : 10.1107/S0567740878003830 .
- ^ Вудл, Ф.; Вобшалл, Д.; Хуфнагель, Э.Дж. (1972). «Электрическая проводимость системы бис (1,3-дитиол)-бис (1,3-дитиолий)». Дж. Ам. хим. Соц. 94 (2): 670–672. дои : 10.1021/ja00757a079 .
- ^ Феррарис, Дж.; Коуэн, DO; Валатка В.В. младший; Перлштейн, Дж. Х. (1973). «Перенос электрона в новом высокопроводящем донорно-акцепторном комплексе». Дж. Ам. хим. Соц. 95 (3): 948–949. дои : 10.1021/ja00784a066 .
- ^ Ларсен, Дж.; Ленуар, К. (1998). «2,2'-би-5,6-дигидро-1,3-дитиол[4,5-b][1,4]дитиенилиден (BEDT-TTF)» . Органические синтезы
{{cite journal}}: CS1 maint: multiple names: authors list (link); Сборник томов , т. 9, с. 72 .
Дальнейшее чтение
[ редактировать ]- Ровира, К. (2004). «Бис (этилентио) тетратиафульвален (BET-TTF) и родственные ему диссимметричные доноры электронов: от молекулы к функциональным молекулярным материалам и устройствам (OFET)». Химические обзоры . 104 (11): 5289–5317. дои : 10.1021/cr030663+ . ПМИД 15535651 .
- Йода, М; Хасэгава, М; Мияке, Ю (2004). «Би-ТТФ, Бис-ТТФ и родственные олигомеры ТТФ». Химические обзоры . 104 (11): 5085–5113. дои : 10.1021/cr030651o . ПМИД 15535643 .
- Фрер, П.; Скабара, П.Дж. (2005). «Соли расширенных аналогов тетратиафульвалена: взаимосвязь между молекулярной структурой, электрохимическими свойствами и организацией твердого тела». Обзоры химического общества . 34 (1): 69–98. дои : 10.1039/b316392j . ПМИД 15643491 .
- Горг, Ален; Юдомм, Петрик; Салле, Марк. (2004). «Высокофункционализированные тетратиафульвалены: путешествие по синтетическому следу электрофильных алкинов». Химические обзоры . 104 (11): 5151–5184. дои : 10.1021/cr0306485 . ПМИД 15535646 .
- Физические свойства тетратиафульвалена из литературы.
- Сегура, Хосе Л.; Мартин, Назарио (2001). «Новые концепции в химии тетратиафульвалена». Angewandte Chemie, международное издание . 40 (8): 1372–1409. doi : 10.1002/1521-3773(20010417)40:8<1372::aid-anie1372>3.0.co;2-i . ПМИД 11317287 .