Сероорганическая химия
Сероорганическая химия — изучение свойств и синтез сераорганических соединений — органических соединений , содержащих серу . [1] Они часто ассоциируются с неприятным запахом, но многие из самых сладких известных соединений являются сероорганическими производными, например, сахарином . Природа изобилует сероорганическими соединениями — сера жизненно необходима для жизни. Из 20 распространенных аминокислот две ( цистеин и метионин ) являются сероорганическими соединениями, а антибиотики, пенициллин и сульфаниламидные препараты содержат серу. В то время как серосодержащие антибиотики спасают множество жизней, сернистый иприт является смертельным боевым отравляющим веществом. Ископаемое топливо , уголь , нефть и природный газ , полученные из древних организмов, обязательно содержат сероорганические соединения, удаление которых является основным направлением деятельности нефтеперерабатывающих заводов .
Сера разделяет халькогенную группу с кислородом , селеном и теллуром , и ожидается, что сераорганические соединения имеют сходство с соединениями углерод-кислород, углерод-селен и углерод-теллур.
Классическим химическим тестом на обнаружение соединений серы является галогенный метод Кариуса .
Структурные классы
[ редактировать ]Сероорганические соединения можно классифицировать по серосодержащим функциональным группам , которые перечислены (примерно) в порядке убывания их встречаемости.
- Иллюстративные сероорганические соединения
- Аллицин , активное вкусовое соединение в измельченном чесноке.
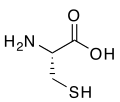
- ( R )- Цистеин , аминокислота, содержащая тиоловую группу.
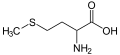
- Метионин — аминокислота , содержащая сульфид.
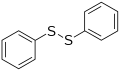
- Дифенилдисульфид , представитель дисульфида.
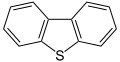
- Дибензотиофен , компонент сырой нефти.
- Перфтороктансульфоновая кислота — спорное поверхностно-активное вещество.
- Липоевая кислота , важный кофактор четырех митохондриальных ферментных комплексов.
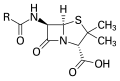
- Основная структура пенициллина , где «R» — переменная группа.
- Сернистый иприт , разновидность сульфида, используемого в качестве боевого отравляющего вещества .
- Суран Мартина с качающейся структурой, как у SF 4. [2]
Сульфиды
[ редактировать ]Сульфиды, ранее известные как тиоэфиры, характеризуются связями C-S-C. [3] [4] По сравнению со связями C-C связи C-S длиннее, поскольку атомы серы больше атомов углерода, и примерно на 10% слабее. Типичные длины связей в соединениях серы составляют 183 пм для одинарной связи S-C в метантиоле и 173 пм в тиофене . C-S Энергия диссоциации связи для тиометана составляет 89 ккал/моль (370 кДж/моль) по сравнению с 100 ккал/моль метана (420 кДж/моль), а при замене водорода метильной группой энергия снижается до 73 ккал/моль. (305 кДж/моль). [5] Одинарная связь углерод-кислород короче, чем связь C-C. Энергии диссоциации связи для диметилсульфида и диметилового эфира составляют соответственно 73 и 77 ккал/моль (305 и 322 кДж/моль).
Сульфиды обычно получают алкилированием тиолов. К алкилирующим агентам относятся не только алкилгалогениды, но также эпоксиды, азиридины и акцепторы Михаэля . [6]
Их также можно получить с помощью перегруппировки Паммерера .
В Феррарио реакции фениловый эфир превращается в феноксатиин под действием элементарной серы и хлорида алюминия . [7]
Тиоацетали и тиокетали имеют последовательность связей C-S-C-S-C. Они представляют собой подкласс сульфидов. Тиоацетали полезны для « умполунга » карбонильных групп. Тиоацетали и тиокетали также можно использовать для защиты карбонильной группы в органическом синтезе.
Вышеуказанные классы соединений серы также существуют в насыщенных и ненасыщенных гетероциклических структурах, часто в сочетании с другими гетероатомами , как показано на тииранах , тииренах , тиетанах , тиетах , дитиетанах , тиоланах , тианах , дитианах , тиепанах , тиепинах , тиазолах , изотиазолах и тиофены и др. Последние три соединения представляют собой особый класс серосодержащих гетероциклов, являющихся ароматическими . Резонансная стабилизация тиофена составляет 29 ккал/моль (121 кДж /моль) по сравнению с 20 ккал/моль (84 кДж/моль) для аналога кислорода фурана . Причиной такого различия является более высокая электроотрицательность кислорода, оттягивающего электроны к себе за счет тока ароматического кольца. Однако как ароматический заместитель тиогруппа менее отдает электроны, чем алкоксигруппа. Дибензотиофены (см. рисунок) — трициклические гетероциклы, состоящие из двух бензольных колец, конденсированных с центральным тиофеновым кольцом, широко встречаются в более тяжелых фракциях нефти.
Тиолы, дисульфиды, полисульфиды
[ редактировать ]Тиоловые группы содержат функциональность R-SH. Тиолы структурно аналогичны спиртовой группе, но эти функциональные группы сильно различаются по своим химическим свойствам. Тиолы более нуклеофильны , более кислы и легче окисляются. Эта кислотность может отличаться на 5 п К а единиц. [8]
Разница в электроотрицательности между серой (2,58) и водородом (2,20) невелика, поэтому водородная связь в тиолах не заметна. Алифатические тиолы образуют монослои на золоте , что актуально в нанотехнологиях .
Доступ к некоторым ароматическим тиолам можно получить с помощью реакции Герца .
Дисульфиды R-S-S-R с ковалентной связью сера-сера важны для сшивания : в биохимии для сворачивания и стабильности некоторых белков и в химии полимеров для сшивания каучука.
Также известны более длинные серные цепи, например, в природном продукте варацине , который содержит необычное пентатиепиновое кольцо (5-серная цепь, циклизованная по бензольному кольцу).
Тиоэфиры
[ редактировать ]Тиоэфиры имеют общую структуру R-C(O)-S-R. Они родственны обычным эфирам (R-C(O)-O-R), но более подвержены гидролизу и связанным с ним реакциям. Тиоэфиры, образующиеся из коэнзима А, играют важную роль в биохимии, особенно в синтезе жирных кислот .
Сульфоксиды, сульфоны и тиосульфинаты
[ редактировать ]Сульфоксид сульфон , R-S(O)-R, представляет собой S -оксид сульфида («сульфид-оксид»), , R-S(O) 2 -R, представляет собой S , S -диоксид сульфида. , тиосульфинат , R-S(O)-S-R, представляет собой S -оксид дисульфида, а тиосульфонат , R-S(O) 2 -S-R, представляет собой S , S -диоксид дисульфида. . Все эти соединения хорошо известны в обширной химии, например, диметилсульфоксид , диметилсульфон и аллицин (см. рисунок).
Сульфимиды, сульфоксимиды, сульфондиимины
[ редактировать ]Сульфимиды (также называемые сульфилиминами) представляют собой серо-азотные соединения структуры R 2 S=NR', азотистый аналог сульфоксидов. Они представляют интерес отчасти из-за своих фармакологических свойств. Когда к сере присоединены две разные группы R, сульфимиды являются хиральными. Сульфимиды образуют стабильные α-карбанионы. [9]
Сульфоксимиды (также называемые сульфоксиминами) представляют собой тетракоординированные серо-азотные соединения, изоэлектронные сульфонам, в которых один атом кислорода сульфона заменен замещенным атомом азота, например, R 2 S(O)=NR'. Когда к сере присоединены две разные группы R, сульфоксимиды являются хиральными. Большая часть интереса к этому классу соединений связана с открытием того, что метионинсульфоксимид (метионинсульфоксимин) является ингибитором глутаминсинтетазы . [10]
Сульфонедиимины (также называемые сульфодиимины, сульфодиимиды или сульфондиимиды) представляют собой тетракоординированные серо-азотные соединения, изоэлектронные сульфонам, в которых оба атома кислорода сульфона заменены замещенным атомом азота, например, R 2 S(=NR') 2 . Они представляют интерес из-за своей биологической активности и в качестве строительных блоков для синтеза гетероциклов. [11]
S -нитрозотиолы
[ редактировать ]S -Нитрозотиолы , также известные как тионитриты, представляют собой соединения, содержащие нитрозогруппу, присоединенную к атому серы тиола, например R-S-N=O. Они привлекли значительное внимание в биохимии, поскольку служат донорами иона нитрозония NO. + и оксид азота NO, которые могут служить сигнальными молекулами в живых системах, особенно в отношении расширения сосудов. [12]
Галогениды серы
[ редактировать ]Известен широкий спектр сераорганических соединений, которые содержат один или несколько атомов галогена («X» в последующих химических формулах), связанных с одним атомом серы, например: сульфенилгалогениды , RSX; сульфинилгалогениды , RS(O)X; сульфонилгалогениды , RSO 2 X; трихлориды алкил- и арилсеры, RSCl 3 и трифториды, RSF 3 ; [13] и алкил- и арилпентафториды серы, RSF 5 . [14] Менее известны тетрагалогениды диалкилсеры, представленные преимущественно тетрафторидами, например R 2 SF 4 . [15]
Тиокетоны, тиоальдегиды и родственные соединения
[ редактировать ]Соединения с двойными связями между углеродом и серой относительно редки, но включают важные соединения сероуглерод , карбонилсульфид и тиофосген . Тиокетоны (RC(=S)R') встречаются редко с алкильными заместителями, но одним из примеров является тиобензофенон . Тиоальдегиды встречаются еще реже, что отражает отсутствие у них стерической защиты (« тиоформальдегид » существует в виде циклического тримера). Тиоамиды с формулой R 1 C(=S)N(R 2 )R 3 более распространены. Обычно их получают реакцией амидов с реагентом Ловессона . Изотиоцианаты с формулой R−N=C=S встречаются в природе. Растительные продукты с характерным вкусом, обусловленным изотиоцианатами, включают васаби , хрен , горчицу , редис , брюссельскую капусту , кресс-салат , настурцию и каперсы .
S -оксиды и S , S -диоксиды тиокарбонильных соединений.
[ редактировать ]S - оксиды тиокарбонильных соединений известны как тиокарбонил- S -оксиды: (R 2 C=S=O и тиокарбонил S , S -диоксиды или сульфены , R 2 C=SO 2 ). Тионовые S -оксиды также известны как сульфины , и хотя ИЮПАК считает этот термин устаревшим, [16] это имя сохранилось в литературе. [17] Эти соединения хорошо известны в обширной химии. [18] [19] Примеры включают син -пропанетиал- S -оксид и сульфен .
Тройные связи между углеродом и серой
[ редактировать ]Тройные связи между серой и углеродом в сульфаалкинах редки и встречаются в моносульфиде углерода (CS). [20] и были предложены для соединений F 3 CCSF 3 [21] [22] и F 5 SCSF 3 . [23] Соединение HCSOH также представлено как имеющее формальную тройную связь. [24]
Тиокарбоновые кислоты и тиоамиды
[ редактировать ]тиокарбоновые кислоты Хорошо известны (RC(O)SH) и дитиокарбоновые кислоты (RC(S)SH). Они структурно похожи на карбоновые кислоты, но более кислые. Тиоамиды аналогичны амидам.
Сульфоновые, сульфиновые и сульфеновые кислоты, сложные эфиры, амиды и родственные соединения
[ редактировать ]Сульфоновые кислоты имеют функциональность R-S(=O) 2 -OH. [25] Это сильные кислоты, которые обычно растворяются в органических растворителях. Сульфоновые кислоты, такие как трифторметансульфоновая кислота, являются часто используемым реагентом в органической химии . Сульфиновые кислоты имеют функциональность R-S(O)-OH, а сульфеновые кислоты имеют функциональность R-S-OH. В ряду сульфоновые-сульфиновые-сульфеновые кислоты в этом порядке уменьшаются как сила кислоты, так и устойчивость. [26] [27] Сульфонамиды, сульфинамиды и сульфенамиды с формулами R-SO 2 NR' 2 , R-S(O)NR' 2 и R-SNR' 2 соответственно имеют богатый химический состав. Например, сульфамидные препараты представляют собой сульфаниламиды, полученные в результате ароматического сульфирования . Хиральные сульфинамиды используются в асимметричном синтезе, а сульфенамиды широко используются в процессе вулканизации для содействия сшиванию. Тиоцианаты , R-S-CN, по реакционной способности родственны сульфенилгалогенидам и сложным эфирам.
Сульфоний, оксосульфоний и родственные соли
[ редактировать ]Ион сульфония представляет собой положительно заряженный ион с тремя органическими заместителями, присоединенными к сере, с формулой [R 3 S] + . Вместе со своим отрицательно заряженным аналогом, анионом, эти соединения называются сульфониевыми солями. Ион оксосульфония представляет собой положительно заряженный ион с тремя органическими заместителями и кислородом, присоединенным к сере, с формулой [R 3 S=O] + . Вместе со своим отрицательно заряженным аналогом, анионом, эти соединения называются солями оксосульфония. Родственные виды включают ионы алкоксисульфония и хлорсульфония, [R 2 SOR] + и [R 2 SCl] + , соответственно.
Сульфоний, оксосульфоний и тиокарбонилилиды
[ редактировать ]Депротонирование солей сульфония и оксосульфония дает илиды структуры R 2 S. + −С − −R′ 2 и R 2 S(O) + −С − −R' 2 . Хотя сульфониевые илиды , например, в реакции Джонсона-Кори-Чайковского , используемой для синтеза эпоксидов , иногда рисуются с двойной связью C=S, например, R 2 S=CR' 2 , илидная связь углерод-сера сильно поляризована и лучше описать как ионный. Илиды сульфония являются ключевыми промежуточными соединениями в синтетически полезной перегруппировке Стивенса . Тиокарбонилилиды (RR'C=S + −С − −RR') может образовываться путем раскрытия цикла тиранов , фотоциклизации арилвинилсульфидов, [28] а также другими процессами.
Сульфураны и персульфураны
[ редактировать ]Сульфураны представляют собой относительно специализированную функциональную группу, содержащую четырехвалентную серу, с формулой SR 4. [2] Аналогичным образом, персульфураны содержат шестивалентный SR 6 .
Один из немногих полностью углеродных персульфуранов имеет два метильных и два бифениленовых лиганда : [29]
Его получают из соответствующего сульфурана 1 с дифторидом ксенона / трифторидом бора в ацетонитриле до сульфуранилдикатиона 2 с последующей реакцией с метиллитием в тетрагидрофуране с образованием (стабильного) персульфурана 3 в качестве цис-изомера . Рентгеновская дифракция C-S показывает, что длины связей находятся в диапазоне от 189 до 193 пм (длиннее стандартной длины связи) с центральным атомом серы в искаженной октаэдрической молекулярной геометрии .
Сероорганические соединения в природе
[ редактировать ]В природе встречается множество сероорганических соединений. Наиболее распространены аминокислоты метионин , цистеин и цистин . Витамины биотин и тиамин , а также липоевая кислота содержат гетероциклы серы. Глутатион является основным внутриклеточным антиоксидантом . [6] Пенициллин и цефалоспорин — жизненно важные антибиотики , полученные из грибов. Глиотоксин представляет собой серосодержащий микотоксин, продуцируемый несколькими видами грибов, исследуемых в качестве противовирусного агента.
В ископаемом топливе
[ редактировать ]Общие сероорганические соединения присутствуют в нефтяных фракциях на уровне 200–500 ppm. Обычными соединениями являются тиофены , особенно дибензотиофены . Эти соединения удаляются в процессе гидрообессеривания (HDS) на нефтеперерабатывающих заводах, как показано на примере гидрогенолиза тиофена: С 4 Ч 4 С + 8 Ч 2 → С 4 Ч 10 + Ч 2 С
Вкус и запах
[ редактировать ]Такие соединения, как аллицин и айоен, ответственны за запах чеснока . Лентионин придает вкус грибам шиитаке . Летучие сераорганические соединения также придают тонкие вкусовые характеристики винам , орехам, сыру чеддер , шоколаду , кофе и тропическим фруктам. [30] Многие из этих натуральных продуктов также обладают важными лечебными свойствами, такими как предотвращение агрегации тромбоцитов или борьба с раком.
Люди и другие животные обладают чрезвычайно чувствительным обонянием к запахам низковалентных сераорганических соединений, таких как тиолы, сульфиды и дисульфиды. Летучие тиолы с неприятным запахом представляют собой продукты распада белков, обнаруженные в гнилой пище, поэтому точная идентификация этих соединений имеет решающее значение для предотвращения интоксикации. Низковалентные летучие соединения серы также обнаруживаются в районах с низким уровнем кислорода в воздухе, что создает риск удушья.
Медь необходима для высокочувствительного обнаружения некоторых летучих тиолов и родственных сераорганических соединений обонятельными рецепторами мышей. Пока неизвестно, нужна ли людям медь для чувствительного обнаружения тиолов. [31]
Ссылки
[ редактировать ]- ^ Блок, Э. (1978). Реакции сероорганических соединений . Академическая пресса. ISBN 0-12-107050-6 .
- ^ Перейти обратно: а б Мартин, Джей Си; Архарт, Р.Дж.; Франц, Дж.А.; Пероцци, EF; Каплан, Л.Дж. «Бис[2,2,2-трифтор-1-фенил-1-(трифторметил)этокси]дифенилсульфуран». Органические синтезы . 57:22 . дои : 10.15227/orgsyn.057.0022 .
- ^ Синяя книга ИЮПАК по органической химии. Правила C-5: Соединения, содержащие двухвалентную серу http://www.acdlabs.com/iupac/nomenclature/79/r79_25.htm
- ^ Синяя книга ИЮПАК по органической химии. Рекомендация R-5.7.1.3.4 Тиокарбоновые и тиокарбоновые кислоты. [1]
- ^ Справочник по химии и физике (81-е изд.). ЦРК Пресс. Июнь 2000 г. ISBN. 0-8493-0481-4 .
- ^ Перейти обратно: а б Чаухан, Панкадж; Махаджан, Суручи; Эндерс, Дитер (2014). «Органокаталитические реакции образования связи углерод-сера». Химические обзоры . 114 (18): 8807–8864. дои : 10.1021/cr500235v . ПМИД 25144663 .
- ^ Сутер, СМ; Максвелл, Чарльз Э. (1938). «Фенокстин [Феноксатиин]». Органические синтезы . 18:64 . дои : 10.15227/orgsyn.018.0064 .
- ^ Кремлин, Р.Дж. (1996). Введение в сероорганическую химию . Чичестер: Джон Уайли и сыновья. ISBN 0-471-95512-4 .
- ^ Гарсиа Руано, JL; Сид, МБ; Мартин Кастро, AM; Алеман, Дж. (2008). «Ациклические S , S -диалкилсульфимиды». Ин Камбе, Н. (ред.). Наука синтеза . Том. 39. Тиме. стр. 352–375. ISBN 978-1-58890-530-7 .
- ^ Драбович Дж.; Левковски Дж.; Кудельска, В.; Гирек, Т. (2008). « S , S -Диалкилсульфоксимиды». Ин Камбе, Н. (ред.). Наука синтеза . Том. 39. Тиме. стр. 154–173. ISBN 978-1-58890-530-7 .
- ^ Драбович Дж.; Левковски Дж.; Кудельска, В.; Гирек, Т. (2008). « S , S -Диалкилсульфондиимины». Ин Камбе, Н. (ред.). Наука синтеза . Том. 39. Тиме. стр. 173–180. ISBN 978-1-58890-530-7 .
- ^ Чжан, Ю.; Хогг, Н. (2005). « S -Нитрозотиолы: клеточное образование и транспорт». Свободный Радик. Биол. Мед . 38 (7): 831–838. doi : 10.1016/j.freeradbiomed.2004.12.016 . ПМИД 15749378 .
- ^ Браверман, С.; Черкинский, М.; Левинджер, С. (2008). «Алкилсера Тригалогениды». Ин Камбе, Н. (ред.). Наука синтеза . Том. 39. Тиме. стр. 187–188. ISBN 978-1-58890-530-7 .
- ^ Шеппард, Вашингтон (1962). «Пентафториды арилсеры». Дж. Ам. хим. Соц. 84 (16): 3064–3072. дои : 10.1021/ja00875a006 .
- ^ Драбович Дж.; Левковски Дж.; Кудельска, В.; Гирек, Т. (2008). «Тетрагалогениды диалкилсеры». Ин Камбе, Н. (ред.). Наука синтеза . Том. 39. Тиме. стр. 123–124. ISBN 978-1-58890-530-7 .
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Интернет-исправленная версия: (2006–) « Сульфины ». два : 10.1351/goldbook.S06108
- ^ Маккоу, Патрик Г.; Бакли, Наоми М.; Коллинз, Стюарт Г.; Магуайр, Анита Р. (март 2016 г.). «Получение, реакционная способность и использование сульфинов в органическом синтезе». Европейский журнал органической химии . 2016 (9): 16:30–1650. дои : 10.1002/ejoc.201501538 .
- ^ Опиц, Г. (февраль 1967 г.). «Сульфины и сульфены – S-оксиды и S,S-диоксиды тиоальдегидов и тиокетонов». Angewandte Chemie International Edition на английском языке . 6 (2): 107–123. дои : 10.1002/anie.196701071 .
- ^ Званенбург, Бинне (май 1989 г.). «Сульфиновая химия». Фосфор, сера, кремний и родственные им элементы . 43 (1–2): 1–24. дои : 10.1080/10426508908040276 .
- ^ Мольцен, ЕК; Клабунде, К.Дж.; Сеннинг, А. (1988). «Моносульфид углерода: обзор». хим. Преподобный . 88 (2): 391. doi : 10.1021/cr00084a003 .
- ^ Поттер, Б.; Зеппельт, К. (1984). «Трифторид трифторэтилидинсеры, F 3 C-C≡SF 3 ». Энджью. хим. Межд. Эд. англ. 23 (2): 150. doi : 10.1002/anie.198401501 .
- ^ Бушманн, Дж.; Дамериус, Р.; Герхардт, Р.; Ленц, Д.; Люгер, П.; Маршалл, Р.; Преугшат, Д.; Зеппельт, К.; Саймон, А. (1992). «(Трифторэтилидин)трифторид серы, F 3 CC≡SF 3 : две твердотельные структуры и реакционная способность карбена». Дж. Ам. хим. Соц. 114 (24): 9465. doi : 10.1021/ja00050a027 .
- ^ Герхардт, Р.; Герлбиг, Т.; Бушаманн, Дж.; Люгер, П.; Зеппельт, К. (1988). «Единица SF 5 как стерическая защитная группа; синтез и структура F 5 S-C≡SF 3 ». Энджью. хим. Межд. Эд. англ. 27 (11): 1534. doi : 10.1002/anie.198815341 .
- ^ Шрайнер, П.; Райзенауэр, Х.; Романски, Дж.; Млостон, Г. (2009). «Формальная тройная связь углерод-сера: H-C≡S-O-H». Энджью. хим. Межд. Эд. англ. 48 (43): 8133–8136. дои : 10.1002/anie.200903969 . ПМИД 19768827 .
- ^ Синяя книга ИЮПАК по органической химии. C-6 Галогениды серы, сульфоксиды, сульфоны и серные кислоты и их производные http://www.acdlabs.com/iupac/nomenclature/79/r79_26.htm
- ^ Браверман, С.; Черкинский, М.; Левинджер, С. (2008). «Алкансульфиновые кислоты и соли». Ин Камбе, Н. (ред.). Наука синтеза . Том. 39. Тиме. стр. 196–211. ISBN 978-1-58890-530-7 .
- ^ Драбович Дж.; Келбасинский, П.; Лыжва, П.; Заяц, А.; Миколайчик, М. (2008). «Алкансульфеновые кислоты». Ин Камбе, Н. (ред.). Наука синтеза . Том 39. Тиме. стр. 550–557. ISBN 978-1-58890-530-7 .
- ^ Шульц, АГ; ДеТар, МБ (1976). «Тиокарбонилилиды. Реакции фотогенерации, перегруппировки и циклоприсоединения». Дж. Ам. хим. Соц. 98 (12): 3564–3572. дои : 10.1021/ja00428a029 .
- ^ Сато, С.; Мацунага, К.; Хорн, Э.; Фурукава, Н.; Набешима, Т. (2006). «Выделение и молекулярная структура органоперсульфуранов [12-S-6(C6)]». Дж. Ам. хим. Соц. 128 (21): 6778–6779. дои : 10.1021/ja060497y . ПМИД 16719444 .
- ^ Цянь, MC; Фан, Х.; Махаттанатави, К., ред. (2011). Летучие соединения серы в продуктах питания . Серия симпозиумов ACS 1068. Том. 1068. Американское химическое общество. дои : 10.1021/bk-2011-1068 . ISBN 978-0-8412-2616-6 .
- ^ Дуань, X.; Блок, Э.; Ли, З.; Коннелли, Т.; Чжан, Дж.; Хуанг, З.; Су, Х.; Пан, Ю.; Ву, Л.; Чи, К.; Томас, С.; Чжан, С.; Ма, М.; Мацунами, Х.; Чен, Г.-К.; Чжан, Х. (2012). «Решающая роль меди в обнаружении одорантов, координирующих металлы» . Учеб. Натл. акад. наук. США . 109 (9): 3492–3497. Бибкод : 2012PNAS..109.3492D . дои : 10.1073/pnas.1111297109 . ПМК 3295281 . ПМИД 22328155 .


![Суран Мартина с качающейся структурой, как у SF4[2]](http://upload.wikimedia.org/wikipedia/commons/thumb/3/36/MartinSulfurane.svg/96px-MartinSulfurane.svg.png)

