Химия органоциркония и гафния

Цирконийорганическая химия — это наука, изучающая свойства, структуру и реакционную способность цирконийорганических соединений , которые представляют собой металлоорганические соединения , содержащие химические связи между углеродом и цирконием . [2] Цирконийорганические соединения широко изучаются, отчасти потому, что они являются полезными катализаторами полимеризации Циглера-Натта .
Сравнение с титаноорганической химией
[ редактировать ]Многие цирконийорганические соединения имеют аналоги по титаноорганической химии . Цирконий(IV) более устойчив к восстановлению, чем соединения титана(IV), которые часто превращаются в производные Ti(III). Кроме того, Zr(II) является особенно мощным восстановителем, образующим прочные азотистые комплексы . Будучи более крупным атомом, цирконий образует комплексы с более высокими координационными числами , например, полимерный [CpZrCl 3 ] n по сравнению с мономерным CpTiCl 3 (Cp = C 5 H 5 ).
История
[ редактировать ]Дибромид цирконоцена был получен в 1953 году реакцией циклопентадиенилмагния бромида и хлорида циркония (IV) . [3] был получен дигидрид Cp 2 ZrH 2 В 1966 году реакцией Cp 2 Zr(BH 4 ) 2 с триэтиламином . [4] В 1970 году родственный гидрохлорид (теперь называемый реактивом Шварца ) был получен восстановлением дихлорида цирконацена (Cp 2 ZrCl 2 ) алюмогидридом лития (или родственным LiAlH(t-BuO) 3 ). [5] [6] [7] Разработка циркониевых реагентов была отмечена Нобелевской премией по химии Эй-Ичи Негиши. [8] [9]
Цирконоценовая химия
[ редактировать ]
Основное применение цирконоценов связано с их использованием в качестве катализаторов полимеризации олефинов. [11] [12]
Реагент Шварца ([Cp 2 ZrHCl] 2 ) участвует в гидроцирконировании, что находит некоторое применение в органическом синтезе . Субстратами для гидроцирконирования являются алкены и алкины . Терминальные алкины образуют виниловые комплексы. Вторичные реакции — нуклеофильное присоединение , трансметаллирование , [13] сопряженное присоединение , реакции сочетания , карбонилирование и галогенирование .
Обширный химический состав также был продемонстрирован на примере дихлорида декаметилцирконоцена Cp* 2 ZrCl 2 . Хорошо изученные производные включают Cp* 2 ZrH 2 , [Cp* 2 Zr] 2 (N 2 ) 3 , Cp* 2 Zr(CO) 2 и Cp* 2 Zr(CH 3 ) 2 .
Дихлорид цирконоцена можно использовать для циклизации енинов и диенов с образованием циклических или бициклических алифатических систем. [14] [15]
Алкиловые и CO комплексы
[ редактировать ]Простейшими цирконийорганическими соединениями являются гомолептические алкилы. Соли [Zr(CH 3 ) 6 ] 2- известны. Тетрабензилцирконий является предшественником многих катализаторов полимеризации олефинов. Его можно превратить в смешанные алкил- , алкокси- и галогенидные производные Zr(CH 2 C 6 H 5 ) 3 X (X = CH 3 , OC 2 H 5 , Cl).
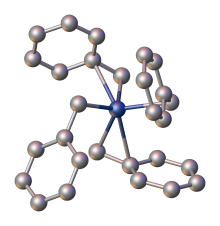
Помимо смешанного Cp 2 Zr(CO) 2 , цирконий образует бинарный карбонил [Zr(CO) 6 ] 2- . [18]
Гафнийорганическая химия
[ редактировать ]Гафнийорганические соединения ведут себя почти идентично циркониевым соединениям, поскольку гафний находится чуть ниже циркония в таблице Менделеева . Известны многие Hf-аналоги соединений Zr, в том числе дихлорид бис(циклопентадиенил)гафния(IV) , дигидрид бис(циклопентадиенил)гафния(IV) и диметилбис(циклопентадиенил)гафния(IV).

Катионные гафноценовые комплексы, постметаллоценовые катализаторы , используются в промышленных масштабах для полимеризации алкенов. [19] [20]
Дополнительное чтение
[ редактировать ]- Уитби, Р.Дж.; Диксон, С.; Мэлони, PR; Делерив, П.; Гудвин, Би Джей; Паркс, диджей; Уилсон, ТМ (2006). «Идентификация низкомолекулярных агонистов орфанных ядерных рецепторов, гомолога рецептора печени-1 и стероидогенного фактора-1». Журнал медицинской химии . 49 (23): 6652–6655. дои : 10.1021/jm060990k . ПМИД 17154495 .
- Касаткин А.; Уитби, Р.Дж. (1999). «Введение 1-хлор-1-литиоалкенов в органоцирконоцены. Универсальный синтез стереоопределенных ненасыщенных систем». Журнал Американского химического общества . 121 (30): 7039–7049. дои : 10.1021/ja9910208 .
Ссылки
[ редактировать ]- ^ Юэн, Дж.А.; Джонс, РЛ; Разави, А.; Феррара, доктор юридических наук (1988). «Синдиоспецифическая полимеризация пропилена с металлоценами группы IVB». Журнал Американского химического общества . 110 (18): 6255–6256. дои : 10.1021/ja00226a056 . ПМИД 22148816 .
- ^ А. Морин Руи (19 апреля 2004 г.). «Приходит цирконийорганическая химия» . Новости химии и техники . 82 (16): 36–39. doi : 10.1021/cen-v082n015.p035 . ISSN 0009-2347 .
- ^ Г. Уилкинсон; П.Л. Паусон; Дж. М. Бирмингем; Ф. А. Коттон (1953). «Бис-циклопентадиенильные производные некоторых переходных элементов». Журнал Американского химического общества . 75 (4): 1011–1012. дои : 10.1021/ja01100a527 .
- ^ Джеймс, Б.Д.; Нанда, РК; Уолбридж, MGH (1967). «Реакции оснований Льюиса с тетрагидроборатными производными элементов группы IVa. Получение новых форм гидрида циркония». Неорганическая химия . 6 (11): 1979–1983. дои : 10.1021/ic50057a009 .
- ^ Уэйлс, ПК; Вейгольд, Х. (1970). «Гидридокомплексы циркония I. Получение». Журнал металлоорганической химии . 24 (2): 405–411. дои : 10.1016/S0022-328X(00)80281-8 .
- ^ Уэйлс, ПК; Вейгольд, Х. (1970). «Гидридокомплексы циркония II. Реакции дициклопентадиенилциркония дигидрида с карбоновыми кислотами». Журнал металлоорганической химии . 24 (2): 413–417. дои : 10.1016/S0022-328X(00)80282-X .
- ^ Уэйлс, ПК; Вейгольд, Х.; Белл, AP (1971). «Гидридокомплексы циркония». Журнал металлоорганической химии . 27 (3): 373–378. дои : 10.1016/S0022-328X(00)82168-3 .
- ^ Негиси, Эй-Ичи; Такахаши, Тамоцу (1988). «Цирконийорганические соединения в органическом синтезе». Синтез . 1988 : 1–19. дои : 10.1055/s-1988-27453 .
- ^ «Открытие реакции ZACA — асимметрического карбоалюминирования алкенов, катализируемого Zr» . Аркивок . 2011 (8): 34. 2010. doi : 10.3998/ark.5550190.0012.803 . hdl : 2027/spo.5550190.0012.803 .
- ^ Джонс, Кристофер Г.; Асай, Мэтью; Ким, Ли Джун; Кляйнсассер, Джек Ф.; Саха, Амбарнейл; Фултон, Тайлер Дж.; Беркли, Кевин Р.; Кашио, Дуилио; Малютин Андрей Георгиевич; Конли, Мэтью П.; Штольц, Брайан М.; Лавалло, Винсент; Родригес, Хосе А.; Нельсон, Осия М. (6 сентября 2019 г.). «Характеристика реакционноспособных металлоорганических соединений с помощью MicroED» . Центральная научная служба ACS . 5 (9): 1507–1513. дои : 10.1021/accentsci.9b00403 . ПМК 6764211 . ПМИД 31572777 .
- ^ Макнайт, Эндрю Л.; Уэймут, Роберт М. (1998). «Катализаторы группы 4анса-циклопентадиенил-амидо для полимеризации олефинов». Химические обзоры . 98 (7): 2587–2598. дои : 10.1021/cr940442r . ПМИД 11848972 .
- ^ Альт, Хельмут Г.; Кёппль, Александр (2000). «Влияние природы металлоценовых комплексов металлов IV группы на их эффективность в каталитической полимеризации этилена и пропилена». Химические обзоры . 100 (4): 1205–1222. дои : 10.1021/cr9804700 . ПМИД 11749264 .
- ^ Сунь, Руен Чу; Окабе, Масами; Коффен, Дэвид Л.; Шварц, Джеффри (1997). «Аллиловые спирты путем переноса алкена от циркония к цинку: 1-[( трет -бутилдифенилсилил)окси]-дец-3-ен-5-ол». Органические синтезы . 74 : 205. дои : 10.15227/orgsyn.071.0083 .
- ^ Филлери, Шон Ф.; Ричард Дж. Уитби; Джордж Дж. Гордон; Тим Люкер (1997). «Тандемные реакции на цирконоценовой матрице» . Чистая и прикладная химия . 69 (3): 633–638. дои : 10.1351/pac199769030633 .
- ^ Негиси, Эй-Ичи (1991). «Бициклизация энинов, стимулируемая цирконием». Комплексный органический синтез . стр. 1163–1184. дои : 10.1016/B978-0-08-052349-1.00149-9 . ISBN 978-0-08-052349-1 .
- ^ Томас, Э.; Диксон, С.; Уитби, Р.Дж. (2006). «Перегруппировка в цирконий-алкенилиден при внедрении дигалокарбеноидов и ацетилидов в цирконациклы» . Angewandte Chemie, международное издание . 45 (42): 7070–7072. дои : 10.1002/anie.200602822 . ПМИД 17009379 .
- ^ Ронг, Йи; Аль-Харби, Ахмед; Паркин, Джерард (2012). «Сильно переменные валентные углы Zr–CH 2 –Ph в тетрабензилцирконии: анализ режимов координации бензильных лигандов» . Металлоорганические соединения . 31 (23): 8208–8217. дои : 10.1021/om300820b .
- ^ Эллис, Дж. Э. (2003). «Анионы карбонила металлов: из [Fe(CO) 4 ] 2− [Hf(CO) 6 ] 2− и далее». Металлоорганические соединения . 22 : 3322–3338. doi : 10.1021/om030105l .
- ^ Чам, PS; Своггер, К.В. (2008). «Технологии олефиновых полимеров - история и последние достижения в химической компании Dow». Прогресс в науке о полимерах . 33 : 797–819. doi : 10.1016/j.progpolymsci.2008.05.003 .
- ^ Клосин Дж.; Фонтейн, ПП; Фигероа, Р. (2015). «Разработка молекулярных катализаторов группы IV для высокотемпературных реакций сополимеризации этилена с Α-олефином» . Отчеты о химических исследованиях . 48 (7): 2004–2016. doi : 10.1021/acs.accounts.5b00065 . ПМИД 26151395 .
