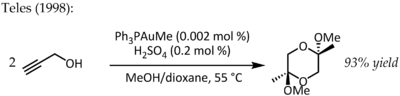Золотоорганическая химия
Золотоорганическая химия – это изучение соединений, содержащих золото – углерод связи . Они изучаются в академических исследованиях, но в остальном широкого применения не получили. Доминирующими степенями окисления для золотоорганических соединений являются I с координационным числом 2 и линейной молекулярной геометрией и III с CN = 4 и плоско-квадратной молекулярной геометрией . [1] [2] [3]
Золото(Я)
[ редактировать ]Комплексы золота(I) представляют собой 2-координатные, линейные, диамагнитные , с 14 электронными группами. [1] [2] [3] Обычно они существуют в виде аддуктов LAuR с лигандом L, например, трифенилфосфином или изоцианидом. Лиганд предотвращает восстановление Au(I) до металлического Au(0) с димеризацией органического остатка. Золото(I) также может существовать в виде аурата M[AuR 2 ] ( атный комплекс ), при этом катион обычно снабжается комплексообразователем для повышения стабильности. АУР 2 − анион также линеен, как и другие M(d 10 ) такие виды, как Hg(Me) 2 и Pd(Me) 2 2+ . Известно, что золото образует ацетилиды (способные образовывать полимерные структуры), карбены и карбины. [ нужна ссылка ] . Классический метод получения соединений LAuR заключается в реакции реактива Гриньяра с галогенидом золота(I) . Последующая реакция с литийорганическим соединением R-Li образует атный комплекс.
В особой группе соединений арильный атом углерода действует как мостик между двумя атомами золота. Одно из таких соединений, (MesAu) 5 , образуется в реакции между Au(CO)Cl и мезитилом Гриньяра. Углерод может координироваться с золотом до значения до 6. Соединения типа C(AuL) 4 изолобальны ) метану, а соединения типа C(AuL 5 + изолобальный с ионом метана. Эти гиперкоординированные золотоорганические кластеры часто стабилизируются за счет аурофильных взаимодействий между золотыми центрами с формально закрытой оболочкой. [4]
Соединения цианида золота ( MAu(CN) 2 ) имеют определенное значение для цианирования золота , процесса извлечения золота из низкосортной руды. Связь углерода с металлом в цианидах металлов обычно ионная, но существуют доказательства того, что связь C-Au в ионе цианида золота является ковалентной. [5]
Золото(III)
[ редактировать ]Комплексы золота(III) четырехкоординатные, плоскоквадратные, диамагнитные , токсичные, с 16 видами электронов. Когда формальное координационное число меньше 4, лиганды, такие как хлор, могут компенсировать его, образуя мостиковый лиганд. Еще одна стратегия – внутримолекулярное хелатирование. В целом соединения золота(III) токсичны и поэтому менее изучены, чем золото(I). Комплексы моноарилзолота(III) представляют собой один хорошо изученный класс комплексов. Их часто получают прямым электрофильным аурированием аренов AuCl 3 . [6] Гомолептические комплексы тетраалкилаурата(III) (например, Li[AuMe 4 ]) также хорошо изучены. [7]
Золотой катализ
[ редактировать ]Общие соображения
[ редактировать ]Реакции, катализируемые золотом, делятся на две основные категории: гетерогенный катализ , включающий катализаторы с помощью наночастиц золота (например, Au/TiO 2 ) и тиоловых монослоев золотых поверхностей, и катализаторы на носителе из оксида алюминия, включая Au/CeO 2 на носителе из оксида алюминия . Эти катализаторы были исследованы для промышленно важных процессов, таких как окисление спиртов, окисление монооксида углерода (CO) и различных реакций селективного гидрирования (например, бутадиена в бутен). Хотя зачастую они эффективны и демонстрируют полезную или уникальную селективность, существует значительная неопределенность в отношении механизма процессов, катализируемых различными гетерогенными золотыми катализаторами, даже по сравнению с другими гетерогенными катализаторами на основе переходных металлов.
Напротив, в гомогенном катализе золотом используются простые или связанные с лигандами соединения золота (I) или золота (III), которые растворяются в органических растворителях и используются для синтеза тонких химических веществ в органической химии. [8] [9] бинарные галогениды золота и простые комплексы, включая хлорид золота(I) , хлорид золота(III) и золотохлористоводородную кислоту В качестве комплексов использованы . Однако эти источники золота быстро приводят к появлению нечетких и легко дезактивируемых (путем восстановления до Au 0 ) активные катализаторы в растворе. Разработка четко определенных фосфин- или NHC-лигированных комплексов золота (I) стала важным достижением и привела к значительному увеличению интереса к синтетическим применениям золотого катализа. Лигированные комплексы золота(I) обычно готовят и хранят в виде стабильных (но нереакционноспособных) хлоридов LAuCl, например, хлор(трифенилфосфин)золота(I) , которые обычно активируются путем отщепления галогенидов с помощью солей серебра, таких как AgOTf, AgBF4 . , или AgSbF 6 для получения катионной разновидности золота(I). [10] [11] Хотя координационно-ненасыщенный комплекс «LAu + «предположительно образуется из смеси LAuCl/AgX, точная природа катионных форм золота и роль соли серебра остаются несколько спорными. [12] [13] [14] Пара . -нитробензоат, бистрифлимид и некоторые нитрильные комплексы представляют собой каталитически активные, но изолируемые предкатализаторы, не содержащие серебра
Катионное золото(I) образует π-комплексы с алкеновыми или алкиновыми связями, следуя модели Дьюара-Чатта-Дункансона . Золото, конечно, не единственный металл, демонстрирующий такой тип связи и реакционную способность; некоторые ионы металлов, изолобальные с простым протоном (т.е. пустая s-орбиталь), тоже имеют такую особенность: например, ртуть(II) и платина(II). Электрофильные ионы и подобные им комплексы с сильной склонностью к образованию π-комплексов обычно известны как пи (π)-кислоты (см. Также: взаимодействие катион-пи ). [15]
Комплексы золото(I)-алкен и -алкин электрофильны и чувствительны к нуклеофильной атаке. При оксимеркурации образующиеся ртутьорганические соединения образуются стехиометрически, и для высвобождения продукта требуется дополнительный этап. В случае золота протонолиз связи Au-C замыкает каталитический цикл, позволяя координировать другой субстрат. Некоторые практические преимущества катализа золотом(I) включают: 1) стабильность на воздухе (из-за высокого окислительного потенциала Au(I)), 2) толерантность к примеси влаги (из-за его низкой оксофильности) и 3) относительно низкую токсичность по сравнению с катализом золота(I). другие пи-кислоты (например, Pt(II) и Hg(II)). Химически комплексы Au(I) обычно не подвергаются окислению до более высоких степеней окисления, а Au(I)-алкилы и -винилы не подвержены отщеплению β-гидрида. [16]
Историческое развитие
[ редактировать ]В 1976 году Томас и его коллеги сообщили о превращении фенилацетилена в ацетофенон с использованием золотохлористоводородной кислоты с выходом 37%. [17] В этой реакции золото(III) использовалось в качестве гомогенного катализатора, заменяющего ртуть при оксимеркурации. В том же исследовании указан опубликованный выход >150%, что указывает на катализ, который, возможно, не был признан химиками.
В 1991 году Утимото провёл реакцию золота(III) (NaAuCl 4 ) с алкинами и водой. [18] Телес выявил главный недостаток этого метода, поскольку Au(III) быстро восстанавливался до каталитически мертвого металлического золота, и в 1998 году вернулся к теме Au(I) на лигандной основе для того же превращения: [19]
Эта конкретная реакция продемонстрировала фантастическую каталитическую эффективность и в ближайшие годы вызовет шквал исследований по использованию комплексов фосфинзолота(I) для активации кратных связей CC. [20] Несмотря на меньшую стабильность комплексов золота(III) в каталитических условиях, простой AuCl 3 также оказался в ряде случаев эффективным катализатором. Например, Хашми сообщил о катализируемой AuCl 3 реакции алкин/ фуран Дильса-Альдера - типе циклоприсоединения, который обычно не происходит - для синтеза 2,3-дизамещенных фенолов : [21]
Дальнейшие механистические исследования пришли к выводу, что это не согласованное преобразование, а скорее начальное гидроарилирование алкинов, за которым следует серия неочевидных внутримолекулярных перегруппировок, завершающихся 6π-электроциклизацией и рероматизацией.
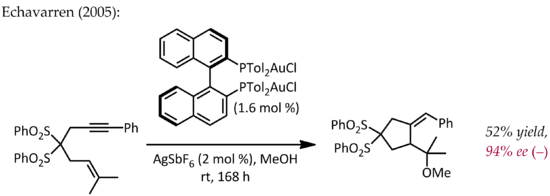
Релятивистские эффекты существенны в золотоорганической химии из-за большого ядерного заряда металла ( Z = 79). В результате релятивистски расширенных 5 d- орбиталей фрагмент LAu может стабилизировать соседний карбокатион посредством донорства электронов на пустую орбиталь p -типа. Таким образом, в дополнение к ожидаемой карбокатионоподобной реакционной способности эти катионы также проявляют значительный карбеновый характер - свойство, которое использовалось в каталитических превращениях, таких как циклопропанирование и внедрение CH. [22] Эфиры пропаргила могут служить предшественниками катионных промежуточных соединений золота и винилкарбена, которые могут согласованно реагировать с алкенами с образованием продукта циклопропанирования. Использование хирального лиганда ( ( R )-DTBM-SEGPHOS ) привело к получению уровней энантиоселективности от хороших до превосходных. [23]


Хотя Эчаваррен первым сообщил о получении хиральных комплексов бисфосфиндизолота(I) для энантиоселективного катализа золотом, протекающего по типичному механизму пи-активации, [24] Ранний, нетипичный пример энантиоселективного катализа золотом был описан Хаяши и Ито в 1986 году. [25] В этом процессе бензальдегид и метилизоцианоацетат подвергаются циклизации в присутствии хирального ферроценилфосфинового лиганда и комплекса бис(изоцианид)золота(I) с образованием хирального оксазолина . Поскольку оксазолины можно гидролизовать с образованием 1,2-аминоспирта, эта реакция представляет собой первый пример каталитической асимметричной альдольной реакции .
В отличие от других описанных выше реакций, эта реакция не включает активацию золотом двойной или тройной связи CC. В простой механистической картине золото(I) одновременно координируется с двумя фосфиновыми лигандами и изоцианатной группой углерода. [26] который затем подвергается атаке карбонильной группы. Дальнейшие исследования способа связи Au(I) показывают, что эту простую картину, возможно, придется пересмотреть.
Гетерогенный золотой катализ – более древняя наука. Золото является привлекательным металлом для использования из-за его устойчивости к окислению и разнообразия морфологии, например, в материалах кластеров золота . Было показано, что золото эффективно при низкотемпературном окислении CO и гидрохлорировании ацетилена до винилхлоридов. Точная природа каталитического центра в этом типе процесса дискутируется. [27] Представление о том, что золото может катализировать реакцию, не означает, что это единственный способ. Однако другие металлы могут выполнить ту же работу недорого, особенно в последние годы железо (см. Железоорганическую химию ).
Реакции, катализируемые золотом
[ редактировать ]Золото катализирует многие органические превращения, обычно образование связи углерод-углерод из Au (I) и образование связи CX (X = O, N) из состояния Au (III) из-за более жесткой кислотности Льюиса этого иона. За последнее десятилетие несколько исследований продемонстрировали, что золото может эффективно катализировать реакции кросс-сочетания CC и C-гетероатомов, которые протекают через цикл Au(I)/Au(III). [28] Хун К. Шен обобщил гомогенные реакции, образующие циклические соединения, на 4 основные категории: [29]
- гетероатома нуклеофильное присоединение к ненасыщенным связям CC, особенно с образованием небольших гетероциклов (фураны, пирролы, тиофены)
- Гидроарилирование: в основном реакция Фриделя-Крафтса с использованием металлалкиновых комплексов. Пример реакции мезитилена с фенилацетиленом : [30]
- Циклизация енина, в частности циклоизомеризация , одним из ранних примеров является циклоизомеризация 5-экзо-диг-1,6 енина: [31]
- реакции циклоприсоединения с ранним примером циклоприсоединения оксида нитрила к алкину. [32]
Другие реакции включают использование золота для активации связи C–H. [33] и альдольные реакции. Золото также катализирует реакции сочетания . [34]
Ограничения
[ редактировать ]В то время как катализируемая золотом гидрофункционализация алкинов, алленов и аллильных спиртов [35] легко происходит в сравнительно мягких условиях, неактивированные алкены в большинстве случаев остаются плохими субстратами. [36] во многом из-за устойчивости промежуточных комплексов алкилзолота(I) к протодеаурации. [37] Развитие межмолекулярных превращений, катализируемых золотом, также отставало от развития внутримолекулярных. [38]
Ссылки
[ редактировать ]- ^ Jump up to: а б Эльшенбройх К. и Зальцер А. (1992) Металлоорганические соединения: краткое введение . Wiley-VCH: Вайнхайм. ISBN 3-527-28165-7
- ^ Jump up to: а б Пэриш, Р.В. (1997). «Золотоорганическая химия: II реакции» . Золотой бюллетень . 30 (2): 55–62. дои : 10.1007/BF03214757 .
- ^ Jump up to: а б Пэриш, Р.В. (1998). «Золотоорганическая химия: III применения» . Золотой бюллетень . 31 : 14–21. дои : 10.1007/BF03215470 .
- ^ Шмидбаур, Хуберт; Шир, Аннет (5 декабря 2011 г.). «Аурофильные взаимодействия как предмет текущих исследований: обновленная информация». Обзоры химического общества . 41 (1): 370–412. дои : 10.1039/C1CS15182G . ISSN 1460-4744 . ПМИД 21863191 .
- ^ Ван, XB; Ван, ЮЛ; Ян, Дж.; Син, XP; Ли, Дж.; Ван, Л.С. (2009). «Свидетельства значительной ковалентной связи в Au (CN) 2 − ". Журнал Американского химического общества . 131 (45): 16368–70. doi : 10.1021/ja908106e . PMID 19860420 .
- ^ Хараш, М.С.; Исбелл, Гораций С. (1 августа 1931 г.). «Химия органических соединений золота. III. Прямое введение золота в ароматическое ядро (предварительное сообщение)». Журнал Американского химического общества . 53 (8): 3053–3059. дои : 10.1021/ja01359a030 . ISSN 0002-7863 .
- ^ Райс, Гэри В.; Тобиас, Р. Стюарт. (01.10.1975). «Синтез тетраметилаурата (III). Структуры диметилаурата лития и тетраметилаурата лития в растворе». Неорганическая химия . 14 (10): 2402–2407. дои : 10.1021/ic50152a020 . ISSN 0020-1669 .
- ^ Золотой катализ для органического синтеза Ф. Дин Тосте (редактор) Тематическая серия открытого доступа в журнале органической химии Beilstein
- ^ Раубенхаймер, Х.Г.; Шмидбаур, Х. (2014). «Поздний старт и удивительный подъем в химии золота». Журнал химического образования . 91 (12): 2024–2036. Бибкод : 2014JChEd..91.2024R . дои : 10.1021/ed400782p .
- ^ Раньери, Беатрис; Эскофет, Имма; Эчаваррен, Антонио М. (24 июня 2015 г.). «Анатомия золотых катализаторов: факты и мифы» . Орг. Биомол. Хим . 13 (26): 7103–7118. дои : 10.1039/c5ob00736d . ISSN 1477-0539 . ПМЦ 4479959 . ПМИД 26055272 .
- ^ Ван, И-Мин; Лакнер, Аарон Д.; Тосте, Ф. Дин (14 ноября 2013 г.). «Разработка катализаторов и лигандов для энантиоселективного катализа золота» . Отчеты о химических исследованиях . 47 (3): 889–901. дои : 10.1021/ar400188g . ПМЦ 3960333 . ПМИД 24228794 .
- ^ Жданко, Александр; Майер, Мартин Э. (9 сентября 2015 г.). «Объяснение «эффектов серебра» в катализируемом золотом (I) гидроалкоксилировании алкинов». АКС-катализ . 5 (10): 5994–6004. дои : 10.1021/acscatal.5b01493 .
- ^ Хомс, Анна; Эскофет, Имма; Эчаваррен, Антонио М. (2013). «Об эффекте серебра и образовании хлоридно-мостиковых комплексов дизолота» . Органические письма . 15 (22): 5782–5785. дои : 10.1021/ol402825v . ПМЦ 3833279 . ПМИД 24195441 .
- ^ Ван, Давэй; Цай, Ронг; Шарма, Шрипад; Жирак, Джеймс; Тумманапелли, Шраван К.; Ахмедов, Новруз Г.; Чжан, Хуэй; Лю, Синбо; Петерсен, Джеффри Л. (18 мая 2012 г.). « Эффект серебра» в катализе золота (I): упущенный из виду важный фактор». Журнал Американского химического общества . 134 (21): 9012–9019. дои : 10.1021/ja303862z . ПМИД 22563621 .
- ^ Фюрстнер, А.; Дэвис, PW (2007). «Каталитическая карбофильная активация: катализ π-кислотами платины и золота». Angewandte Chemie, международное издание . 46 (19): 3410–3449. дои : 10.1002/anie.200604335 . ПМИД 17427893 .
- ^ Шен, ХК (2008). «Последние достижения в синтезе гетероциклов и карбоциклов посредством гомогенного золотого катализа. Часть 1: реакции присоединения гетероатомов и гидроарилирования алкинов, алленов и алкенов». Тетраэдр . 64 (18): 3885–3903. дои : 10.1016/j.tet.2008.01.081 .
- ^ Норман, Китайская республика; Парр, WJE; Томас, CB (1976). «Реакции алкинов, циклопропанов и производных бензола с золотом (III)». Журнал Химического общества, Perkin Transactions 1 (18): 1983. doi : 10.1039/P19760001983 .
- ^ Фукуда, Ю.; Утимото, К. (1991). «Эффективное преобразование неактивированных алкинов в кетоны или ацетали с помощью катализатора золото (III)». Журнал органической химии . 56 (11): 3729–3731. дои : 10.1021/jo00011a058 .
- ^ Телес, Дж. Х.; Броде, С.; Чабанас, М. (1998). «Катионные комплексы золота(I): высокоэффективные катализаторы присоединения спиртов к алкинам» . Angewandte Chemie, международное издание . 37 (10): 1415–1418. doi : 10.1002/(SICI)1521-3773(19980605)37:10<1415::AID-ANIE1415>3.0.CO;2-N . ПМИД 29710887 .
- ^ Ньюджент, Вашингтон (2012). « События «черного лебедя» в органическом синтезе». Angewandte Chemie, международное издание . 51 (36): 8936–49. дои : 10.1002/anie.201202348 . ПМИД 22893229 .
- ^ Хашми, СПРОСИТЕ; Фрост, ТМ; Летучие мыши, JW (2000). «Высокоселективный синтез арена, катализируемый золотом». Журнал Американского химического общества . 122 (46): 11553–11554. дои : 10.1021/ja005570d .
- ^ Горин, Дэвид Дж.; Тосте, Ф. Дин (2007). «Релятивистские эффекты в гомогенном золотом катализе» . Природа . 446 (7134): 395–403. Бибкод : 2007Natur.446..395G . дои : 10.1038/nature05592 . ПМИД 17377576 . S2CID 4429912 .
- ^ Йоханссон, Магнус Дж.; Горин, Дэвид Дж.; Стабен, Стивен Т.; Тосте, Ф. Дин (30 ноября 2005 г.). «Стереоселективное циклопропанирование олефинов, катализируемое золотом (I)». Журнал Американского химического общества . 127 (51): 18002–18003. дои : 10.1021/ja0552500 . ПМИД 16366541 .
- ^ Муньос, М. Пас; Адрио, Хавьер; Карретеро, Хуан Карлос; Эчаваррен, Антонио М. (12 февраля 2005 г.). «Эффекты лиганда в катализируемой золотом и платиной циклизации энинов: хиральные комплексы золота для энантиоселективной алкоксициклизации». Металлоорганические соединения . 24 (6): 1293–1300. дои : 10.1021/om0491645 .
- ^ Ито, Ю.; Савамура, М.; Хаяши, Т. (1986). «Каталитическая асимметричная альдольная реакция: реакция альдегидов с изоцианоацетатом, катализируемая хиральным комплексом ферроценилфосфин-золото (I)». Журнал Американского химического общества . 108 (20): 6405–6406. дои : 10.1021/ja00280a056 .
- ^ Тони, А.; Пастор, С.Д. (1990). «Хиральная кооперативность: природа диастереоселективной и энантиоселективной стадии в катализируемой золотом (I) альдольной реакции с использованием хиральных ферроцениламиновых лигандов». Журнал органической химии . 55 (5): 1649–1664. дои : 10.1021/jo00292a046 .
- ^ Хатчингс, Дж.Дж.; Бруст, М.; Шмидбаур, Х. (2008). «Золото — вводный взгляд». Обзоры химического общества . 37 (9): 1759–65. дои : 10.1039/b810747p . ПМИД 18762825 .
- ^ Ниджамудхин, А.; Датта, Аян (2020). «Реакции перекрестного сочетания, катализируемые золотом: обзор стратегий проектирования, механистических исследований и приложений». Химия: Европейский журнал . 26 (7): 1442–1487. дои : 10.1002/chem.201903377 . ПМИД 31657487 . S2CID 204947412 .
- ^ Шен, ХК (2008). «Последние достижения в синтезе карбоциклов и гетероциклов посредством гомогенного золотого катализа. Часть 2: Циклизации и циклоприсоединения». Тетраэдр . 64 (34): 7847–7870. дои : 10.1016/j.tet.2008.05.082 .
- ^ Ритц, Монтана; Соммер, К. (2003). «Катализируемое золотом гидроарилирование алкинов». Европейский журнал органической химии . 2003 (18): 3485–3496. дои : 10.1002/ejoc.200300260 .
- ^ Ньето-Оберхубер, К.; Муньос, член парламента; Бунюэль, Э.; Невадо, К.; Карденас, диджей; Эчаваррен, AM (2004). «Катионные комплексы золота (I): высокоалкинофильные катализаторы экзо- и эндо-циклизации энинов». Angewandte Chemie, международное издание . 43 (18): 2402–2406. дои : 10.1002/anie.200353207 . ПМИД 15114573 .
- ^ Гаспаррини, Ф.; Джованноли, М.; Мисити, Д.; Натил, Г.; Пальмиери, Г.; Мареска, Л. (1993). «Катализируемый золотом (III) однореакторный синтез изоксазолов из концевых алкинов и азотной кислоты». Журнал Американского химического общества . 115 (10): 4401–4402. дои : 10.1021/ja00063a084 .
- ^ Хоффманн-Рёдер, А.; Краузе, Н. (2005). «Золотые ворота к катализу». Органическая и биомолекулярная химия . 3 (3): 387–91. дои : 10.1039/b416516k . ПМИД 15678171 .
- ^ Вегнер, ХА; Аузиас, М. (2011). «Золото для реакций сочетания CC: катализатор швейцарского армейского ножа?» . Angewandte Chemie, международное издание . 50 (36): 8236–47. дои : 10.1002/anie.201101603 . ПМИД 21818831 .
- ^ Бандини, Марко (01 февраля 2011 г.). «Аллиловые спирты: устойчивые источники каталитических энантиоселективных реакций алкилирования». Angewandte Chemie, международное издание . 50 (5): 994–995. дои : 10.1002/anie.201006522 . hdl : 11585/96637 . ISSN 1521-3773 . ПМИД 21268189 .
- ^ Чжан, Жибин; Ли, Сон Ду; Виденхофер, Росс А. (22 апреля 2009 г.). «Межмолекулярное гидроаминирование этилена и 1-алкенов циклическими мочевинами, катализируемое ахиральными и хиральными комплексами золота (I)» . Журнал Американского химического общества . 131 (15): 5372–5373. дои : 10.1021/ja9001162 . ISSN 0002-7863 . ПМЦ 2891684 . ПМИД 19326908 .
- ^ ЛаЛонд, Ребекка Л.; Брензович, Уильям Э. младший; Бенитес, Диего; Ткачук Екатерина; Келли, Котаро; III, Уильям А. Годдард; Тосте, Ф. Дин (2010). «Комплексы алкилзолота путем внутримолекулярной аминоаурации неактивированных алкенов» . Химическая наука . 1 (2): 226. дои : 10.1039/C0SC00255K . ПМЦ 3866133 . ПМИД 24358445 .
- ^ Мураторе, Майкл Э.; Хомс, Анна; Обрадорс, Карла; Эчаваррен, Антонио М. (01 ноября 2014 г.). «Решение проблемы межмолекулярного циклоприсоединения алкинов и алленов, катализируемого золотом (I)» . Химия: Азиатский журнал . 9 (11): 3066–3082. дои : 10.1002/asia.201402395 . ISSN 1861-471X . ПМК 4676923 . ПМИД 25048645 .