Висмуторганическая химия

Висмуторганическая химия — химия металлоорганических соединений, содержащих углерода с висмутом химическую связь . Приложений мало. [1] [2] Основными степенями окисления висмута являются Bi(III) и Bi(V), как и во всех элементах более высокой группы 15 . Энергия связи с углеродом в этой группе убывает в ряду P > As > Sb > Bi. [3] Первое сообщение об использовании висмута в органической химии было при окислении спиртов Фредериком Челленджером в 1934 году (с использованием Ph 3 Bi(OH) 2 ). [4] Знания о метилированных формах висмута в окружающей среде и биологических средах ограничены. [5]
Открытие
[ редактировать ]Триэтилвисмут, первое известное висмуторганическое соединение, был получен в 1850 году Лёвигом и Швейцером из йодэтана и сплава калия с висмутом. Как и большинство соединений триалкилвисмута, BiEt 3 имеет чрезвычайно резкий и неприятный запах и самопроизвольно окисляется на воздухе. [6] Химии этих комплексов впервые стало уделяться значительное внимание, когда стали доступны реактивы Гриньяра и литийорганические соединения .
Биорганические соединения(III)
[ редактировать ]Свойства и структура
[ редактировать ]
Триорганические соединения висмута (III) являются мономерами с пирамидальной структурой, напоминающей химию фосфорорганических соединений (III). Однако галогениды принимают гипервалентные структуры. Эту тенденцию иллюстрирует листовая структура дихлорида метилвисмута . [7]
Большинство алифатических соединений висмута(III) легко окисляются, причем более легкие соединения являются пирофорными . Диалкилгалобисмутины нельзя хранить, так как они разлагаются даже в инертной атмосфере. [8] : 413
Диарилвисмутины являются одними из самых мощных известных средств от чихания. [8] : 413
Висмуторганические гетероциклы основаны на Bi(III). Циклическое соединение бисмол , структурный аналог пиррола , не выделено, но известны замещенные бисмолы. [9] Бисмабензол был обнаружен в лаборатории. [10]
Синтез
[ редактировать ]Наиболее общая и широко используемая методика синтеза гомолептических триалкил- и триарилвисмутовых комплексов заключается в взаимодействии BiX 3 с литийорганическими или - магниевыми реагентами: [6]
- BiCl 3 + 3RMgX → R 3 Bi + 3MgXCl
- BiCl 3 + 3LiR → BiR 3 + 3LiCl.
впервые были получены триорганические соединения висмута : Вместо них из K 3 Bi и галогенорганических соединений [6]
- К 3 Би + 3RX → BiR 3 + 3KX.
Этот метод, как правило, более сложен и дает меньший выход. Однако по состоянию на 2006 год он оставался единственным методом, например, (Me 3 Si) 3 Bi. синтеза [6]
Соединения триарила висмута (III) обычно представляют собой стабильные на воздухе кристаллические твердые вещества, и заместители вступают в реакцию до образования связей углерод-висмут в соответствующих условиях: [11]

Асимметричные висмуторганические соединения наиболее естественно образуются из (нестабильных) висмутгалогенидов RBiX 2 и R 2 BiX. [6]
Реакции
[ редактировать ]В промышленности соединения триарилвисмута катализируют различные полимеризации алкенов и алкинов . [8] : 415
Соединения триарилвисмута имеют очень ограниченное применение в органическом синтезе. [12] Их связи слабы и легко вытесняются другими элементами, как металлическими, так и неметаллическими. [8] : 413 Такие реакции протекают легче, чем для более легких конгенеров. Разумеется, трифенилвисмут претерпевает перераспределение вместе со своим тригалогенидом с образованием смешанных производных, таких как хлорид дифенилвисмута (Ph 2 BiCl). [13] Интересно, что реагенты висмута(III) могут передавать заместители соединениям таллия(III) : [8] : 414
Bi(CH 2 =CMe) 3 + 3 TlCl 3 → (CH 2 =CMe) 2 TlCl + 2 BiCl 3 при −40 °C
Соединения триарилвисмута (III) также можно использовать в превращениях, образующих связи C–N и C–C, с подходящим металлическим сокатализатором. Например, Бартон и его коллеги продемонстрировали, что амины могут быть N -арилированы реагентом висмута (III) в присутствии соли меди (II). [14]

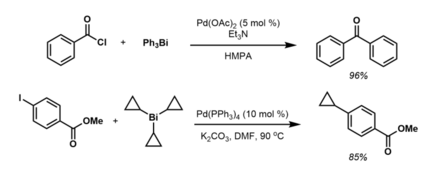
Аналогично ацилхлориды реагируют под катализом Pd(0) с образованием различных фенилкетонов. [15] Хотя формально это не арены, реагенты трициклопропилвисмута (III) реагируют с арилгалогенидами и трифлатами под катализом Pd (0) аналогичным образом, образуя различные арил- и гетероарилциклопропаны: [16]
Bi(V)органические соединения
[ редактировать ]Структура и стабильность
[ редактировать ]Термическая устойчивость соединений R 5 M снижается в ряду As > Sb > Bi. Арильные соединения более стабильны, чем алкильные соединения. Me 5 Bi взрывоопасно разлагается при 20°C. [ нужна ссылка ]
Природа арильных лигандов важна для определения того, является ли геометрия комплекса тригонально-бипирамидальной или плоско-квадратной, а также его цвета. [6] Обычно гомолептические соединения типа Ar 5 Bi имеют квадратно-пирамидальную структуру. Пентафениловое соединение имеет интенсивную окраску и термохромность , возможно, из-за равновесия между геометриями. [17]
Карбоксилаты редко образуют хелатные комплексы висмута. Вместо этого висмуторганические карбоксилаты обычно являются полимерными, при этом каждый кислород карбоксилата координируется с различным атомом висмута. [18] : 330–332, 344–345 Этого нельзя сказать о ксантогенатах . [18] : 334, 340
Галогениды висмута, координированные с аренами, представляют собой комплексы рояль-табурет . [18] : 337, 341–343
Синтез из соединений висмута(III)
[ редактировать ]Интересно, что хотя неорганических Bi очень мало V Известны соединения, имеется большое разнообразие пентакоординированных висмуторганических комплексов. [8] : 415 Триарилорганические комплексы висмута легко окисляются до комплексов висмута(V) при обработке хлором или бромом с образованием Ar 3 BiX 2 (X = Cl, Br). Вместо этого реакции с йодом вытесняют лиганды с образованием трехкоординированного Ar 3-x BiI x , тогда как реакции с фтором слишком энергичны, чтобы их можно было контролировать. [6]
Затем можно получить доступ к полноуглеродным висмуторганическим комплексам (V) путем замещения вновь образованной связи висмут-галоген алкилом или ариллитием или реактивом Гриньяра. Например:
- Me 3 Bi + SO 2 Cl 2 → Me 3 BiCl 2 + SO 2
- Me 3 BiCl 2 + 2 MeLi → Me 5 Bi + 2 LiCl
Нестабильный фиолетовый Ph 5 Bi был синтезирован первым. [6]
Bi(V) легко образует ониевый ион , например, путем протонирования п -толуолсульфоновой кислотой : [19]
- Ph 5 Bi + HO 3 SAr → Ph 4 Bi + [О 3 САр − ]
Пентафенилвисмут образует комплекс при обработке фениллитием : [20]
- Ph 5 Bi + PhLi → Li + [Ф 6 Би − ]
В органическом синтезе
[ редактировать ]Реагенты висмуторганический (V) полезны для широкого спектра органических преобразований. По сравнению со своими более легкими родственниками соединения Bi(V) являются сильными окислителями, дегидрирующими спирты всех видов до карбонила и расщепляющими гликоли до альдегидов. Они также занимаются арилпереносом . [6]
Соединения Ph 3 Bi(OOtBu) 2 , Ph 3 BiCO 3 и (Ph 3 BiCl) 2 O исследованы на окисление оксима , тиола , фенола и фосфина . [21] [ нужна страница ] В общем, окисление ускоряется, когда арильные лиганды имеют электроноакцепторные заместители и атакуют спирты раньше тиолов или селенидов. [8] : 416–417 Гидразины дегидрируются до азосоединений , а тиолы — до смеси сульфидов и дисульфидов. [8] : 417–418 Для высоких выходов необходимы сильно основные условия (при их отсутствии наиболее эффективным является карбонат), что позволяет предположить, что активными частицами являются оксиды триарилвисмута. Однако соединения пентаарилвисмута также поглощают водород. [8] : 416–417
В целом соединения висмута(V) арилируются неэффективно, передавая субстрату только один из пяти лигандов. [22] и оставляя после себя отходы триарилвисмута(III). [23] Повторное окисление Bi III комплекс к Би V труден и препятствует замыканию каталитического цикла вокруг этой химии. [22] Тем не менее, Ph 5 Bi и Ph 3 BiCl 2 арилируют 1,3-дикарбонилы и арены : [24]
В ходе реакции реагент висмута(V) теряет арильную группу и связывается с кислородом. Последующее арилирование и элиминирование асинхронны и согласованы: [23]

Соседние доноры электронных пар определяют региоселективность.
В присутствии соли меди такие реагенты арилируют амины и спирты. Под воздействием ультрафиолета они также моноарилатируют гликоли. Стерические затруднения определяют их высокую селективность: вторичные спирты арилируются по сравнению с третичными, а аксиальные спирты – по сравнению с экваториальными. [8] : 417–431
См. также
[ редактировать ]- Металлоорганическая химия висмута - лиганды висмута для переходных металлов.
Ссылки
[ редактировать ]- ^ Оллевье, Тьерри, изд. (2012). Органические реакции, опосредованные висмутом . Темы современной химии. Том. 311. дои : 10.1007/978-3-642-27239-4 . ISBN 978-3-642-27239-4 . S2CID 92683528 . [ нужна страница ]
- ^ фон Вангелин, Аксель Якоби (2004). «Висмутовые реагенты и катализаторы в органическом синтезе». Переходные металлы для органического синтеза . стр. 379–394. дои : 10.1002/9783527619405.ch2r . ISBN 9783527619405 .
- ^ К. Эльшенбройх, А. Металлоорганические соединения Зальцера : краткое введение (2-е изд.) ( 1992 ) из Wiley-VCH: Weinheim. ISBN 3-527-28165-7 . [ нужна страница ]
- ^ Челленджер, Фредерик; Ричардс, Освальд В. (1934). «94. Органопроизводные висмута и таллия». Журнал Химического общества (обновленный) : 405. doi : 10.1039/JR9340000405 .
- ^ Филелла, Монтсеррат (2010). «9. Алкильные производные висмута в экологических и биологических средах». Металлоорганические соединения в окружающей среде и токсикологии . Ионы металлов в науках о жизни. Том. 7. С. 303–318. дои : 10.1039/9781849730822-00303 . ISBN 978-1-84755-177-1 . ПМИД 20877811 .
- ^ Jump up to: а б с д и ж г час я Р., Кинг (2005). Энциклопедия неорганической химии . Том. Я: AC (2-е изд.). Уайли. стр. 345–369. ISBN 9780470860786 .
- ^ Альтхаус, Хенрик; Брюниг, Ханс Иоахим; Лорк, Энно (февраль 2001 г.). «Синтез и химия дигалогенидов метилсурьмы и метилвисмута: расширенный двумерный каркас в кристаллической структуре CH 3 BiCl 2 и молекулярные единицы в структурах [CH 3 ECl 2 (2,2'-бипиридин)] (E = Sb , Би)». Металлоорганические соединения . 20 (3): 586–589. дои : 10.1021/om000749i .
- ^ Jump up to: а б с д и ж г час я дж Фридман, Леон Д.; Доук, Джордж О. (1989). «Применение сурьмяорганических и висмуторганических соединений в органическом синтезе». В Хартли, Фрэнк Робинсон (ред.). Химия связи металл — углерод . (Патаи) Химия функциональных групп. Том. 5. Чичестер, Великобритания: Interscience . стр. 413–436. дои : 10.1002/9780470772263.ch9 . ISBN 0471915564 .
- ^ Кастер, Кеннет К. (1996). «Арсоли, стиболы и бисмоли». В Катрицки, Алан Р.; Рис, Чарльз Уэйн; Скривен, Эрик Ф.В. (ред.). Комплексная гетероциклическая химия II: Пятичленные кольца с одним гетероатомом и конденсированные карбоциклические производные . Пергамон. стр. 857–902. ISBN 978-0-08-042725-6 .
- ^ Ганьон, Александр; Дансеро, Жюльен; Ле Рох, Адриан (2 марта 2017 г.). «Висмуторганические реагенты: синтез, свойства и применение в органическом синтезе». Синтез . 49 (8): 1707–1745. дои : 10.1055/s-0036-1589482 .
- ^ Эбер, Мартин; Петио, Полина; Бенуа, Эмелин; Дансеро, Жюльен; Ахмад, Табинда; Ле Рох, Адриан; Оттенвальдер, Ксавьер; Ганьон, Александр (1 июля 2016 г.). «Синтез высокофункционализированных триарилвисмутинов путем манипулирования функциональными группами и использования в реакциях арилирования, катализируемых палладием и медью». Журнал органической химии . 81 (13): 5401–5416. дои : 10.1021/acs.joc.6b00767 . ПМИД 27231755 .
- ^ Фине, Жан Пьер (1 ноября 1989 г.). «Реакции арилирования с висмуторганическими реагентами». Химические обзоры . 89 (7): 1487–1501. дои : 10.1021/cr00097a005 .
- ^ Бартон, Дерек HR; Бхатнагар, Нирджа Ядав; Фине, Жан-Пьер; Мазервелл, Уильям Б. (январь 1986 г.). «Пятивалентные висмуторганические реагенты. Часть VI. Сравнительная миграционная способность арильных групп при арилировании фенолов и енолов реагентами пятивалентного висмута». Тетраэдр . 42 (12): 3111–3122. дои : 10.1016/S0040-4020(01)87378-6 .
- ^ Бартон, Дерек HR; Фине, Жан-Пьер; Хамси, Джамал (январь 1987 г.). «Соли меди катализ N -фенилирования аминов трехвалентными висмуторганическими соединениями». Буквы тетраэдра . 28 (8): 887–890. дои : 10.1016/S0040-4039(01)81015-7 .
- ^ Бартон, Дерек HR; Озбалик, Нубар; Рамеш, Маниан (январь 1988 г.). «Химия реагентов органовисмута: соединение лигандов части XIII, индуцированное Pd (0)». Тетраэдр . 44 (18): 5661–5668. дои : 10.1016/S0040-4020(01)81427-7 .
- ^ Ганьон, Александр; Дюплесси, Мартин; Альсабе, Памела; Барабе, Фрэнсис (1 мая 2008 г.). «Катализируемая палладием реакция перекрестного сочетания трициклопропилвисмута с арилгалогенидами и трифлатами». Журнал органической химии . 73 (9): 3604–3607. дои : 10.1021/jo702377h . ПМИД 18363369 .
- ^ украшения, Арно; Зеппельт, Конрад (май 1989 г.). «Структуры соединений пентаарилвисмута». Химические отчеты . 122 (5): 803–808. дои : 10.1002/cber.19891220502 .
- ^ Jump up to: а б с Патай, Саул , изд. (1994). Химия органических соединений мышьяка, сурьмы и висмута . Химия функциональных групп. Чичестер, Великобритания: Wiley. дои : 10.1002/0470023473 . ISBN 047193044X .
- ^ Бартон, Дерек HR; Шарпио, Бриджит; Дау, Элиза Чан Хуу; Мазервелл, Уильям Б.; Паскар, Клодин; Пишон, Клотильда (14 марта 1984 г.). «Структурные исследования кристаллических пятикалентных висмуторганических соединений». Helvetica Chimica Acta . 67 (2): 586–599. дои : 10.1002/hlca.19840670227 .
- ^ Валленхауэр, Стефан; Леопольд, Дитер; Зеппельт, Конрад (сентябрь 1993 г.). «Шестикоординационные висмуторганические соединения». Неорганическая химия . 32 (18): 3948–3951. дои : 10.1021/ic00070a029 .
- ^ Химия висмута Хитоми Судзуки, Ёсихиро Матано Эльзевир, 2001
- ^ Jump up to: а б Эллиотт, Грегори И.; Конопельски, Джозеф П. (июль 2001 г.). «Арилирование свинцовоорганическими и висмуторганическими реагентами». Тетраэдр . 57 (27): 5683–5705. дои : 10.1016/S0040-4020(01)00385-4 .
- ^ Jump up to: а б Бартон, Дерек HR; Бхатнагар, Нирджа Ядав; Фине, Жан-Пьер; Мазервелл, Уильям Б. (январь 1986 г.). «Пятивалентные висмуторганические реагенты. Часть VI. Сравнительная миграционная способность арильных групп при арилировании фенолов и енолов реагентами пятивалентного висмута». Тетраэдр . 42 (12): 3111–3122. дои : 10.1016/S0040-4020(01)87378-6 .
- ^ Бартон, DHR; Фине, Ж.-П. (1 января 1987 г.). «Реактивы висмута(V) в органическом синтезе» . Чистая и прикладная химия . 59 (8): 937–946. дои : 10.1351/pac198759080937 . S2CID 96332137 .
