Дикарбонил
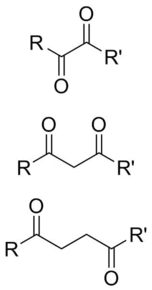
В органической химии дикарбонил содержащая - это молекула, два карбонила ( C = O ) группы . Хотя этот термин может относиться к любому органическому соединению , содержащему две карбонильные группы, он используется более конкретно для описания молекул, в которых оба карбонилы находятся в близко достаточно 1,4-дикарбонилс. Их свойства часто отличаются от свойств монокарбонилов, и поэтому они обычно считаются собственными функциональными группами. Эти соединения могут иметь симметричные или несимметричные заместители на каждом карбониле, а также могут быть функционально симметричными (диалдегиды , ди кетоны , ди -эфиры и т. Д. ) Или несимметричным (кето-эфиры, кето-акиды и т. Д. ).
1,2-дикарбонилс
[ редактировать ]1,2-диалдегид
[ редактировать ]Единственный 1,2-диалдегид- глиоксаль , (Чо) 2 . Как и многие алкилдиалдегиды, глиоксал встречается почти исключительно как его гидрат и его олигомеры. Эти производные часто ведут себя эквивалентно для альдегидов , поскольку гидратация обратима. Глисаль легко конденсируется аминами . С помощью таких реакций это является предшественником многих гетероциклов , например, имидазолов .

1,2-дикетоны
[ редактировать ]Основным дикетоном является диацетил , также известный как 2,3-бутандионе, CH 3 C (O) C (O) CH 3 . 1,2-дикетоны часто генерируются путем окисления (дегидрирования) диолов : [ 1 ]
2,3-бутандионе, 2,3-пентанедионе и 2,3-гексанедиона встречаются в небольших количествах в различных продуктах. Они используются в качестве ароматических компонентов в беспроводных напитках и в выпечке. [ 1 ] Бензил , (PHCO) 2 , является соответствующим производным дифенила.
Отличительной особенностью 1,2-дикета является длинная CC Bond, связывающая карбонильные группы. Это расстояние связи составляет около 1,54 Å по сравнению с 1,45 Å для соответствующей связи в 1,3-бутадиене . Эффект объясняется отталкиванием между частичными положительными зарядами атомов карбонильного углерода. [ 2 ]
1,2-дикетоны конденсируются со многими бифункциональными нуклеофилами, такими как мочевина и Thiurea, чтобы дать гетероциклы. Конденсация ароматическими аминами дает дикетимин ( (Rc = nar) 2 ).
В случаях 1,2-циклогександионе и 1,2-циклопентатанедиона enol . составляет примерно 1-3 ккал/моль стабильнее, чем форма дикето [ 3 ]
ортоцинон , C 4 H 4 (CO) 2 , является родителем большой семьи 1,2-дикетонов.
1,2-кетоальдегиды
[ редактировать ]
Хорошо известным соединением этого класса является метилглаксаль , CH 3 C (O) CHO , также известный как пиральдегид. Эти соединения также известны как 2-оксоальдегиды [ 4 ] или α-кетоальдегиды.
1,2-дискеры и диасиды
[ редактировать ]Оксальновая кислота и ее сложные эфиры определяют это семейство соединений. Диацид производится в промышленности путем окисления отходов сахара. Это происходит естественным образом (как конъюгатное основание), особенно у членов вида растений оксалис . Конденсация диеров с диаминами дает циклические диамиды.
α-кето- и формалкарбоновые кислоты
[ редактировать ]
α-кето-акислой и -естер хорошо известны. Пировиновая кислота ( CH 3 C (O) CO 2 H ) является родительским α-кетоцидом. Его сопряженное основание, пируват ( CH 3 C (O) CO - 2 ), является компонентом цикла лимонной кислоты и продуктом метаболизма глюкозы ( гликолиз ). Соответствующим альдегид-кислотой является глиоксаловая кислота ( HC (O) CO 2 H ).
1,3-дикарбонилс
[ редактировать ]1,3-диалдегиды
[ редактировать ]Родитель 1,3-диалдегид это малонологичный - Ch 2 (CHO) 2 ), β-дикарбонил. Как и большинство диальдегидов, он редко встречается как таковой. Вместо этого он обрабатывается почти исключительно как его гидрат, метилацетал и их олигомеры. Эти производные часто ведут себя как родитель. Многие 2-ободощенные производные известны. Они часто получают алкилирование энолята малонологичного радгида .
1,3-дикетоны
[ редактировать ]1,3-дикетоны также называют β-дикетонами. Важным членом является ацетилацетон , CH 3 C (O) CH 2 C (O) CH 3 . Dimedone -циклический 1,3-дикетон. 1,3-индионион является циклическим 1,3-дикетоном, слитым с бензольным кольцом. Ацетилацетон готовится промышленно путем термической перестройки изопропенилацетата. [ 1 ] Другим циклическим 1,3-дикетоном является 2,2,4,4-тетраметилциклобутандионе , который является предшественником полезного диола .
1,3-дикетоны часто тавтомеризуются к enol и кетолу. Они обычно существуют преимущественно в форме enol [ Цитация необходима ] Полем Процент ENOL в ацетилацетоне , трифторуацетилацетоне и гексафторуацетилацетоне составляет 85, 97 и 100%соответственно (аккуратный, 33 ° C). [ 5 ] Циклические 1,3-дикетоны, такие как 1,3-циклогексанедион и димедон , аналогично существуют в форме enol.
Как и другие дикетоны, 1,3-дикетоны являются универсальными предшественниками гетероциклов. Конъюгатное основание, полученное из 1,3-кетонов, может служить лигандом S, образуя металлические координационные комплексы ацетилацетоната . В Demayo реакция 1,3-дикетоны реагируют с алкенами в фотохимической перициклической реакции с образованием (замещенным) 1,5-дикетонами.
Классически 1,3-дикетоны готовятся конденсацией кетона с эфиром.
1,3-дискеры и диасиды
[ редактировать ]Малоновая кислота и ее сложные эфиры являются родителями этого класса дикарбонилов. Также распространены 2-размененные производные с формулой RCH (CO 2 R) 2 , который возникает при C-алкилировании конъюгатного основания (enalt) После (co 2 r) 2 .
β-кето-энд
[ редактировать ]β-кето-пирожки легко возникают путем конденсации пары сложных эфиров. Хорошо известным примером является этилацетоацетат (хотя он подготовлен с помощью этанолиза кетена ).
1,4-дикарбонилс
[ редактировать ]1,4-диалдегиды
[ редактировать ]Сукциналдегид (Ch 2 CHO) 2 -самый простой и родительский 1,4-диалдегид. Ароматическим производным является фталальдегид .
1,4-дикетоны
[ редактировать ]
Дикетоны с двумя метиленовыми группами, разделяющими карбонильные группы, также называемые γ-дикетонами, как правило, сосуществуют со своими Enol таутомерами . Выдающимся членом является ацетонилцетон . 1,4-дикетоны являются полезными предшественниками гетероциклов через синтез Paal-Knorr , который дает пирролы :
Эта реакционная способность является основой нейротоксичности γ -дикетонов. [ 6 ] 1,4-дикетоны также являются предшественниками фуранов и тиофенов . Конденсация 1,4-дикетонов (и связанных с ними субстратов) с гидразинами дают дигидропиридазины, которые могут быть преобразованы в пиридазины .
Para -quinone , C 4 H 4 (Co) 2 , является родителем большой семьи 1,4 -дикетонов.
1,4-дискеры и диасиды
[ редактировать ]Сукциновая кислота и ее сложные эфиры являются родителями этого семейства 1,4-дикарбонилов. Сукциновая кислота заметна в качестве компонента в цикле лимонной кислоты . Он образует ангидрид циклического кислоты, ярко -ангидрид . Ненасыщенные члены включают малеиновые и фумариновые кислоты и их сложные эфиры.
1,5-дикарбонилс
[ редактировать ]1,5-диалдегиды
[ редактировать ]Глутаральдегид (Ch 2 ) 3 (CHO) 2 -самый простой и родительский 1,5-диалдегид. Он легко увлажняет. Ароматический аналог - изофталальдегид . [ 7 ]
1,5-дикетоны
[ редактировать ]Эти дикетоны имеют три метиленовые группы, разделяющие карбонильные группы.
1,5-дискеры и диасиды
[ редактировать ]Глютариновая кислота (CH 2 ) 3 (CO 2 H) 2 -родительский 1,5-диацид.
Гидратация и циклизация
[ редактировать ]
Маленькие альдегиды имеют тенденцию к гидрате. Гидратация распространена для диальдегидов. Глисаль образует серию циклических гидратов. Сукциналдегид гидраты с готовностью дают 2,5-дигидрокситетрагидрофуран. Ароматический фталальдегид также образуется гидратированным.

Аналогичные равновесия гидратации и циклизации применяются к малеискому диальдегиду, [ 8 ] [ 9 ] глутаральдегид и адипальдегид .
Безопасность
[ редактировать ]Ряд дикарбонильных соединений является биологически активным. Известно, что диацетил вызывает облитерации бронхиолита заболевания легких у тех, кто подвергался ему воздействия в профессиональных условиях. [ 10 ] Диалдегиды, например, глутаральдегид и малональдегид, являются фиксаторами или стерилизаторами.
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный в резкий Зигель; Манфред Эгрсорфер (2007). "Кононы" Энциклопедия Вейнхайм: Wiley-VCH п. 16. doi 10.1002/14356007.a15_077: ISBN 978-3527306732 .
- ^ Эрикс, К.; Хейден, ТД; Ян, С. Хси; Чан, IY (1983). «Кристаллическая и молекулярная структура биацетил (2,3 -бутандионе), (H 3 CCO) 2 , при -12 и -100 ° C». J. Am. Химический Соц 105 (12): 3940–3942. doi : 10.1021/ja00350a032 .
- ^ Яна, Калянашис; Ganguly, Bishwajit (2018). «Исследование DFT для изучения важности размера кольца и влияния растворителей на процесс тавтомеризации кето-эзола α- и β-циклодионов» . ACS Omega . 3 (7): 8429–8439. doi : 10.1021/acsomega.8b01008 . PMC 6644555 . PMID 31458971 .
- ^ "Chebi: 27659 - 2 -Oxo Aldehyde" . Химические сущности, представляющие биологический интерес (Chebi).
- ^ Джейн Л. Бердетт; Макс Т. Роджерс (1964). «Кето-энол таутомеризм в β-дикарбонилах, изученных с помощью ядерной магнитно-резонансной спектроскопии. I. Протонные химические сдвиги и равновесные константы чистых соединений». J. Am. Химический Соц 86 : 2105–2109. doi : 10.1021/ja01065a003 .
- ^ Стивен Р. Клаф; Лейна Малхолланд (2005), «Гексан», Энциклопедия токсикологии , вып. 2 (2 -е изд.), Elsevier, стр. 522–525
- ^ Акерман, Дж. Х; Суррей, АР (1967). «Изофталальдегид». Органические синтезы . 47 : 76. doi : 10.15227/orgsyn.047.0076 .
- ^ Харди, ПМ; Николс, AC; Rydon, HN (1972). «Гидратация и полимеризация сукцинальногодегида, глутаральдегида и адипальдегида». Журнал химического общества, Perkin Transactions 2 (15): 2270. DOI : 10.1039/p29720002270 .
- ^ DM Burness (1960). «2,5-дигидро-2,5-диметоксифуран». Органические синтезы . 40 : 29. doi : 10.15227/orgsyn.040.0029 .
- ^ Крейс, Кэтлин (август 2017 г.). «Признание профессиональных эффектов диацетила: чему мы можем извлечь из этой истории?» Полем Токсикология . 388 : 48–54. doi : 10.1016/j.tox.2016.06.009 . PMC 5323392 . PMID 27326900 .



