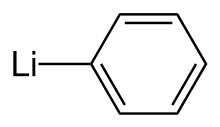
Фениллитий
| |

| |
| Имена | |
|---|---|
| Систематическое название ИЮПАК
Фениллитий [ 2 ] | |
| Другие имена
Литиобензол [ 1 ]
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Сокращения | ЛиФ,ФЛи |
| 506502 | |
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.008.838 |
| Номер ЕС |
|
| 2849 | |
| МеШ | фениллитий |
ПабХим CID
|
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| ЛиК 66Ч 5 | |
| Молярная масса | 84.045 g mol −1 |
| Появление | Бесцветные кристаллы |
| Плотность | 828 мг см −3 |
| Точка кипения | От 140 до 143 ° C (от 284 до 289 ° F; от 413 до 416 К) |
| Реагирует | |
| Термохимия | |
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
48,3-52,5 кДж раз −1 |
| Опасности | |
| СГС Маркировка : | |
  
| |
| Опасность | |
| Х226 , Х250 , Х261 , Х302 , Х312 , Х314 , Х332 | |
| P210 , P222 , P231+P232 , P233 , P240 , P241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P280 , P301+P312 , P301+P330+P331 , P302+P334 , P302+P352 , P303+ P361+P353 P304 , +P312 , P304+P340 , P305+P351+P338 , P310 , P312 , P321 , P322 , P330 , P363 , П370+П378 , П402+П404 , П403+П235 , П405 , П422 , П501 | |
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов |
| Родственные соединения | |
Родственные соединения
|
фенилмедь , фенилнатрий , фенилкобальт |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Фениллитий представляет собой металлоорганическое вещество с брутто-формулой C 6 H 5 Li. Чаще всего он используется в качестве металлирующего агента в органическом синтезе и заменителя реактивов Гриньяра для введения фенильных групп в органическом синтезе. [ 3 ] Кристаллический фениллитий бесцветен; однако растворы фениллития имеют различные оттенки коричневого или красного цвета в зависимости от используемого растворителя и примесей, присутствующих в растворенном веществе. [ 4 ]
Подготовка
[ редактировать ]Фениллитий впервые был получен реакцией металлического лития с дифенилртутью : [ 5 ]
- (C 6 Η 5 ) 2 Ηg + 2Li → 2C 6 Η 5 Li + Ηg
Реакция фенилгалогенида с металлическим литием дает фениллитий:
- X-Ph + 2Li → Ph-Li + LiX
Фениллитий также можно синтезировать с помощью реакции обмена металл-галоген:
- н-BuLi + X-Ph → n-BuX + Ph-Li
Преобладающим методом получения фениллития сегодня являются два последних синтеза.
Реакции
[ редактировать ]Основное использование PhLi заключается в облегчении образования углерод-углеродных связей в результате реакций нуклеофильного присоединения и замещения:
- PhLi + R 2 C=O → PhR 2 COLi
2-Фенилпиридин получают реакцией фениллития с пиридином, процесс, который влечет за собой путь присоединения-отщепления: [ 6 ]
- C 6 H 5 Li + C 5 H 5 N → C 6 H 5 -C 5 H 4 N + LiH
Структура и свойства
[ редактировать ]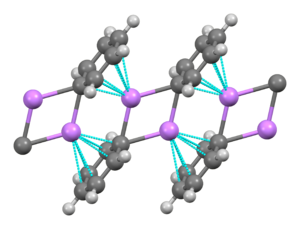
Фениллитий — литийорганическое соединение, образующее моноклинные кристаллы. Твердый фениллитий можно описать как состоящий из димерных субъединиц Li 2 Ph 2 . Атомы Li и атомы углерода ипсо фенильных колец образуют плоское четырехчленное кольцо. Плоскости фенильных групп перпендикулярны плоскости этого кольца Li 2 C 2 . Между этими димерами фениллития и π-электронами фенильных групп в соседних димерах возникает дополнительная прочная межмолекулярная связь, что приводит к образованию бесконечной полимерной лестничной структуры. [ 7 ]
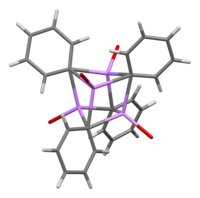
В растворе он принимает различные структуры в зависимости от органического растворителя. В тетрагидрофуране он уравновешивает состояния мономера и димера. В эфире, который обычно продается, фениллитий существует в виде тетрамера. Четыре атома Li и четыре углеродных центра ipso занимают чередующиеся вершины искаженного куба. Фенильные группы находятся на гранях тетраэдра и связываются с тремя ближайшими атомами Li.
Длины связей C–Li составляют в среднем 2,33 Å. Молекула эфира связывается с каждым из центров Li через свой атом кислорода. В присутствии LiBr, побочного продукта прямой реакции лития с фенилгалогенидом, комплекс [(PhLi•Et 2 O) 4 ] вместо этого превращается в [(PhLi•Et 2 O) 3 ·LiBr]. Атом Li в LiBr занимает одну из литиевых позиций в кластере кубанового типа , а атом Br находится в соседней углеродной позиции. [ 8 ]
Ссылки
[ редактировать ]- ^ Обычно используется для описания замещенных производных. См., например, Кацутоши Кобаяши; Соичи Сато; Хорн, Эрнст; Наомичи Фурукава (1998), «Первое выделение и характеристика катионных солей сульфения, стабилизированных координацией двух атомов азота», Tetrahedron Letters , 39 : 17, стр. 2593-2596. ISSN 0040-4039. ДОИ 10.1016/S0040-4039(98)00277-9 .
- ^ «фениллитий (CHEBI:51470)» . Химические соединения биологического интереса (ХЭБИ) . Кембридж, Великобритания: Европейский институт биоинформатики. 22 января 2009 г. Основной . Проверено 1 июня 2013 г.
- ^ Вительманн, У.; Бауэр, Р.Дж. «Литий и литиевые соединения» . Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a15_393 . ISBN 978-3527306732 .
- ^ Гилман, Х.; Зелльнер, Э.А.; Селби, WM (1932). «Усовершенствованная методика получения литийорганических соединений». Журнал Американского химического общества . 54 (5): 1957–1962. дои : 10.1021/ja01344a033 .
- ^ Грин, ДП; Зуев, Д. (2008). «Фениллитий» . Энциклопедия реагентов для органического синтеза . Уайли и сыновья. дои : 10.1002/047084289X.rp076.pub2 . ISBN 978-0471936237 .
- ^ Эванс, JCW; Аллен, CFH «Органический синтез 2-фенилпиридина» (1938), том. 18, с. 70 дои : 10.15227/orgsyn.018.0070
- ^ Диннебье, RE; Беренс, У.; Ольбрих, Ф. (1998). «Фениллитий без основания Льюиса: определение структуры твердого тела методом синхротронной порошковой дифракции». Журнал Американского химического общества . 120 (7): 1430–1433. дои : 10.1021/ja972816e .
- ^ Хоуп, Х.; Власть, ПП (1983). «Выделение и кристаллическая структура безгалогенидных и богатых галогенидами комплексов эфирата фениллития [(PhLi•Et 2 O) 4 ] и [(PhLi•Et 2 O) 3 ·LiBr]». Журнал Американского химического общества . 105 (16): 5320–5324. дои : 10.1021/ja00354a022 .