Мезитилен
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 1,3,5-Триметилбензол [1] | |||
| Другие имена Мезитилен [1] сим -триметилбензол | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.003.278 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
| Число | 2325 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 9 Ч 12 | |||
| Молярная масса | 120.19 g/mol | ||
| Появление | Бесцветная жидкость [2] | ||
| Запах | Необычный, ароматный [2] | ||
| Плотность | 0,8637 г/см 3 при 20 °С | ||
| Температура плавления | -44,8 ° C (-48,6 ° F; 228,3 К) | ||
| Точка кипения | 164,7 ° С (328,5 ° F; 437,8 К) | ||
| 0,002% (20°С) [2] | |||
| Давление пара | 2 мм рт.ст. (20°С) [2] | ||
| -92.32·10 −6 см 3 /моль | |||
| Структура | |||
| 0,047 Д [3] | |||
| Опасности | |||
| точка возгорания | 50 °С; 122 °Ф; 323 К [2] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
МЕХ (Допускается) | никто [2] | ||
РЕЛ (рекомендуется) | СВВ 25 частей на миллион (125 мг/м 3 ) [2] | ||
IDLH (Непосредственная опасность) | без даты [2] | ||
| Паспорт безопасности (SDS) | [1] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Мезитилен или 1,3,5-триметилбензол — производное бензола с тремя метильными заместителями, расположенными симметрично вокруг кольца. Два других изомерных триметилбензола — это 1,2,4-триметилбензол (псевдокумол) и 1,2,3-триметилбензол (гемимеллит). Все три соединения имеют формулу C 6 H 3 (CH 3 ) 3 , которую обычно называют C 6 H 3 Me 3 . Мезитилен — бесцветная жидкость со сладким ароматным запахом. Это компонент каменноугольной смолы , которая является ее традиционным источником. Это предшественник различных чистых химикатов . Мезитильная H группа (Mes) представляет собой заместитель формулы C 6 и 2 Me 3 встречается в различных других соединениях. [4]
Подготовка
[ редактировать ]Мезитилен получают трансалкилированием ксилола кислотном на твердом катализаторе : [4]
- 2 С 6 Н 4 (СН 3 ) 2 ⇌ С 6 Н 3 (СН 3 ) 3 + С 6 Н 5 СН 3
- C 6 H 4 (CH 3 ) 2 + CH 3 OH → C 6 H 3 (CH 3 ) 3 + H 2 O
Хотя это и непрактично, его можно получить тримеризацией пропина , что также требует кислотного катализатора , и дает смесь 1,3,5- и 1,2,4-триметилбензолов.
Тримеризация ацетона является посредством альдольной конденсации , которая катализируется и дегидратируется , серной кислотой еще одним методом синтеза мезитилена. [5]
Реакции
[ редактировать ]Окисление мезитилена азотной кислотой дает тримезиновую кислоту C 6 H 3 (COOH) 3 . При использовании диоксида марганца , более мягкого окислителя 3,5-диметилбензальдегид . , образуется Мезитилен окисляется трифторперуксусной кислотой с образованием мезитола (2,4,6-триметилфенола). [6] Бромирование происходит легко с образованием мезитилбромида : [7]
- (CH 3 ) 3 C 6 H 3 + Br 2 → (CH 3 ) 3 C 6 H 2 Br + HBr
Мезитилен является лигандом в металлоорганической химии , одним из примеров является молибденорганический комплекс [( η 6 -C 6 H 3 Me 3 )Mo(CO) 3 ] [8] который можно получить из гексакарбонила молибдена .
Приложения
[ редактировать ]Мезитилен в основном используется в качестве предшественника 2,4,6-триметиланилина , предшественника красителей. Это производное получают путем селективного мононитрования мезитилена, избегая окисления метильных групп. [9]
Нишевое использование
[ редактировать ]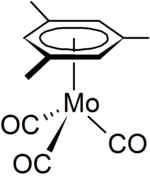
Мезитилен используется в лаборатории как специальный растворитель. В электронной промышленности мезитилен использовался в качестве проявителя для силиконов с фоторисунком из -за его свойств растворителя.
Три ароматических атома водорода мезитилена находятся в одинаковых условиях химического сдвига. Поэтому они дают только один пик около 6,8 ppm в 1 Спектр ЯМР 1Н ; то же самое верно и для девяти метильных протонов, которые дают синглет около 2,3 м.д. По этой причине мезитилен иногда используется в качестве внутреннего стандарта в образцах ЯМР, содержащих ароматические протоны. [10]
Увитовую кислоту получают окислением мезитилена или конденсацией пировиноградной кислоты с баритовой водой . [11]
Реакцию Гаттермана можно упростить, заменив HCN/AlCl 3 комбинацию цианидом цинка (Zn(CN) 2 ). [12] Несмотря на высокую токсичность, Zn(CN) 2 представляет собой твердое вещество, поэтому работать с ним безопаснее, чем с газообразным цианистым водородом (HCN). [13] Zn(CN) 2 реагирует с HCl с образованием ключевого реагента HCN и ZnCl 2 , который служит катализатором кислоты Льюиса in-situ . Примером метода Zn(CN) 2 является синтез мезитальдегида из мезитилена. [14]
История
[ редактировать ]Мезитилен был впервые получен в 1837 году ирландским химиком Робертом Кейном путем нагревания ацетона с концентрированной серной кислотой. [15] Он назвал свое новое вещество «мезитилен», потому что немецкий химик Карл Райхенбах назвал ацетон «месит» (от греческого μεσίτης, посредник). [16] и Кейн полагал, что его реакция привела к обезвоживанию мезита, превратив его в алкен , «мезитилен». [17] Однако определение Кейном химического состава («эмпирической формулы») мезитилена было неверным. Правильную эмпирическую формулу дал Август В. фон Гофман в 1849 году. [18] В 1866 году Адольф фон Байер дал правильную эмпирическую формулу мезитилена; однако с неправильной структурой тетрацикло[3.1.1.1 1, 3.1 3,5 ]нонан. [19] Убедительное доказательство того, что мезитилен представляет собой триметилбензол, было предоставлено Альбертом Ладенбургом в 1874 году; однако, если предположить неправильную бензольную структуру призмана . [20]
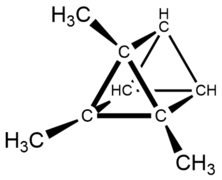
- Исторические мезитиленовые структуры
- Мезитилен Адольфа фон Байера (тетрацикло [3.1.1.1 1, 3.1 3,5 ]нонан)
- Мезитилен Альберта Ладенбурга (1,2,6-триметилпризман)
Мезитильная группа
[ редактировать ]Группа (CH 3 ) 3 C 6 H 2 – называется мезитилом (обозначение органической группы: Mes). Производные мезитила, например тетрамезитилди железа , обычно получают из реактива Гриньяра (CH 3 ) 3 C 6 H 2 MgBr. [21] Из-за своей большой стерической потребности мезитильная группа используется в качестве большой блокирующей группы в асимметричном катализе (для повышения диастерео- или энантиоселективности) и металлоорганической химии (для стабилизации металлоцентров с низкой степенью окисления или низким координационным числом). Более крупные аналоги с еще большей стерической потребностью, например 2,6-диизопропилфенил (Дипп) и аналогичный Трипп (( я Pr) 3 C 6 H 2 , Is) и супермезитил (( т Группы Bu) 3 C 6 H 2 , Mes*) могут оказаться еще более эффективными для достижения этих целей.
Безопасность и окружающая среда
[ редактировать ]Мезитилен также является основным городским летучим органическим соединением (ЛОС), образующимся в результате сгорания . Он играет значительную роль в образовании аэрозольного и тропосферного озона , а также в других реакциях химии атмосферы . [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 139. дои : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Перейти обратно: а б с д и ж г час Карманный справочник NIOSH по химическим опасностям. «#0639» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Чжао, Цзюнь; Чжан, Реньи (2004). «Константы скорости реакции переноса протона между ионами гидроксония (H 3 O + ) и летучих органических соединений». Атмосферная среда . 38 (14): 2177–2185. Bibcode : 2004AtmEn..38.2177Z . doi : 10.1016/j.atmosenv.2004.01.019 .
- ^ Перейти обратно: а б Карл Грисбаум, Арно Бер, Дитер Биденкапп, Хайнц-Вернер Фогес, Доротея Гарбе, Кристиан Паец, Герд Коллин, Дитер Майер, Хартмут Хёке «Углеводороды» в Энциклопедии промышленной химии Ульмана, 2002 Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a13_227 .
- ^ Камминг, WM (1937). Систематическая органическая химия (3Е) . Нью-Йорк, США: Компания Д. Ван Ностранда. п. 57.
- ^ Чемберс, Ричард Д. (2004). «Функциональные соединения, содержащие кислород, серу или азот и их производные» . Фтор в органической химии . ЦРК Пресс . стр. 242–243. ISBN 9780849317903 .
- ^ Ли Ирвин Смит (1931). «Бромомезитилен». Орг. Синтез . 11:24 . дои : 10.15227/orgsyn.011.0024 .
- ^ Джиролами, Г.С .; Раухфусс, Т.Б. и Анжеличи, Р.Дж. , Синтез и техника в неорганической химии, Университетские научные книги: Милл-Вэлли, Калифорния, 1999. ISBN 0-93570248-2 .
- ^ Джеральд Бут (2007). «Нитросоединения ароматические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a17_411 . ISBN 978-3527306732 .
- ^ «Мезитилен (1,3,5-триметилбензол)» .
- ^ «Определение увитовой кислоты» . merriam-webster.com . Проверено 31 октября 2016 г.
- ^ Адамс Р .; Левин, И. (1923). «Упрощение синтеза гидроксиальдегидов по методу Гаттермана». Дж. Ам. хим. Соц. 45 (10): 2373–77. дои : 10.1021/ja01663a020 .
- ^ Адамс, Роджер (1957). Органические реакции, Том 9 . Нью-Йорк: John Wiley & Sons, Inc., стр. 38 и 53–54. дои : 10.1002/0471264180.или009.02 . ISBN 9780471007265 .
- ^ Фьюсон, Колорадо; Хорнинг, ЕС; Роуленд, СП; Уорд, ML (1955). «Мезитальдегид». Органические синтезы . дои : 10.15227/orgsyn.023.0057 ; Сборник томов , т. 3, с. 549 .
- ^ Роберт Кейн (1839) «О серии комбинаций, полученных из пироуксусного спирта [ацетона]» Труды Королевской ирландской академии , том. 18, страницы 99–125.
- ^ Отрывок из исследования Райхенбаха приведен в: К. Райхенбах (1834) «Ueber Mesit ( Essiggeist) und Holzgeist» (О mesit (уксусном спирте) и древесных спиртах), Annalen der Pharmacie , vol. 10, № 3, стр. 298–314.
- ^ Объяснение оригинала названия «мезитилен» см. Также: Генри Э. Роско, Трактат по химии (Нью-Йорк, Нью-Йорк: Д. Эпплтон и Ко, 1889), том. III, стр. 102 , сноска 2.
- ^ AW Hofmann (1849) «О составе мезитилола [мезитилена] и некоторых его производных», Ежеквартальный журнал Лондонского химического общества , том. 2, страницы 104–115 . (Примечание: эмпирическая формула мезитилена, указанная в статье Хофмана (C 18 H 12 ), неверна; однако это произошло потому, что Хофманн использовал 6 в качестве атомного веса углерода вместо правильного атомного веса 12. Как только правильный атомный вес вес используется в расчетах Гофмана, его результаты дают правильную эмпирическую формулу C 9 H 12 .)
- ^ Адольф фон Байер (1866) «Ueber die Condensationsprodukte des Acetones» (О продуктах конденсации ацетона), Annals of Chemistry and Pharmacie , vol. 140, страницы 297–306.
- ^ Альберт Ладенбург (1874) «Ueber das Mesitylene» (О мезитилене), Отчеты Немецкого химического общества , том. 7, страницы 1133–1137. два : 10.1002/cber.18740070261
- ^ Ли Ирвин Смит (1931). «Изодурен». Орг. Синтез . 11:66 . дои : 10.15227/orgsyn.011.0066 .


![Мезитилен Адольфа фон Байера (тетрацикло[3.1.1.11,3.13,5]нонан)](http://upload.wikimedia.org/wikipedia/commons/thumb/0/0e/Mesitylen_by_Adolf_von_Baeyer.png/260px-Mesitylen_by_Adolf_von_Baeyer.png)