Цианид цинка
 | |
| Имена | |
|---|---|
| Другие имена Нейтральный цианид цинка (1:2) | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.008.331 |
| Номер ЕС |
|
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1713 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Zn(CN) 2 | |
| Молярная масса | 117.444 g/mol |
| Появление | белое твердое вещество |
| Плотность | 1,852 г/см 3 , твердый |
| Температура плавления | 800 ° C (1470 ° F, 1070 К) (разлагается) |
| 0,0005 г/100 мл (20 °С) | |
| Растворимость | подвергается воздействию щелочей , KCN , аммиака |
| −46.0·10 −6 см 3 /моль | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Токсично, выделяет цианид-ион в организме. [1] |
| СГС Маркировка : [2] | |
  | |
| Опасность | |
| Х300 , Х301 , Х310 , Х330 , Х410 | |
| P260 , P262 , P264 , P270 , P271 , P273 , P280 , P284 , P301+P310 , P302+P350 , P304+P340 , P310 , P320 , P322 , P330 , P361 , P363 , P391 , П403+П233 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) | 100 мг/кг, крыса (внутрибрюшинно) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Цианид цинка – неорганическое соединение формулы Zn ( CN ) 2 . Это белое твердое вещество, которое используется главным образом для гальваники цинка, но также имеет более специализированное применение для синтеза органических соединений .
Структура
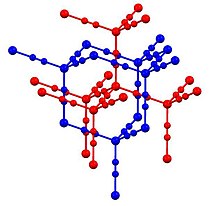
[ редактировать ]В Zn(CN) 2 цинк принимает тетраэдрическую координационную среду, все связанные мостиковыми цианидными лигандами . Структура состоит из двух «взаимопроникающих» структур (синяя и красная на картинке выше). Такие мотивы иногда называют «расширенными алмазоидными » структурами. Некоторые формы SiO 2 имеют аналогичную структуру, в которой тетраэдрические центры Si связаны оксидами. Цианидная группа демонстрирует беспорядок «голова к хвосту», при этом любой атом цинка имеет от одного до четырех соседей углерода, а остальные являются атомами азота. [4] Он показывает один из самых больших отрицательных коэффициентов теплового расширения (превышает предыдущего рекордсмена — вольфрамат циркония ).
Химические свойства
[ редактировать ]Типичный для неорганического полимера Zn(CN) 2 нерастворим в большинстве растворителей. Твердое вещество растворяется или, точнее, разлагается под действием водных растворов основных лигандов, таких как гидроксид , аммиак и дополнительный цианид, с образованием анионных комплексов.
Синтез
[ редактировать ]Zn(CN) 2 легко получить путем объединения водных растворов цианида и ионов цинка, например, посредством реакции двойного замещения между KCN и ZnSO 4 : [5]
- ZnSO 4 + 2 IZ → Zn(CN) 2 + K 2 SO 4
Для коммерческого применения предпринимаются некоторые усилия, чтобы избежать примесей галогенидов , используя ацетатные соли цинка: [5] [6]
- Zn(CH 3 COO) 2 + HCN → Zn(CN) 2 + 2 CH 3 COOH
Цианид цинка также производится как побочный продукт некоторых методов добычи золота . Процедуры выделения золота из водного цианида золота иногда требуют добавления цинка:
- 2 [Аи(CN) 2 ] − + Zn → 2 Au + Zn(CN) 2 + 2 CN −
Приложения
[ редактировать ]Гальваника
[ редактировать ]Основное применение Zn(CN) 2 – гальваническое осаждение цинка из водных растворов, содержащих дополнительный цианид. [6]
Органический синтез
[ редактировать ]Zn(CN) 2 используется для введения формильной группы в ароматические соединения в реакции Гаттермана , где он служит удобной, более безопасной и негазовой альтернативой HCN . [7] Поскольку в реакции используется HCl , Zn(CN) 2 также обеспечивает реакцию in situ с ZnCl 2 , катализатором на основе кислоты Льюиса . Примеры использования Zn(CN) 2 таким образом включают синтез 2-гидрокси-1-нафтальдегида и мезитальдегида. [8]
Zn(CN) 2 также используется в качестве катализатора цианосилилирования альдегидов и кетонов. [9]
Ссылки
[ редактировать ]- ^ Токсичность цианида цинка
- ^ «ЦИНК цианид» . pubchem.ncbi.nlm.nih.gov .
- ^ «ЦИАНИД ЦИНКА | CAMEO Chemicals | NOAA» . www.cameochemicals.noaa.gov .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Jump up to: а б Ф. Вагенкнехт; Р. Джуза (1963). «Цианид цинка». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии, 2-е изд . Том. 2. Нью-Йорк, Нью-Йорк: Академик Пресс. п. 1087.
- ^ Jump up to: а б Эрнст Гейл, Стивен Гос, Рупрехт Кульцер, Юрген Лореш, Андреас Рубо и Манфред Зауэр «Цианосоединения, неорганические» Энциклопедия промышленной химии Ульмана Wiley-VCH, Вайнхайм, 2004. два : 10.1002/14356007.a08_159.pub2
- ^ Адамс, Роджер (1957). Органические реакции, Том 9 . Нью-Йорк: John Wiley & Sons, Inc., стр. 53–54. ISBN 9780471007265 . Проверено 18 июля 2014 г.
- ^ Адамс Р. , Левин И. (1923). «Упрощение синтеза гидроксиальдегидов по методу Гаттермана». Дж. Ам. хим. Соц. 45 (10): 2373–77. дои : 10.1021/ja01663a020 . Фьюсон Р.К., Хорнинг Э.К., Роуленд С.П., Уорд М.Л. (1955). «Мезитальдегид». Органические синтезы . дои : 10.15227/orgsyn.023.0057
{{cite journal}}: CS1 maint: multiple names: authors list (link); Сборник томов , т. 3, с. 549 . - ^ Расмуссен Дж.К., Хайльманн С.М. (1990). «Цианосилилирование карбонильных соединений in situ: О-триметилсилил-4-метоксиманделонитрил». Органические синтезы . дои : 10.15227/orgsyn.062.0196 ; Сборник томов , т. 7, с. 521 .
