Цианид аммония
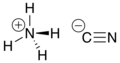 | |
 | |
| Идентификаторы | |
|---|---|
3D model ( JSmol ) | |
| ХимическийПаук | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| NH4 CN | |
| Молярная масса | 44.0559 g/mol |
| Появление | бесцветное кристаллическое твердое вещество |
| Плотность | 1,02 г/см 3 |
| Температура плавления | 36 °С (разл.) |
| очень растворим | |
| Растворимость | очень растворяется в спирте |
| Структура | |
| кубический | |
| Родственные соединения | |
Другие анионы | Гидроксид аммония Азид аммония Нитрат аммония |
Другие катионы | Цианид натрия Цианид калия |
Родственные соединения | Аммиак Цианистый водород |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Цианид аммония – нестабильное неорганическое соединение формулы NH 4 CN.
Использование
[ редактировать ]Цианид аммония обычно используется в органическом синтезе. [ нужна ссылка ] Будучи нестабильным, он не поставляется и не продается на коммерческой основе.
Подготовка
[ редактировать ]Цианид аммония получают соединением растворов цианистого водорода и аммиака : [ нужна ссылка ]
- HCN + NH 3 → NH 4 CN
Его можно получить реакцией цианида кальция и карбоната аммония : [ нужна ссылка ]
- Ca(CN) 2 + (NH 4 ) 2 CO 3 → 2 NH 4 CN + CaCO 3
В сухом состоянии цианид аммония получают путем нагревания смеси цианида калия или ферроцианида калия с хлоридом аммония и конденсации паров в кристаллы цианида аммония: [ нужна ссылка ]
- KCN + NH 4 Cl → NH 4 CN + KCl
Реакции
[ редактировать ]Цианид аммония разлагается на аммиак и цианистый водород, часто образуя черный полимер цианистого водорода: [1]
- NH 4 CN → NH 3 + HCN
В растворе с рядом солей металлов он подвергается реакции солевого обмена с образованием металлоцианидных комплексов.
Реакция с кетонами и альдегидами дает аминонитрилы , как и на первой стадии синтеза аминокислот Стрекера :
- NH 4 CN + CH 3 COCH 3 → (CH 3 ) 2 C(NH 2 )CN + H 2 O
Токсичность
[ редактировать ]Цианид аммония очень токсичен.
Примечания
[ редактировать ]- ^ Мэтьюз, Клиффорд Н. (1991). «Полимеризация цианида водорода: предпочтительный космохимический путь». Биоастрономия: поиск внеземной жизни — исследование расширяется . Конспект лекций по физике. Том. 390. стр. 85–87. дои : 10.1007/3-540-54752-5_195 . ISBN 978-3-540-54752-5 .
Ссылки
[ редактировать ]- А. Ф. Уэллс, Структурная неорганическая химия , 5-е изд., Oxford University Press, Оксфорд, Великобритания, 1984.