Мурексид
| |

| |
| Имена | |
|---|---|
| Название ИЮПАК
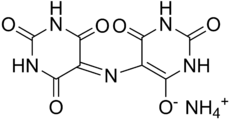
2,6-диоксо-5-[(2,4,6-триоксо-5-гексагидропиримидинилиден)амино]-3H - пиримидин-4-олат аммония
| |
| Другие имена
Аммониевая соль пурпурной кислоты
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.019.334 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 8 Ч 8 Н 6 О 6 | |
| Молярная масса | 284.188 g·mol −1 |
| Плотность | 1,72 г/см 3 (гидрат соли аммония) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Мурексид (NH 4 C 8 H 4 N 5 O 6 , или C 8 H 5 N 5 O 6 ·NH 3 ), также называемый пурпуратом аммония или MX , представляет собой аммониевую соль пурпурной кислоты . Это фиолетовое твердое вещество, растворимое в воде. Соединение когда-то использовалось в качестве индикаторного реагента . [1] Водные растворы имеют желтый цвет при низком pH , красновато-фиолетовый цвет в слабокислых растворах и сине-фиолетовый цвет в щелочных растворах.
Подготовка
[ редактировать ]Мурексид получают обработкой аллоксантина аммиаком до 100° С или обработкой урамила (5-аминобарбитуровой кислоты) оксидом ртути . [2] Его также можно получить путем расщепления аллоксана спиртовым . аммиаком
История
[ редактировать ]Юстус фон Либих и Фридрих Велер в Гиссене, Германия, исследовали фиолетовый продукт, мурексид, полученный из экскрементов змей, в 1830-х годах, но это не было распространенным сырьем, и метод использования его в качестве красителя в то время не был разработан. время. [3] В 1850-х годах французским колористам и производителям красителей, таким как Depoully в Париже, удалось получить мурексид из обильного южноамериканского гуано и нанести его на натуральные волокна. Затем он получил широкое распространение в Великобритании, Франции и Германии.
Использовать
[ редактировать ]Мурексид применяют в аналитической химии как комплексометрический индикатор для комплексометрического титрования, чаще всего ионов кальция , [4] но также для меди , никеля , кобальта , тория и редкоземельных металлов. Он действует как тридентатный лиганд. [1]
Его использование затмили кальций- селективные электроды .
Ссылки
[ редактировать ]- ^ Jump up to: а б Мартин, Раймонд Л.; Уайт, Аллан Х.; Уиллис, Энтони К. (1977). «Структурные исследования в комплексах металл-чистый. Часть 1. Кристаллические структуры тригидрата очищенного калия и моногидрата очищенного аммония (мурексида)». Дж. Хим. Soc., Далтон Транс. (14): 1336–1342. дои : 10.1039/DT9770001336 .
- ^ Некоторая информация о химике У. Н. Хартли доступна здесь. Архивировано 26 мая 2013 г. в Wayback Machine .
- ^ Питер Дж. Т. Моррис; Энтони С. Трэвис (ноябрь 1992 г.), «История международной индустрии красителей» , American Dyestuff Reporter , 81 (11), заархивировано из оригинала 11 июня 2007 г.
{{citation}}: CS1 maint: неподходящий URL ( ссылка ) - ^ Льюис, Майкл Дж. (2011). «Измерение и значение ионного кальция в молоке - обзор» . Международный журнал молочной технологии . 64 : 1–13. дои : 10.1111/j.1471-0307.2010.00639.x .
В эту статью включен текст из публикации, которая сейчас находится в свободном доступе : Чисхолм, Хью , изд. (1911). « Мюрексид ». Британская энциклопедия . Том. 19 (11-е изд.). Издательство Кембриджского университета. п. 36.