Сульфинилгалогенид

Сульфинилгалогенид имеет общую формулу r -s (o) -x, где x является галогеном. Они являются промежуточными по уровню окисления между сульфенилгалогениями , R -S -X и сульфонилгалогенками , R - SO 2 -x. Наиболее известными примерами являются сульфинилхлориды, термолабильные, чувствительные к влаге соединения, которые являются полезными промежуточными соединениями для приготовления других производных суфинила, таких как сульфинамиды, сульфинаты, сульфоксиды и тиосульфинаты. [ 1 ] В отличие от атома серы в сульфонилгалогендах и сульфенилгалогендах , атом серы в сульфинильных галогенках хиральным является [ 2 ] как показано для метанасульфинилахлорида.
Сульфинилхлориды
[ редактировать ]Хлориды сульфиновой кислоты, или сульфинилхлориды, представляют собой сульфинилгалогениды с общей формулой R - S (O) -CL. Метанасульфинилхлорид, CH 3 S (O) Cl, получают хлорированием диметил дисульфида с получением CH 3 SCL 3 , который обрабатывается уксусным ангидридом . Это соломенная жидкость. [ 3 ] Толуэенсульфинилхлорид получают путем обработки тозилата натрия тионилохлоридом : [ 4 ] Также соломенная жидкость, она кипит около 100 ° C при 0,5 мм рт. Ст.
Общий подход к образованию сульфинилхлоридов является реакцией соответствующего тиола с сульфурил -хлоридом , таким образом
2 кл
2 ; В тех случаях, когда сельфенилхлорид , RSCL, вместо этого приводит к окислению трифторпероуперационной кислоты, дает желаемый продукт, как в случае 2,2,2,2-трифтор-1,1- дифенилтананатиол : [ 5 ]
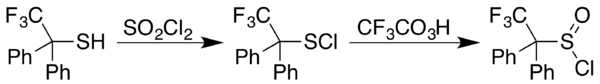
Реакция
[ редактировать ]Эти соединения легко реагируют с нуклеофилами, такими как вода, спирты, амины, тиолы и реагенты Grignard . Если нуклеофил является водой, продукт является сульфиновой кислотой , если это алкоголь, продукт является сульфиновым сложным эфиром, если это первичный или вторичный амин, продукт является сульфинамидом , если это тиол, продукт является тиосольфинатом, в то время как он является тиозольфинатом , в то время как, находясь Если это реагент Grignard, продукт является сульфоксидом . Из -за их реакционной способности и нестабильности алкансульфинилхлориды обычно используются без очистки сразу после их синтеза. Хранение не рекомендуется, поскольку давление развивается в контейнере из -за высвобождения хлорида водорода.
Обработка алкансульфинилхлоридов, имеющих α -гидрогенов с третичными основаниями амина, дает тиокарбонильные S -оксиды (сульфины) в качестве изоляционных соединений. образом, обработка N -пропанесульфинилхлорида триэтиламина дает син -пропанетиал -оксид , лахриматорный агент лука Таким . [ 6 ] Обработка метансульфинилхлорида или этана-1,2-бис-сульфинилхлорид, CLS (O) CH 2 CH 2 S (O) CL (приготовленный окислительным хлорированием 1,2-этанедитиола, HSCH 2 CH 2 SH), с Третичный амин в присутствии хиральной глюкозы вторичной алкогольной диацетон -d -глюкозы обеспечивает оптически чистые сульфинатные эфиры в процессе динамического кинетического разрешения . [ 7 ] [ 8 ] Сульфинилхлориды подвергаются реакциям Фриделя -Крафта с аренами, дающими сульфоксиды .
Сульфиниловые фториды, бромиды и йодиды
[ редактировать ]Гидролиз комнатной температуры CF 3 SF 3 дает сульфиниловый фторид CF 3 S (O) F за несколько часов в количественном выходе. Обработка CF 3 S (O) F с помощью водородного бромида при -78 ° C дает сульфиниловый бромид CF 3 S (O) BR, который нестабилен при комнатной температуре и легко непропорционально. [ 9 ] Сульфинильные йодиды, по -видимому, неизвестны.
Ссылки
[ редактировать ]- ^ Braverman, S; Cherkinsky, M.; Левингер С. (2008). «Алкансульфинилгалогениды». Наука Синтезатор 39 : 188–196. ISBN 9781588905307 .
{{cite journal}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Жиль Ханке*, Франсуаз Колоберт, Стив Ланнерс и Гай Соллади. «Недавние разработки хиральной неракемической химии сульфинил-группы при асимметричном синтезе» (PDF) . Получено 13 мая 2012 года .
{{cite web}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Дуглас, IB; Нортон, RV (1960). «Метанасульфинилхлорид». Органические синтезы . 40 : 62. doi : 10.15227/orgsyn.040.0062 .
- ^ Фредерик Курзер (1954). «Толуэенсульфинилхлорид». Орг Синтезатор 34 : 93. doi : 10.15227/orgsyn.034.0093 .
- ^ Page, PCB; Уилкс, Rd; Рейнольдс, Д. (1995). «Алкил-халькогениды: функциональные группы на основе серы» . В Лей, Стивен В. (ред.). Синтез: углерод с одним гетероатомом, прикрепленным одной связью . Комплексные трансформации органических функциональных групп. Elsevier . С. 113–276. ISBN 9780080423234 .
- ^ Блок Э., Джиллис Дж. « Химия Allium : микроволновая спектроскопическая идентификация, механизм образования, синтез и реакции ( e , z ) -пропанетиального S -оксида, лахримальный фактор лука ( allium cepa )». J. Am. Химический Соц 118 (32): 7492–7501. doi : 10.1021/ja960722j .
{{cite journal}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Fernández I., Khiar N., Llera JM, Alcudia F. (1992). «Асимметричный синтез алкан- и арансульфинатов диацетона-D-глюкозы (DAG): улучшенный и общий путь к обоим энантиомерически чистым сульфоксидам». J. Org. Химический 57 (25): 6789–6796. doi : 10.1021/jo00051a022 .
{{cite journal}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Khiar N., Araújo CS, Alcudia F., Fernández I. (2002). «Динамическая кинетическая трансформация сульфинилхлоридов: синтез энантиометрически чистых C 2 -симметричных бис -сульфоксидов». J. Org. Химический 67 (2): 345–356. doi : 10.1021/jo0159183 . PMID 11798304 .
{{cite journal}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Ratcliffe CT, Shreeve JM (1968). «Некоторые перфтоороалкилсульфинилгалогениды, r f s (o) x. Новые препараты трифторметилсульфура трифторида». J. Am. Химический Соц 90 (20): 5403–5408. doi : 10.1021/ja01022a013 .