Тиоамид

Тиоамид функциональную (реже тионамид , но также известный как тиурилены ) представляет собой группу с общей структурой Р 1 -C(=S)-NR 2 Р 3 , где Р 1 , Р 2 и Р 3 представляют собой любые группы (обычно органильные группы или водород ). Аналогично амидам , тиоамиды проявляют больший характер кратных связей вдоль связи CN, что приводит к большему вращательному барьеру. [ 1 ]
Примеры
[ редактировать ]Хорошо известным тиоамидом является тиоацетамид , который используется в качестве источника сульфид - иона и является строительным блоком в гетероциклической химии . Тиоциануровая кислота представляет собой тристиоамид.
Тиоамиды или антитиреоидные препараты также представляют собой класс препаратов , используемых для борьбы с тиреотоксикозом .
Подготовка и структура
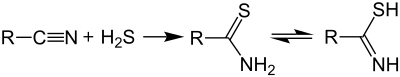
[ редактировать ]Тиоамиды обычно получают путем обработки амидов сульфидами фосфора, такими как пентасульфид фосфора , - реакция, впервые описанная в 1870-х годах. [ 2 ] [ 3 ] [ 4 ] Альтернативные пути включают использование реагента Ловессона. [ 5 ] или реакция нитрилов с сероводородом :
Реакция Виллгеродта -Киндлера также дает бензилтиоамиды. [ 6 ]
Ядро C(R)(N)(S) тиоамидов плоское. Используя тиоацетамид в качестве представителя: расстояния CS, CN и CC составляют 1,68, 1,31 и 1,50 Å соответственно. Короткие расстояния CS и CN указывают на множественное соединение. [ 7 ]
Тиоамиды в биохимии и медицине.
[ редактировать ]Тиоамиды также представляют собой класс препаратов , которые используются для борьбы с тиреотоксикозом .
Тиоамиды включаются в пептиды в качестве изостеров амидной связи. [ 8 ] Модификации пептидов являются аналогами нативного пептида, которые позволяют выявить взаимосвязь структура-активность ( SAR ). Аналоги пептидов также можно использовать в качестве препаратов с улучшенной пероральной биодоступностью . Тиоамиды ингибируют фермент тиреопероксидазу в щитовидной железе , снижая синтез трийодтиронина (Т 3 ) и тироксина (Т 4 ), тем самым блокируя поглощение йодтирозинов из коллоида . Они также блокируют высвобождение йода из периферических гормонов. Максимальный эффект наступает только через месяц, поскольку истощение гормонов вызвано снижением синтеза, а это медленный процесс.
Ссылки
[ редактировать ]- ^ Виберг, Кеннет Б.; Раблен, Пол Р. (1995). «Почему у тиоформамида больший барьер вращения, чем у формамида?». Дж. Ам. хим. Соц. 117 (8): 2201–2209. дои : 10.1021/ja00113a009 .
- ^ «Получение тиамидов» . Журнал Химического общества, Тезисы . 34 : 396. 1878. doi : 10.1039/CA8783400392 .
- ^ Гомппер, Р.; Эльзер, В. (1973). «2-Метилмеркапто- N -Метил-Δ 2 -Пирролин» . Органический синтез ; Сборник томов , т. 5, с. 780 .
- ^ Шварц, Джордж (1955). «2,4-Диметилтиазол» . Органические синтезы ; Сборник томов , т. 3, с. 332 .
- ^ Шабана, Р.; Шейби, С.; Клаузен, К.; Олесен, С.О.; Ловессон, С.-О. (1980). «Исследования фосфорорганических соединений XXXI. Синтез тиолактамов и тиоимидов». Nouveau Journal de Chimie . 1980 (4): 47.
- ^ Рольфс, Андреас; Либшер, Юрген (1998). «Морфолид 3-морфолино-2-фенилтиоакриловой кислоты и 5-(4-бромбензоил-2-(4-морфолино)-3-фенилтиофен» Органический синтез ; Сборник томов , т. 9, с. 99 .
- ^ Тревор В. Хэмбли; Дэвид Э. Хиббс; Питер Тернер; Сиан. Т. Ховард; Майкл Б. Херстхаус (2002). «Понимание связей и направленности водородных связей в тиоацетамиде на основе экспериментального распределения заряда». Дж. Хим. Soc., Перкин Транс. (2): 235–239. дои : 10.1039/B109353C .
- ^ Артис, Дин Р.; Липтон, Марк А. (1998). «Конформации тиоамидсодержащих дипептидов: вычислительное исследование». Дж. Ам. хим. Соц . 120 (47): 12200–12206. дои : 10.1021/ja982398t .