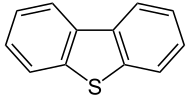
Дибензотиофен
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Дибензо[ b , d ]тиофен | |
| Другие имена Дифениленсульфид, ДБТ | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.004.613 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 12 Ч 8 С | |
| Молярная масса | 184.26 g/mol |
| Появление | Бесцветные кристаллы |
| Плотность | 1,252 г/см 3 |
| Температура плавления | От 97 до 100 ° C (от 207 до 212 ° F; от 370 до 373 К) (лит.) |
| Точка кипения | От 332 до 333 ° C (от 630 до 631 ° F; от 605 до 606 К) |
| стелька. | |
| Растворимость в других растворителях | бензол и родственные ему |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | легковоспламеняющийся, токсичный |
| СГС Маркировка : | |
   | |
| Опасность | |
| Х301 , Х302 , Х311 , Х315 , Х331 , Х332 , Х410 | |
| P261 , P264 , P270 , P271 , P273 , P280 , P301+P312 , , P302+P352 P304 P304 + +P312 , P340 , P311 , P312 , P321 , P322 , P330 , P332+P313 , 61 , П363 , П362 , П391 , П403+П233 , П405 , П501 | |
| Родственные соединения | |
Родственные соединения | Тиофен Антрацен Бензотиофен Дибензофуран |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Дибензотиофен (ДБТ, дифениленсульфид ) — сероорганическое соединение, состоящее из двух бензольных колец, конденсированных с центральным тиофеновым кольцом. Он имеет химическую формулу C 12 H 8 S. Это бесцветное твердое вещество, химически несколько похожее на антрацен . Этот трициклический гетероцикл и особенно его дизамещенное производное 4,6-диметилдибензотиофен являются проблемными примесями в нефти . [1]
Синтез и реакции
[ редактировать ]Дибензотиофен получают реакцией бифенила с дихлоридом серы в присутствии хлорида алюминия . [2]
Восстановление литием приводит к разрыву одной связи CS. С бутиллитием этот гетероцикл подвергается ступенчатому литиированию в положении 4. S-окисление пероксидами дает сульфоксид . [3]
Дибензотиофен богат электронами и естественным образом подвергается ароматическому пара -замещению в сульфид. Окисление до сульфоксида или сульфона оставляет соединение бедным электронами, и вместо этого происходит замещение в мета -положении. [4]
Ссылки
[ редактировать ]- ^ Хо, Тех К. (2004). «Глубокая HDS дизельного топлива: химия и катализ». Катализ сегодня . 98 (1–2): 3–18. дои : 10.1016/j.cattod.2004.07.048 .
- ^ Клемм, Л.Х.; Качеси, Джозеф Дж. (1978). «Введение и экструзия гетеросерных мостиков. VIII. Дибензотиофен из бифенила и его производных». Журнал гетероциклической химии . 15 (4): 561–563. дои : 10.1002/jhet.5570150407 .
- ^ Вальдекер, Бернд; Кафута, Кевин; Алькарасо, Мануэль (2019). «Получение трифлата 5-(триизопропилалкинил)дибензо[b,d]тиофения» . Органические синтезы . 96 : 258–276. дои : 10.15227/orgsyn.096.0258 . S2CID 239319277 .
- ^ Бханучандра, М.; Ёримицу Хидеки. «Дибензотиофен 5,5-диоксид». Энциклопедия реагентов для органического синтеза . дои : 10.1002/047084289X.rn02046 .