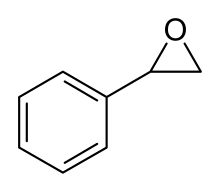
Оксид стирола
| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Фенилоксиран | |
| Другие имена
Эпоксистирол; стирилоксид; Оксид фенилэтилена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 108582 | |
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.002.252 |
| Номер ЕС |
|
| 50213 | |
| КЕГГ | |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 2810 3082 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 8 Н 8 О | |
| Молярная масса | 120.151 g·mol −1 |
| Появление | Бесцветная или светло-желтая жидкость |
| Плотность | 1,052 г/мл |
| Температура плавления | -37 ° C (-35 ° F; 236 К) |
| Точка кипения | 194 ° С (381 ° F; 467 К) |
| Опасности | |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х312 , Х319 , Х350 | |
| P201 , P202 , P264 , P280 , P281 , P302+P352 , P305+P351+P338 , P308+P313 , P312 , P322 , P337+P313 , P363 , P405 , P501 | |
| Паспорт безопасности (SDS) | Паспорт безопасности Оксфордского университета |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Оксид стирола представляет собой эпоксид, полученный из стирола . Его можно получить эпоксидированием стирола по пероксибензойной кислотой реакции Прилежаева : [ 1 ]
Оксид стирола мало растворим в воде. Следовое количество кислоты в воде вызывает гидролиз до рацемического фенилэтиленгликоля через бензильный катион. Если количества воды недостаточно, кислотно-катализируемая изомеризация фенилацетальдегида . произойдет [ 2 ]
Оксид стирола в организме метаболизируется до миндальной кислоты , фенилглиоксиловой кислоты , бензойной кислоты и гиппуровой кислоты .
Гидрирование оксида стирола дает фенэтиловый спирт . [ 3 ]
Стереоспецифические реакции
[ редактировать ]Поскольку оксид стирола имеет хиральный центр при бензильном атоме углерода, существуют ( R )-оксид стирола и ( S )-оксид стирола. Если использовать оптически чистый реагент, будет получено только одно оптически чистое соединение.
Токсикология
[ редактировать ]Оксид стирола является основным метаболитом стирола у человека или животных, образующимся в результате окисления цитохромом P450 . Считается, что он может быть канцерогенным при введении значительных количеств мышам и крысам. [ 4 ] Оксид стирола впоследствии гидролизуется vivo до стиролгликоля эпоксидгидролазой in . [ 5 ]
Оксид стирола имеет хиральный центр и, следовательно, два энантиомера . Сообщалось, что два энантиомера имели разную токсикокинетику и токсичность. [ нужна ссылка ] . Сообщалось, что ( R )-оксид стирола преимущественно образуется у мышей, особенно в легких, тогда как ( S )-оксид стирола преимущественно образуется у крыс. У людей-добровольцев кумулятивная экскреция ( S )-энантиомера стирола гликоля и миндальной кислоты была выше, чем R -формы после воздействия стирола. В микросомах печени человека окисление стирола, опосредованное цитохромом P450, показало образование большего количества энантиомера S по сравнению с R. энантиомером Также было обнаружено, что ( S )-оксид стирола гидролизуется преимущественно, чем R -энантиомер, в микросомах печени человека. Исследования на животных показали, что ( R )-энантиомер оксида стирола был более токсичным, чем ( S )-энантиомер у мышей.
Ссылки
[ редактировать ]- ^ Гарольд Хибберт и Полин Берт (1941). «Оксид стирола» . Органические синтезы ; Сборник томов , т. 1, с. 494 .
- ^ Процесс производства фенилацетальдегида, патент BASF DE3546372A1 от 2 июля 1987 г.
- ^ Фальбуш, Карл-Георг; Хаммершмидт, Франц Иосиф; Пантен, Йоханнес; Пикенхаген, Вильгельм; Шатковский, Дитмар; Бауэр, Курт; Гарбе, Доротея; Сурбург, Хорст (2003). «Вкусы и ароматы». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a11_141 . ISBN 978-3-527-30673-2 .
- ^ Оценка EPA оксида стирола
- ^ Кеннет К. Либман (1975). «Метаболизм и токсичность стирола» (PDF) . Перспективы гигиены окружающей среды . 11 : 115–119. дои : 10.2307/3428333 . JSTOR 3428333 . ПМЦ 1475194 . ПМИД 809262 . [ постоянная мертвая ссылка ]
