Диметилфенилфосфин
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Диметил(фенил)фосфан | |||
| Другие имена Диметилфенилфосфин | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.010.543 | ||
| Номер ЕС |
| ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 8 Ч 11 П | |||
| Молярная масса | 138.14 g/mol | ||
| Появление | прозрачная светлая бледно-желтая жидкость | ||
| Плотность | 0,971 г/см 3 | ||
| Температура плавления | Н/Д | ||
| Точка кипения | От 74 до 75 ° C (от 165 до 167 ° F; от 347 до 348 К) при 12 мм рт. ст. | ||
| нерастворимый | |||
| Структура | |||
| Пирамидальный | |||
| Опасности | |||
| СГС Маркировка : | |||
  | |||
| Предупреждение | |||
| Х226 , Х315 , Х319 , Х335 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P271 , P280 , P302+P352 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P312 , П332 1 , +П313 , П337+ P313 , P362 , P370+P378 , P403+P233 , P403+P235 , P405 , P501 | |||
| точка возгорания | 49 ° С (120 ° F; 322 К) | ||
| Паспорт безопасности (SDS) | [1] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
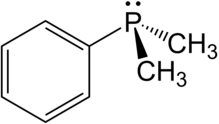
Диметилфенилфосфин представляет собой фосфорорганическое соединение формулы P(C 6 H 5 )(CH 3 ) 2 . Фосфор . связан с фенильной группой и двумя метильными группами, что делает его простейшим ароматическим алкилфосфином Это бесцветная воздухочувствительная жидкость. Это член ряда (CH 3 ) 3-n (C 6 H 5 ) 2 P, который также включает соединения n = 0 , n = 2 и n = 3 , которые часто используются в качестве лигандов в металлофосфиновых комплексах .
Подготовка
[ редактировать ]Диметилфенилфосфин получают реакцией галогенида метилмагния с дихлорфенилфосфином .
- (C 6 H 5 )Cl 2 P + 2CH 3 MgBr → (C 6 H 5 )(CH 3 ) 2 P + 2MgBrCl
Фосфин . очищают перегонкой при пониженном давлении [1] Раствор (C 6 H 5 )(CH 3 ) 2 P в CDCl 3 показывает сигналы ЯМР протонов при δ 7,0-7,5 и дублет при δ 1,2. Спектр ЯМР фосфора-31 показывает синглет при -45,9 м.д. в CDCl 3 . [2]
Структура и свойства
[ редактировать ]Диметилфенилфосфин представляет собой пирамидальную молекулу , в которой фенильная группа и две метильные группы соединены с фосфором. Длина связи и углы следующие: PC Me : 1,844, PC Ph : 1,845 Å, CC: 1,401 Å, CH Me : 1,090 Å, CH Ph : 1,067 Å, CPC: 96,9°, CPC (кольцо): 103,4°, ПКХ: 115,2°. [3]
При присоединении к хиральным металлцентрам P-метильные группы являются диастереотопными , проявляясь в виде отдельных дублетов в 1 Спектр ЯМР 1Н.
Сравнение с родственными фосфиновыми лигандами
[ редактировать ]ν CO IrCl(CO)(PPh 3 ) 2 и IrCl(CO)(PMe 2 Ph) 2 оба находятся при 1960 см-1. −1 , тогда как ν CO для IrCl(CO)(PMe 3 ) 2 находится при 1938 см-1. −1 . [4] [5]
По основности диметилфенилфосфин занимает промежуточное положение между триалкил- и трифенилфосфином: [6] [7]
- [HPEt 3 ] + = 8.7
- [HPMe 2 Ф] + = 6.8
- [ГФФ 3 ] + = 2.7
лиганда Угол конуса (θ) представляет собой угол при вершине цилиндрического конуса, центр которого находится на расстоянии 2,28 Å от центра атома P. Однако угол конуса несимметричного лиганда определить таким же образом невозможно. Чтобы определить эффективный угол конуса для несимметричного лиганда PX 1 X 2 X 3 , используется следующее уравнение:
Где θ i представляет половину угла.
Результирующие углы для PMe 3 , PMe 2 Ph, PPh 3 составляют:PMe 3 = 118°, PMe 2 Ph = 122°, PPh 3 = 145°. Таким образом, PMe 2 Ph занимает промежуточное положение по размеру относительно PMe 3 и PPh 3 . [8]
Ссылки
[ редактировать ]- ^ К. Фраерман; Б. Менье (1983). Получение диметилфенилфосфина . Неорганические синтезы. Том. 22. С. 133–135. дои : 10.1002/9780470132531 . ISBN 9780470132531 .
- ^ Ласло Т. Мика; Ласло Орха; Норберт Фаркас; Иштван Т. Хорват (2009). «Эффективный синтез водорастворимых алкил-бис(м-сульфированный фенил)- и диалкил-(м-сульфированный фенил)фосфинов и их оценка при катализируемом родием гидрировании малеиновой кислоты в воде». Металлоорганические соединения . 28 (5): 1593. doi : 10.1021/om800570r .
- ^ Новиков, ВП; Коломеец В.И., Сыщиков Ю.В. Н.; Вилков Л.В.; Ярков А.В.; Цветков Е.Н.; Раевский О.А. "Исследование структуры диметилфенилфосфина методами газофазной электронографии и колебательной спектроскопии" Ж. с. Структ. Хим. (J. Struc. Chem.) 1984, том 25, № 5, 688. два : 10.1007/BF00747909
- ^ С.А. Коттон, Химия драгоценных металлов., 1997, 152-157, ISBN 0-7514-0413-6 , ISBN 978-0-7514-0413-5
- ^ А. Р. Норрис; Дж. А. Кессель, «Окислительное присоединение 3,5-динитробензоилхлорида к транс -хлоркарбонилбис(диметилфенилфосфин)иридию (I) Canadian Journal of Chemistry , 1973, том 51, 4145-4151, два : 10.1139/CJC-51-24-4145 .
- ^ Рассел К. Буш; Роберт Дж. Анджеличи (1988). «Основность фосфина, определенная по энтальпии протонирования». Неорг. Хим . 27 (4): 681–686. дои : 10.1021/ic00277a022 .
- ^ Тяньшу Ли; Алан Дж. Лох; Роберт Х. Моррис (2007). «Шкала кислотности тетрафторборатных солей соединений фосфония и гидрида железа в [D2] дихлорметане». Химия: Европейский журнал . 13 (13): 3796–3803. дои : 10.1002/chem.200601484 . ПМИД 17245785 . .
- ^ CA Толман, Chem. Rev. , Стерические эффекты фосфорных лигандов в металлоорганической химии и гомогенном катализе., 1977, том 77, страницы 313-348. два : 10.1021/cr60307a002


