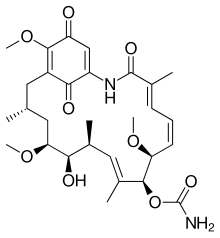
Гелданамицин
| |
| Имена | |
|---|---|
| Название ИЮПАК
(4 E , 6 Z , 8 S , 9 S , 10 E , 12 S , 13 R , 14 S , 16 R )-13-гидрокси-
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 29 Н 40 Н 2 О 9 | |
| Молярная масса | 560.64 g/mol |
| Появление | Мелкокристаллический порошок золотисто-желтого цвета. |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Гелданамицин представляет собой 1,4-бензохинон- ансамицина противоопухолевый антибиотик , который ингибирует функцию Hsp90 (белок теплового шока 90) путем связывания с необычным АДФ/АТФ-связывающим карманом белка. [ 1 ] Белки-клиенты HSP90 играют важную роль в регуляции клеточного цикла, росте клеток, выживании клеток, апоптозе , ангиогенезе и онкогенезе . [ 2 ]
Гелданамицин индуцирует деградацию белков, которые мутированы или сверхэкспрессируются в опухолевых клетках, таких как v-Src , Bcr-Abl , p53 и ERBB2 . Этот эффект опосредован HSP90. Несмотря на свой мощный противоопухолевый потенциал, гелданамицин имеет несколько серьезных недостатков в качестве кандидата на лекарственное средство, таких как гепатотоксичность , кроме того, Jilani et al. . , что гелданамицин индуцирует апоптоз эритроцитов сообщили при физиологических концентрациях. [ 4 ] Эти побочные эффекты привели к разработке аналогов гельданамицина, в частности аналогов, содержащих дериватизацию в 17-м положении:
Биосинтез
[ редактировать ]Гелданамицин был первоначально обнаружен в организме Streptomyces hygroscopeus . [ 5 ] Это макроциклический поликетид, который синтезируется поликетидсинтазой I типа . Гены gelA, gelB и gelC кодируют поликетидсинтазу. ПКС сначала загружается 3-амино-5-гидроксибензойной кислотой (АНБА). Затем он использует малонил-КоА , метилмалонил-КоА и метоксималонил-КоА для синтеза молекулы-предшественника прогельданамицина. [ 6 ] Этот предшественник подвергается нескольким ферментативным и неферментативным стадиям адаптации для получения активной молекулы гельданамицина, которые включают гидроксилирование, о-метилирование, карбамоилирование и окисление. [ 7 ]
Примечания
[ редактировать ]- ^ Шульте, ТВ; Акинага, С.; Сога, С.; Салливан, В.; Стенсгард, Б.; Тофт, Д.; Некерс, LM (1998). «Антибиотик радицикол связывается с N-концевым доменом Hsp90 и разделяет важную биологическую активность с гелданамицином» . Клеточные стрессы и шапероны . 3 (2): 100–108. doi : 10.1379/1466-1268(1998)003<0100:ARBTTN>2.3.CO;2 (неактивен 26 апреля 2024 г.). ПМК 312953 . ПМИД 9672245 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка ) - ^ Уэйн, Н.; Мишра, П.; Болон, Д.Н. (2011). «Hsp90 и созревание клиентского белка». Молекулярные шапероны . Методы Мол Биол. Том. 787. стр. 33–44. дои : 10.1007/978-1-61779-295-3_3 . ISBN 978-1-61779-294-6 . ПМК 5078872 . ПМИД 21898225 .
- ^ Стеббинс, CE; Руссо, А.А.; Шнайдер, К.; Розен, Н.; Хартл, ФУ; Павлетич, Н.П. (1997). «Кристаллическая структура комплекса Hsp90-гелданамицин: нацеливание белка-шаперона противоопухолевым агентом» . Клетка . 89 (2): 239–250. дои : 10.1016/S0092-8674(00)80203-2 . ПМИД 9108479 . S2CID 5253110 .
- ^ Джилани, Кашиф; Кадри, Сайед М.; Ланг, Флориан (2013). «Гельданамицин-индуцированная транслокация фосфатидилсерина в мембране эритроцитов» . Клеточная Физиол Биохимия . 32 (6): 1600–1609. дои : 10.1159/000356596 . ПМИД 24335345 .
- ^ Он, В.; Ву, Л.; Гао, К.; Ду, Ю.; Ван, Ю. (2006). «Идентификация генов биосинтеза AHBA, связанных с биосинтезом гельданамицина у Streptomyces hygroscopeus 17997». Современная микробиология . 52 (3): 197–203. дои : 10.1007/s00284-005-0203-y . ПМИД 16502293 . S2CID 22291736 .
- ^ Ким, В.; Ли, Д.; Хонг, СС; На, З.; Шин, Джей Си; Ро, С.Х.; Ву, Чехия; Чой, О.; Лук-порей.; Шен, Ю.М.; Пайк, СГ; Ли, Джей-Джей; Хонг, Ю.С. (2009). «Рациональная биосинтетическая инженерия для оптимизации аналогов гелданамицина». ХимБиоХим . 10 (7): 1243–1251. дои : 10.1002/cbic.200800763 . ПМИД 19308924 . S2CID 3273370 .
- ^ Ли, Д.; Лук-порей.; Кай, XF; Дат, Северная Каролина; Буванахалли, СК; Ли, М.; Шин, Джей Си; Ким, В.; Чон, Дж. К.; Ли, Дж. С.; Ли, Швейцария; Ли, Дж. Х.; Хонг, Ю.С.; Ли, Джей-Джей (2006). «Биосинтез ингибитора белка теплового шока 90 гелданамицина: новый взгляд на образование бензохинонового фрагмента». ХимБиоХим . 7 (2): 246–248. дои : 10.1002/cbic.200500441 . ПМИД 16381049 . S2CID 42998903 .
Ссылки
[ редактировать ]- Бедин, М.; Габен, AM; Сосье, CC; Местер, Дж. (2004). «Гельданамицин, ингибитор шаперонной активности HSP90, индуцирует МАРК-независимую остановку клеточного цикла» . Международный журнал рака . 109 (5): 643–652. дои : 10.1002/ijc.20010 . ПМИД 14999769 . S2CID 39451213 .