Дифенилфосфин
| |

| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Дифенилфосфан | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.011.447 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 12 Ч 11 П | |
| Молярная масса | 186.19 g/mol |
| Появление | бесцветная жидкость |
| Плотность | 1,07 г/см 3 , жидкость |
| Точка кипения | 280 ° С (536 ° F; 553 К) |
| нерастворимый | |
| Опасности | |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х250 , Х315 , Х319 , Х335 | |
| P210 , P222 , P261 , P264 , P271 , P280 , P302+P334 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313 , P337+P313 , П362 , П370+П378 , П403+П233 , П405 , П422 , П501 | |
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
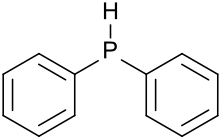
Дифенилфосфин , также известный как дифенилфосфан, представляет собой фосфорорганическое соединение формулы (C 6 H 5 ) 2 PH. Эта бесцветная жидкость с неприятным запахом легко окисляется на воздухе. Это предшественник фосфорорганических лигандов для использования в качестве катализаторов .
Синтез
[ редактировать ]Дифенилфосфин можно получить из трифенилфосфина восстановлением до дифенилфосфида лития , который можно протонировать с получением указанного в заголовке соединения: [ 1 ]
- ПФ 3 + 2 Li → LiPPh 2 + LiPh
- LiPPh 2 + H 2 O → Ph 2 PH + LiOH
Использование и реакции
[ редактировать ]В лаборатории дифенилфосфин является распространенным промежуточным продуктом. Его можно депротонировать с образованием производных дифенилфосфида: [ 2 ]
- Ф 2 ФН + н BuLi → Ph 2 PLi + н БуХ
Получение фосфиновых лигандов , реагентов Виттига-Хорнера и фосфониевых солей обычно осуществляют путем алкилирования дифенилфосфина. Атом водорода, связанный с фосфором, подвергается присоединению по принципу Михаэля к активированным алкенам, образуя продукты, из которых образуются фосфиновые лиганды, такие как 1,2-бис(дифенилфосфино)этан (Ph 2 PC 2 H 4 PPh 2 ) и BINAP . [ 3 ] через его бис- трифлатные производные. Оба ( R )- и ( S ) -энантиомеры , а также рацемат коммерчески доступны. Одно из широких применений включает хемоселективное гидрирование, при котором BINAP конъюгирован с родием.
Производные дифенилфосфина и особенно дифенилфосфида являются нуклеофилами, поэтому они присоединяются по двойным связям углерод – гетероатом. [ 2 ] Например, в присутствии концентрированной соляной кислоты при 100 °C дифенилфосфин присоединяется к атому углерода бензальдегида с образованием (фенил-(фенилметил)фосфорил)бензола.
- Ф 2 PH + PhCHO → Ф 2 P(O)CH 2 Ph
По сравнению с третичными фосфинами дифенилфосфин является слабоосновным. pKa протонированного производного составляет 0,03: [ 4 ]
- Ф 2 Ф 2 + ⇌ Фаза 2 ФН + Н +
Обработка свойств
[ редактировать ]Дифенилфосфин легко окисляется. [ 5 ]
- Ph 2 PH + O 2 → Ph 2 P(O)OH
Промежуточным продуктом этого окисления является оксид дифенилфосфина . Использование дифенилфосфин-боранового комплекса Ph 2 PH•BH 3 позволяет избежать проблемы окисления фосфина, защищая фосфин от окисления, и его можно приобрести у поставщиков химической продукции. [ 2 ]
Ссылки
[ редактировать ]- ^ В.Д. Бьянко; С. Доронцо (1976). «Дифенилфосфин». Неорганические синтезы . Том. 16. С. 161–188. дои : 10.1002/9780470132470.ch43 . ISBN 9780470132470 .
- ^ Jump up to: а б с Пиотровски, Д.В. (2001). «Дифенилфосфин». Энциклопедия реагентов для органического синтеза . Нью-Йорк: Джон Уайли и сыновья. дои : 10.1002/047084289X.rd427 . ISBN 0471936235 .
- ^ Цай, Дунвэй; Дж. Ф. Пайак; доктор Бендер; Д. Л. Хьюз; Т.Р. Верховен; Пи Джей Рейдер (1999). «( R )-(+)- и ( S )-(-)-2,2'-бис(дифенилфосфино)-1,1'-бинафтил (BINAP)» . Органические синтезы . 76 :6 .
- ^ CA Streuli, «Определение основности замещенных фосфинов методом неводной титриметрии», Analytical Chemistry 1960, том 32, страницы 985-987. два : 10.1021/ac60164a027
- ^ Свара, Дж.; Веферлинг, Н.; Хофманн, Т. «Органические соединения фосфора». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a19_545.pub2 . ISBN 978-3527306732 .