фосфоний


4 , исходный катион фосфония.
В химии термин фосфоний (более неясно: фосфиний ) описывает многоатомные катионы с химической формулой P R +
4 (где R представляет собой водород или алкильную , арильную или галогенидную группу). Эти катионы имеют тетраэдрическую структуру . Соли обычно бесцветны или принимают цвет анионов. [ 1 ]
Типы катионов фосфония
[ редактировать ]Протонированные фосфины
[ редактировать ]Исходный фосфоний - PH. +
4 , обнаруженный в йодистой соли, йодиде фосфония . Соли исходного PH +
4 встречаются редко, но этот ион является промежуточным продуктом при получении промышленно используемого хлорида тетракис(гидроксиметил)фосфония :
- PH 3 + HCl + 4 CH 2 O → P(CH
2 ОХ) +
4 кл −
Многие фосфониевые соли получают протонированием первичных, вторичных и третичных фосфинов :
- ПР 3 + Н + → HPR +
3
Основность фосфинов соответствует обычным тенденциям: R = алкил более основной, чем R = арил. [ 2 ]
Катионы тетраорганофосфония
[ редактировать ]Наиболее распространенные соединения фосфония имеют четыре органических заместителя, присоединенных к фосфору. Катионы четвертичного фосфония включают тетрафенилфосфоний , (C 6 H 5 ) 4 P + и тетраметилфосфоний P(CH
3 ) +
4 .


Катионы четвертичного фосфония ( PR +
4 ) получают алкилированием органофосфинов. [ 3 ] Например, реакция трифенилфосфина с бромистым метилом дает бромид метилтрифенилфосфония :
- ПФ 3 + СН 3 Br → [СН 3 ППф 3 ] + Бр −
Метильная группа в таких фосфониевых солях умеренно кислая, с ap K, по оценкам , около 15: [ 5 ]
- [CH 3 PPh 3 ] + + основание → CH 2 =PPh 3 + [Hbase] +
Эта реакция депротонирования дает реагенты Виттига . [ 6 ]
Пентахлорид фосфора и родственные соединения
[ редактировать ]Твердый пентахлорид фосфора представляет собой ионное соединение , имеющее формулу PCl. +
4 ПКл −
6 , то есть соль, содержащая катион тетрахлорфосфония. [ 7 ] [ 8 ] Разбавленные растворы диссоциируют по следующему равновесию:
- ПКл 5 ⇌ ПКл +
4 + кл −
Трифенилфосфиндихлорид (Ph 3 PCl 2 ) существует как в виде пентакоординированного фосфорана, так и в виде хлорида хлортрифенилфосфония, в зависимости от среды. [ 9 ] Ситуация аналогична ситуации с PCl 5 . Это ионное соединение (PPh 3 Cl). + кл. − в полярных растворах и молекулярные разновидности с тригонально-бипирамидальной молекулярной геометрией в неполярном растворе. [ 10 ]
Соли алкоксифосфония: реакция Арбузова
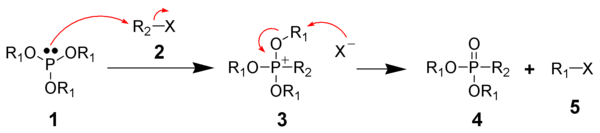
[ редактировать ]Реакция Михаэлиса-Арбузова представляет собой химическую реакцию сложного эфира трехвалентного фосфора с алкилгалогенидом с образованием разновидностей пятивалентного фосфора и другого алкилгалогенида. Обычно фосфорным субстратом является фосфитный эфир (P(OR) 3 ), а алкилирующим агентом является алкилйодид. [ 11 ]
Использование
[ редактировать ]Текстильная отделка
[ редактировать ]
Хлорид тетракис(гидроксиметил)фосфония имеет промышленное значение в производстве устойчивых к складкам и огнестойких покрытий на хлопчатобумажных тканях и других целлюлозных тканях. [ 12 ] [ 13 ] Огнестойкое покрытие можно получить из THPC с помощью процесса Proban. [ 14 ] в котором THPC обрабатывается мочевиной. Мочевина . конденсируется с гидроксиметильными группами на THPC структура фосфония преобразуется в оксид фосфина . В результате этой реакции [ 15 ]
Катализаторы фазового переноса и осадители
[ редактировать ]Органические катионы фосфония липофильны и могут быть полезны в катализе фазового переноса , как и соли четвертичного аммония. Соли или неорганические анионы и тетрафенилфосфоний ( PPh +
4 ) растворимы в полярных органических растворителях. Одним из примеров является перренат (PPh 4 [ReO 4 ]). [ 16 ]
Реагенты для органического синтеза
[ редактировать ]Реактивы Виттига используются в органическом синтезе . Они получены из солей фосфония. сильное основание, такое как бутиллитий Для депротонирования требуется или амид натрия:
- [Ф 3 П + СН 2 R]X − + C 4 H 9 Li → Ph 3 P=CHR + LiX + C 4 H 10
Одним из простейших илидов является метилентрифенилфосфоран (Ph 3 P=CH 2 ). [ 6 ]
Соединения Ph 3 PX 2 (X = Cl, Br) используются в реакции Кирсанова . [ 17 ] Реакцией Киннера -Перрена получают алкилфосфонилдихлориды (RP(O)Cl 2 ) и сложные эфиры (RP(O)(OR') 2 ). Ключевым промежуточным продуктом являются соли алкилтрихлорфосфония, полученные алкилированием трихлорида фосфора : [ 18 ]
- RCl + PCl 3 + AlCl 3 → [RPCl 3 ] + AlCl −
4
Производство аммиака для «зеленого водорода»
[ редактировать ]Сегодня основной промышленной процедурой производства аммиака является термический процесс Габера-Боша , в котором в качестве источника водорода обычно используется ископаемый газ, который затем объединяется с азотом для производства аммиака. В 2021 году профессор Дуг Макфарлейн и его коллеги Александр Симонов и Брайан Сурианто из Университета Монаша разработали метод производства зеленого аммиака, который потенциально может сделать установки Хабер-Боша устаревшими. [ 19 ] Их процесс аналогичен методу электролиза для получения водорода. Работая с местной компанией Verdant, которая хотела производить отбеливатель из соленой воды путем электролиза, Сурианто обнаружил, что соль тетраалкилфосфония позволяет эффективно производить аммиак при комнатной температуре. [ 20 ]
См. также
[ редактировать ]- Аммоний ( NH +
4 ) - Арсоний ( AsH +
4 ) - Гидроний (H 3 O + )
- Ониевые соединения
- Фосфорорганическая химия
Ссылки
[ редактировать ]- ^ Корбридж, Декабрь (1995). Фосфор: очерк химии, биохимии и технологии (5-е изд.). Амстердам: Эльзевир. ISBN 978-0-444-89307-9 .
- ^ Ли, Т.; Лох, Эй Джей; Моррис, Р.Х. (2007). «Шкала кислотности тетрафторборатных солей фосфониевых и гидридных соединений железа в [D 2 ]дихлорметане». хим. Евро. Дж . 13 (13): 3796–3803. дои : 10.1002/chem.200601484 . ПМИД 17245785 .
- ^ Перейти обратно: а б Х.-Ф. Кляйн (1978). «Метилид триметилфосфония (триметилметиленфосфоран)». Неорганические синтезы . Неорганические синтезы. Том. 18. С. 138–140. дои : 10.1002/9780470132494.ch23 . ISBN 9780470132494 .
- ^ Финч, А.; Фитч, АН; Гейтс, ПН (1993). «Кристаллическая и молекулярная структура метастабильной модификации пентахлорида фосфора». Журнал Химического общества, Chemical Communications (11): 957–958. дои : 10.1039/c39930000957 .
- ^ Лин-Чунг, Сим; Продажи, Кейт Д.; Атли, Джеймс HP (1990). «Измерение значений p K a для солей фосфония посредством кинетики переноса протона на электрогенерированное основание». Журнал Химического общества, Chemical Communications (9): 662. doi : 10.1039/C39900000662 .
- ^ Перейти обратно: а б Виттиг; Шелькопф, У. (1960). «Метиленциклогексан». Органические синтезы . 40:66 . дои : 10.15227/orgsyn.040.0066 . . Описывает Ph 3 P=CH 2 .
- ^ Холлеман, А.Ф.; Вибер, Э.; Виберг, Н. (2001). Неорганическая химия . Академическая пресса. ISBN 978-0-12-352651-9 .
- ^ Сутер, RW; Кначел, ХК; Петр, вице-президент; Ховатсон, Дж. Х. и Шор, С. Г. (1978). «Природа хлорида фосфора (V) в ионизирующих и неионизирующих растворителях». Журнал Американского химического общества . 95 (5): 1474–1479. дои : 10.1021/ja00786a021 .
- ^ С.М. Годфри; Калифорния Маколифф; Р.Г. Причард; Дж. М. Шеффилд (1996). «Рентгеновское кристаллорографическое исследование реагента Ph 3 PCl 2 ; не с переносом заряда, R 3 P–Cl–Cl, тригонально-бипирамидальный или [R 3 PCl]Cl, а необычный двухъядерный ионный тип, [Ph 3 PCl] + ⋯Cl – ⋯ + CIPPh 3 ]Cl, содержащий длинные контакты Cl-Cl». Chemical Communications (22): 2521–2522. doi : 10.1039/CC9960002521 .
- ^ Дженнингс, EV; Никитин, К; Ортин, Ю; Гилхиани, генеральный директор (2014). «Вырожденное нуклеофильное замещение в фосфониевых солях». Дж. Ам. хим. Соц . 136 (46): 16217–16226. дои : 10.1021/ja507433g . ПМИД 25384344 .
- ^ Бхаттачарья, АК; Тьягараджан, Г. (1981). «Перегруппировка Михаэлиса – Арбузова». хим. Преподобный о. 81 (4): 415–430. дои : 10.1021/cr00044a004 .
- ^ Вейл, Эдвард Д.; Левчик, Сергей В. (2008). «Антипирены в коммерческом использовании или разработке для текстиля». Дж. Наука о пожаре. 26 (3): 243–281. дои : 10.1177/0734904108089485 . S2CID 98355305 .
- ^ Свара, Юрген; Веферлинг, Норберт ; Хофманн, Томас. Соединения фосфора органические. Энциклопедия промышленной химии Ульмана. Джон Уайли и сыновья, Inc., 2008 г. два : 10.1002/14356007.a19_545.pub2
- ^ «Часто задаваемые вопросы: Что такое процесс PROBAN®?» . Родия Пробан. Архивировано из оригинала 7 декабря 2012 года . Проверено 25 февраля 2013 г.
- ^ Ривз, Уилсон А.; Гатри, Джон Д. (1956). «Промежуточный продукт для огнестойких полимеров - реакции хлорида тетракис (гидроксиметил) фосфония». Промышленная и инженерная химия . 48 (1): 64–67. дои : 10.1021/ie50553a021 .
- ^ Дилворт-младший; Хусейн, В.; Хатсон, Эй Джей; Джонс, CJ; Маккуиллан, Ф.С. (1996). «Тетрагалогеноксоренат-анионы». Неорганические синтезы . Неорганические синтезы. Том. XXXI. стр. 257–262. дои : 10.1002/9780470132623.ch42 . ISBN 9780470132623 .
- ^ Исследования по фосфорорганической химии. I. Превращение спиртов и фенолов в галогениды третичными дигалогенидами фосфина Г.А. Уайли, Р.Л. Гершковитц, Б.М. Рейн, BC Чунг Дж. Ам. хим. Соц. , 1964 , 86 (5), стр. 964–965. два : 10.1021/ja01059a073
- ^ Свара, Дж.; Веферлинг, Н.; Хофманн, Т. «Органические соединения фосфора». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a19_545.pub2 . ISBN 978-3527306732 .
- ^ Прорыв приближает производство экологически чистого аммиака к реальности.
- ^ Восстановление азота до аммиака с высокой эффективностью и скоростью на основе фосфониевого протонного челнока.