Окисление спиртов до альдегидов сульфонием.
Окисление спиртов до альдегидов на основе сульфония суммирует группу органических реакций , которые превращают первичный спирт в соответствующий альдегид (и вторичный спирт в соответствующий кетон ). Селективное окисление спиртов до альдегидов требует предотвращения чрезмерного окисления до карбоновой кислоты. Одним из популярных подходов являются методы, в которых используются промежуточные формы алкоксисульфония ( RO-SMe +
2 X- , например соединение 6 ), как подробно описано здесь. Поскольку в большинстве этих методов в качестве окислителя используется диметилсульфоксид (ДМСО) и образуется диметилсульфид , их часто в разговорной речи называют окислением ДМСО. Концептуально, получение альдегида и диметилсульфида из спирта и ДМСО требует дегидратирующего агента для удаления H 2 O, в идеале электрофила, одновременно активирующего ДМСО. Напротив, методы получения промежуточного сульфония из диметилсульфида не требуют дегидратирующего агента. Тесно связаны окисления, опосредованные диметилселеноксидом и диметилселенидом. [ 1 ]
Сравнение с родственными методами
[ редактировать ]Для сравнения, методы на основе сульфония популярны, поскольку реакции эффективны (высокие выходы, сравнительно быстро, отсутствие переокисления, мало побочных реакций, воспроизводимые результаты), условия реакции мягкие (низкая температура, отсутствие сильных кислот и оснований), реакции они просты в эксплуатации (не требуется специального оборудования или необычных и/или дорогостоящих реагентов, побочные продукты часто легко отделяются, устойчивы к кислороду и влаге), и они, как правило, не требуют использования высокотоксичных исходных материалов и утилизации токсичных отходов. Однако эти реакции не слишком популярны среди многих студентов-химиков, работающих в лаборатории, поскольку обычный побочный продукт — диметилсульфид — имеет сильный запах, напоминающий запах яиц, поэтому требует хорошо вентилируемого вытяжного шкафа. Другие недостатки могут включать избыток основания, обращение с дегидратирующим агентом, ограниченный выбор растворителя или побочные реакции при повышенной температуре, например, перегруппировку Паммерера или удаление сульфониевого промежуточного продукта до реакционноспособного H 2 C=(S+)-CH 3. -виды, образующие метилтиометиловые эфиры со спиртами. Вследствие этого это означает, что активность окисления не может регулироваться по желанию путем повышения температуры реакции, например, для ускорения окисления нереакционноспособного спирта.
Распространенной альтернативой этим методам на основе сульфония являются окисления с
- гипервалентный йод (например, периодинан Десс-Мартина , 2-йодоксибензойная кислота )
- реагенты хрома (например, хлорхромат пиридиния , реактив Коллинза )
- оксиды рутения (например, перрутенат тетрапропиламмония )
- виды оксоаммония (например, TEMPO )
- перенос гидрирования или перенос гидрида (например, окисление Оппенауэра )
- MnO 2 , Манганат бария , 2,3-Дихлор-5,6-дициано-1,4-бензохинон для аллиловых спиртов
Категории
[ редактировать ]Окисления сульфония можно разделить на две группы: методы, открытые раньше всех, основаны на использовании активированных спиртов, таких как алкилтозилаты ( окисление Корнблюма ). [ 2 ] или алкилхлорформиаты (из реакции спиртов с фосгеном: Бартона-Корнблюма) [ 3 ] которые реагируют как электрофилы при обработке ДМСО, высвобождая кислородсодержащую уходящую группу (например, OTs- ). Однако дополнительная стадия предварительной активации спирта и иногда жесткие условия реакции нуклеофильного замещения оказались менее удобными. Поэтому позже были разработаны методы получения активированных сульфоксидов. Ниже изображен активированный сульфоксид, образующийся при окислении Сверна 4 при реакции со вторичным спиртом 5 с образованием алкоксисульфониевых разновидностей 6 .
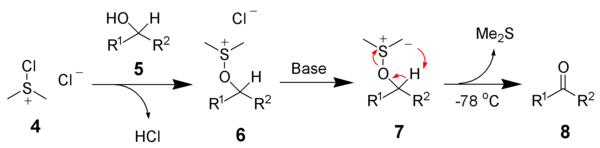
Эти активированные сульфоксиды реагируют как электрофилы при обработке спиртом, удаляя уходящую группу, которая может одновременно действовать как противоион по отношению к алкоксисульфониевым формам ( RO-SMe +
2 ) генерируется. При депротонировании, которому обычно способствует мягкое основание, такое как триэтиламин, алкоксисульфоний разлагается с образованием альдегида и диметилсульфида. Последняя коллекция содержит популярные окисления, такие как
а также включает Олбрайта-Голдмана , Олбрайта-Онодера (ДМСО/P 2 O 5 ), ТФАА /ДМСО (Swern) и Me 2 S/Cl 2 . Недавно SO 2 F 2 был предложен для получения активированного сульфоксида из ДМСО. [ 4 ]
См. также
[ редактировать ]- Окисление спирта
- Окисление комплексами хром(VI)-амина.
- Окисление, катализируемое оксоаммонием
- Окисление Десса – Мартина
Ссылки
[ редактировать ]- ^ Тидвелл, Т.Т. (1990). «Окисление спиртов до карбонильных соединений посредством алкоксисульфоний-илидов: процессы Моффатта, Сверна и родственные окисления». doi: 10.1002/0471264180.or039.03». Органические реакции : 297–555. дои : 10.1002/0471264180.или039.03 .
- ^ Корнблюм, Н.; Джонс, WJ; Андерсон, Дж.Дж. (1959). «Новый селективный метод окисления. Превращение алкилгалогенидов и алкилтозилатов в альдегиды». Дж. Ам. хим. Соц. 81 (15): 4113–4114. дои : 10.1021/ja01524a080 .
- ^ Бартон, DHR; Гарнер, Би Джей; Уайтман, Р.Х. (1964). «Новый метод окисления спиртов». Дж. Хим. Соц. : 1855–1857. дои : 10.1039/JR9640001847 .
- ^ Жа, Г.-Ф.; Фанг, Вирджиния; Ленг, Дж.; Цинь, Х.-Л. (2019). «Простое, умеренное и общее окисление спиртов до альдегидов или кетонов SO 2 F 2 /K 2 CO 2 с использованием ДМСО в качестве растворителя и окислителя». Адв. Синтез. Катал. 361 (10): 2262–2267. дои : 10.1002/adsc.201900104 .