Период Десс – Мартина
| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
3-Оксо-1л 5 ,2-benziodoxole-1,1,1(3 H )-triyl triacetate | |
| Другие имена
Период Десс – Мартина
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.197.885 |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 13 Ч 13 ИО 8 | |
| Молярная масса | 424.14 g/mol |
| Появление | белый порошок, чипсы, кристаллы или кристаллический порошок и/или кусочки |
| Плотность | 1,362 г/см 3 твердый |
| Температура плавления | От 103 до 133 ° C (от 217 до 271 ° F; от 376 до 406 К) |
| Родственные соединения | |
Родственные соединения
|
2-йодоксибензойная кислота |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
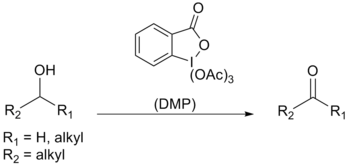
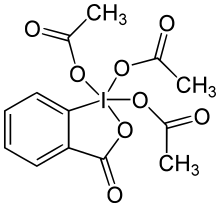
Периодинан Десса-Мартина ( DMP ) — химический реагент, используемый при окислении Десса-Мартина , окисляющем первичные спирты до альдегидов и вторичные спирты до кетонов . [ 1 ] [ 2 ] Этот периодинан имеет несколько преимуществ перед окислителями на основе хрома и ДМСО , которые включают более мягкие условия (комнатная температура, нейтральный pH), более короткое время реакции, более высокие выходы, упрощенные методы обработки, высокую хемоселективность, толерантность к чувствительным функциональным группам и длительный срок хранения. Однако использование в промышленных масштабах затруднено из-за его стоимости и потенциально взрывоопасного характера. [ 3 ] Он назван в честь американских химиков Дэниела Бенджамина Десса и Джеймса Каллена Мартина, которые разработали реагент в 1983 году. Он основан на IBX , но из-за ацетатных групп, присоединенных к центральному атому йода, DMP гораздо более реакционноспособен, чем IBX, и значительно более активен. более растворим в органических растворителях. [ 4 ]
Подготовка
[ редактировать ]Было установлено, что наиболее щадящим синтезом IBX является обработка 2-йодбензойной кислоты в оксоном воде при повышенных температурах в течение 3 часов. [ 5 ] Затем IBX ацилируют с использованием соединений Ирландии и Лю. [ 6 ] изменения исходной процедуры. Эти модификации позволили повысить выходы и упростить процедуру обработки. Полученные твердые вещества можно получить фильтрованием и промыванием эфиром. Айрленд и Лю использовали каталитическое количество тозиловой кислоты , что позволило реакции завершиться менее чем за 2 часа (по сравнению с классическим синтезом, требующим 24 часов) и с выходами, превышающими 90%.
Классический метод, представленный Р.К. Бекманом и Дж.Дж. Маллинзом. [ 7 ] включал нагревание раствора бромата калия , серной кислоты и 2-иодбензойной кислоты с получением IBX (1-гидрокси-1,2-бензиодоксол-3(1H)-он-1-оксид, 2-иодоксибензойная кислота ). Затем IBX ацилировали с использованием уксусной кислоты и уксусного ангидрида .
Структура
[ редактировать ]ДМП имеет квадратно-пирамидальную геометрию с 4 гетероатомами в базальных положениях и одной апикальной фенильной группой.
Механизм окисления
[ редактировать ]Периодинан Десса-Мартина в основном используется в качестве окислителя для сложных, чувствительных и многофункциональных спиртов . Одной из причин его эффективности является высокая селективность к комплексообразованию гидроксильной группы , что позволяет спиртам быстро осуществлять лигандный обмен; первый этап реакции окисления.
Протонный ЯМР показал, что при использовании одного эквивалента спирта образуется промежуточный диацетоксиалкоксипериодинан. Затем ацетат действует как основание для депротонирования α-H из спирта с образованием карбонильного соединения, йодинана и уксусной кислоты .
При диола использовании или более чем одного эквивалента спирта вместо него образуется ацетоксидиалкоксипериодинан. Из-за лабильной природы именно этого периодинана окисление происходит гораздо быстрее. [ 4 ]
Шрайбер и его коллеги показали, что вода увеличивает скорость реакции окисления. [ 8 ] Десс и Мартин первоначально заметили, что окисление этанола усиливается при наличии дополнительного эквивалента этанола. Считается, что скорость диссоциации конечного ацетатного лиганда от йода увеличивается из-за электронодонорной способности гидроксильной группы (тем самым ослабляя связь I-OAc). [ 4 ]
Хемоселективность
[ редактировать ]Используя стандартные условия периодинана Десса-Мартина, спирты можно окислить до альдегидов/кетонов, не затрагивая фурановые кольца, сульфиды , виниловые эфиры и вторичные амиды . [ 4 ] Аллиловые спирты легко окисляются с помощью ДМФ, которые обычно трудно превратить в соответствующие карбонилы с использованием типичных окислителей. [ 9 ]
Майерс и его коллеги определили, что ДМП может окислять N-защищенные аминоспирты без эпимеризации (в отличие от большинства других окислителей, включая окисление Сверна). Эти защищенные аминоспирты могут иметь очень важное значение в фармацевтической промышленности. [ 10 ]
Бензиловые и аллиловые спирты реагируют быстрее, чем насыщенные спирты. [ 4 ] в то время как ДМП окисляет альдоксимы и кетоксимы до соответствующих альдегидов и кетонов быстрее, чем первичный, вторичный или бензиловый спирт до соответствующего карбонила. [ 11 ]
Один из примеров окисления Десса-Мартина включает преобразование чувствительного α-β-ненасыщенного спирта в соответствующий ему альдегид. Этот фрагмент был обнаружен в нескольких натуральных продуктах и благодаря своей высокой функциональности может быть ценным синтетическим строительным блоком в органическом синтезе. Тонгсорнклиб и Данхайзер окислили этот чувствительный спирт, применив окисление Десса Мартина и изменив процедуру обработки (разбавление пентанами, промывание поли( 4-винилпиридином ) для удаления уксусной кислоты, образующейся во время реакции, фильтрование и концентрирование путем перегонки). [ 12 ]
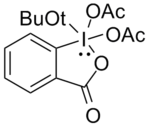
т -Бутил ДМП
[ редактировать ]Дифтор- и монофторспирты окисляются труднее. Было использовано окисление Сверном , но пришлось использовать большой избыток окислителя, что в некоторых случаях не давало воспроизводимых результатов. Линдерман и Грейвс [ 13 ] обнаружили, что ДМП был успешным в большинстве случаев, но не переносил присутствие нуклеофильных функциональных групп в спирте, поскольку они реагировали с ДМП, вытесняя ацетат. Использование соединения, показанного ниже, дает желаемые карбонилы с высокими выходами, поскольку добавление трет -бутоксигруппы из-за ее стерической массы сводит к минимуму эти побочные реакции.
См. также
[ редактировать ]- Окисление спирта
- Хлорохромат пиридиния
- Окисление Джонса
- Окисление Оппенауэра
- Окисление Пфицнера-Моффатта
- Окисление Париха – Деринга
- Окисление Олбрайта-Гольдмана
- Окисление Сверна
- Окисление Кори-Кима
- Лей-окисление ( окисление TPAP )
- ТЕМПО окисление
Ссылки
[ редактировать ]- ^ Десс, Д.Б.; Мартин, Джей Си (1983). «Легкодоступный окислитель 12-I-5 для превращения первичных и вторичных спиртов в альдегиды и кетоны». Дж. Орг. хим. 48 (22): 4155–4156. дои : 10.1021/jo00170a070 .
- ^ Бекман, Роберт Дж.; Джордж, Келли М. (2009). «1,1,1-Триацетокси-1,1-дигидро-1,2-бензиодоксол-3(1Н)-он». Энциклопедия реагентов для органического синтеза . дои : 10.1002/047084289X.rt157m.pub2 . ISBN 978-0471936237 .
- ^ Пламб, Дж. Б.; Харпер, диджей (1990). «Химическая безопасность: 2-йодоксибензойная кислота» . хим. англ. Новости . 68 : 3. doi : 10.1021/cen-v068n029.p002 .
- ^ Jump up to: а б с д и Десс, Д.Б.; Мартин, Джей Си (1991). «Полезный 12-I-5 триацетоксипериодинан (периодинан Десс-Мартина) для селективного окисления первичных или вторичных спиртов и множества родственных видов 12-I-5». Дж. Ам. хим. Соц. 113 (19): 7277–7287. дои : 10.1021/ja00019a027 .
- ^ Фриджерио, М.; Сантагостино, М.; Спьюторе, С. (1999). «Удобный для пользователя вход в 2-йодоксибензойную кислоту (IBX)». Дж. Орг. Хим . 64 (12): 4537–4538. дои : 10.1021/jo9824596 .
- ^ Ирландия, RE; Лю, Л. (1993). «Улучшенная процедура приготовления периодинана Десс-Мартена». Дж. Орг. Хим . 58 (10): 2899. doi : 10.1021/jo00062a040 .
- ^ Бекман-младший, РК; Шао, П.; Маллинз, Джей-Джей (2004). «Период Десс-Мартен» . Органические синтезы ; Сборник томов , т. 10, с. 696 .
- ^ Мейер, С.Д.; Шрайбер, С.Л. (1994). «Ускорение окисления Десс-Мартена водой». Дж. Орг. хим. 59 (24): 7549–7552. дои : 10.1021/jo00103a067 .
- ^ Лоуренс, Нью-Джерси; Крамп, JP; Макгоун, AT; Хэдфилд, Дж. А. (2001). «Реакция продуктов Бейлиса-Хиллмана с окислителями Сверна и Десс-Мартина». Тетраэдр Летт. 42 (23): 3939–3941. дои : 10.1016/S0040-4039(01)00587-1 .
- ^ Майерс, АГ; и др. (2000). «Синтез высокоэпимеризуемых N-защищенных _-аминоальдегидов с высоким энантиомерным избытком». Тетраэдр Летт. 41 : 1359. doi : 10.1016/S0040-4039(99)02293-5 .
- ^ Чаудхари, СС; Акаманчи, КГ (1999). «Мягкий хемоселективный окислительный метод деоксимации с использованием периодинана Десса-Мартина». Синтез . 1999 (5): 760–764. дои : 10.1055/s-1999-3476 .
- ^ Тонгсорнклиб, К.; Данхайзер, РЛ (2005). «Практический метод синтеза 2-алкинилпропеналей» . Дж. Орг. хим. 70 (6): 2364–2367. дои : 10.1021/jo047869a . ПМК 2897060 . ПМИД 15760233 .
- ^ Линдерман, Р.Дж.; Грейвс, DM (1989). «Окисление фторалкилзамещенных карбинолов реагентом Десса-Мартина». Дж. Орг. хим. 54 (3): 661–668. дои : 10.1021/jo00264a029 .