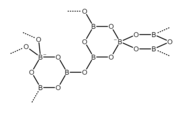
Борат
Борат . представляет собой любой из ряда бора оксианионов , анионов, содержащих бор и кислород , таких как ортоборат BO 3− 3 , метаборат BO - 2 , или тетраборат В 4 О 2- 7 ; или любая соль таких анионов, такая как метаборат натрия , Уже + [БО 2 ] − и бура (Что + ) 2 [Б 4 О 7 ] 2− . Название также относится к сложным эфирам таких анионов, например, триметилборату. B(OCH 3 ) 3 но они являются алкоксидами.
Естественное явление
[ редактировать ]Ионы бората встречаются отдельно или вместе с другими анионами во многих боратных и боросиликатных минералах , таких как бура , борацит , улексит (боронатрокальцит) и колеманит . Бораты также встречаются в морской воде, где они вносят важный вклад в поглощение низкочастотного звука в морской воде. [1]
Бораты также встречаются в растениях, включая почти все фрукты. [2]
Анионы
[ редактировать ]Основными боратными анионами являются:
- тетрагидроксиборат [Б(ОН) 4 ] − , содержится в тетрагидроксиборате натрия Na[B(OH) 4 ] .
- ортоборатный [ BO3 ] 3− , содержится в ортоборате тринатрия Na3 [ BO3 ]
- [БО
4 ] 5−
, обнаруженный в оксиапатите боросиликата кальция и иттрия Ca
33 года
77БО
4 (SiO
4 )
5 О - перборат [В 2 О 4 (ОН) 4 ] 2− , как в перборате натрия Na2 [ H4B2O8 B2O8]
- метаболиты [БО 2 ] − или его циклический тример [ B3O6 6] 3− , содержится в метаборате натрия Na3 [ B3O6 O6]
- диборировать [Б 2 О 5 ] 4− , содержится в диборате магния Mg 2 [B 2 O 5 ] ( суанит ),
- триборат [ B3O7 7] 5− , содержится в триборате кальция и алюминия Ca[AlB 3 O 7 ] ( йохахидолит ),
- тетраборат [Б 4 О 7 ] 2− , содержится в безводной буре Na2 [ B4O7 O7]
- тетрагидрокситетраборат [В 4 О 5 (ОН) 4 ] 2− , найденный в «декагидрате» буры. Na 2 [B 4 O 5 (OH) 4 ]·8H 2 O
- тетраборат(6-) [Б 4 О 9 ] 6− найден в тетраборате лития (6-) Ли 6 [В 4 О 9 ]
- пентаборат [Б 5 О 8 ] − или [Б 10 О 16 ] 2− , содержится в пентаборате натрия Na 2 [B 10 O 16 ]·10H 2 O
- октаборат [Б 8 О 13 ] 2− содержится в октаборате динатрия Na2 [ B8O13 O13]
- Строение тетрагидроксиборат-иона ( [Б(ОН) 4 ] − ). Этот анион имеет тетраэдрическую молекулярную геометрию у атома бора.
- Структура ортоборатного иона ( [ BO3 ] 3− ). Этот анион имеет тригональную плоскую молекулярную геометрию .
- Строение тримера метаборат-иона ( [ B3O6 6] 3− ). Этот анион представляет собой циклическую молекулу и имеет тригональную плоскую молекулярную геометрию у атомов бора. Все девять атомов этого аниона лежат в одной плоскости.
- Строение тетрагидрокситетраборат-иона ( [В 4 О 5 (ОН) 4 ] 2− ). Этот анион представляет собой мостиковую бициклическую молекулу, содержит кислорода, атомы соединяющие мостиковые атомы бора , которые связаны с четырьмя гидроксильными группами ( −OH ), по одному на каждый атом бора. Анион имеет тетраэдрическую молекулярную геометрию у двух тетракоординированных атомов бора и тригональную плоскую молекулярную геометрию у двух трехкоординированных атомов бора.
- Строение тетраборат-иона ( [Б 4 О 7 ] 2− ). Этот анион имеет ту же топологию, что и тетрагидрокситетраборат-ион, но без гидроксильных групп, и все атомы бора имеют тригональную плоскую молекулярную геометрию. [3]
- Строение перборат-иона ( [В 2 О 4 (ОН) 4 ] 2− ). Этот анион представляет собой циклическую молекулу и имеет тетраэдрическую геометрию молекулы у атомов бора. Он содержит две мостиковые пероксидные группы ( -O-O- ) и четыре гидроксильные группы ( −OH ) присоединены к атомам бора, по два на каждый бор. Кольцо имеет форму стула . [4]
- Строение повторяющейся единицы октаборат-иона ( [Б 8 О 13 ] 2− ) в альфа-форме октабората динатрия (α- Na 2 [B 8 O 13 ] ). [5] Этот анион является циклическим и полимерным . Он имеет тетраэдрическую молекулярную геометрию у отрицательно заряженных атомов бора и тригональную плоскую молекулярную геометрию у нейтральных атомов бора.
Подготовка
[ редактировать ]В 1905 году Берджесс и Холт заметили, что плавление смесей оксида бора B 2 O 3 и карбонат натрия Na 2 CO 3 при охлаждении дал два кристаллических соединения определенного состава, соответствующего безводной буре. Na 2 B 4 O 7 (что можно записать Na 2 O·2B 2 O 3 ) и октаборат натрия Na 2 B 8 O 13 (что можно записать Na 2 O 4B 2 O 3 ). [6]
Структуры
[ редактировать ]Борат-анионы (и функциональные группы) состоят из тригональных плоских BO 3 и/или тетраэдрический Структурные единицы BO 4 , объединенные вместе через общие атомы кислорода (углы) или пары атомов (края) в более крупные кластеры, чтобы образовывать различные ионы, такие как [Б 2 О 5 ] 4− , [ B3O8 8] 7− , [Б 4 О 12 ] 12− , [В 5 О 6 (ОН) 5 ] 2− , [Б 6 О 13 ] 8− и т. д. Эти анионы могут иметь циклическую или линейную структуру и могут в дальнейшем полимеризоваться в бесконечные цепи, слои и трехмерные каркасы. [7] [8] Концевые (неразделенные) атомы кислорода в борат-анионах могут быть блокированы атомами водорода ( −OH ) или может нести отрицательный заряд ( −О − ).
Планарный Единицы BO 3 могут быть уложены в кристаллическую решетку так, чтобы иметь π-сопряженные молекулярные орбитали , что часто приводит к полезным оптическим свойствам, таким как генерация сильных гармоник , двойное лучепреломление и пропускание УФ-излучения . [8]
Полимерные борат-анионы могут иметь линейные цепи из 2, 3 или 4 тригональных BO 3 структурные единицы, каждая из которых имеет общие атомы кислорода с соседними единицами. [7] как в LiBO 2 , содержат цепочки тригональных БО 3 Структурные подразделения . Другие анионы содержат циклы; например, НаБО 2 и КБО 2 содержат циклический [ B3O6 6] 3− ион, [9] Состоит из шестичленного кольца, состоящего из чередующихся атомов бора и кислорода, с одним дополнительным атомом кислорода, присоединенным к каждому атому бора.
Тепловое расширение кристаллических боратов обусловлено тем фактом, что БО 3 и Многогранники БО 4 и состоящие из них жесткие группы практически не меняют свою конфигурацию и размеры при нагревании, но иногда вращаются шарнирно, что приводит к сильно анизотропному термическому расширению, в том числе к линейному отрицательному расширению. [10]
Реакции
[ редактировать ]Водный раствор
[ редактировать ]В водном растворе борная кислота B(OH) 3 может действовать как слабая кислота Бренстеда , то есть донор протона , с p K a ~ 9 . Однако чаще всего она действует как кислота Льюиса , принимая электронную пару от гидроксильного иона, воды образующегося в результате автопротолиза : [11]
Эта реакция очень быстрая, с характерным временем менее 10 мкс . [13] Полимерные оксоанионы бора образуются в водном растворе борной кислоты при pH 7–10, если концентрация бора превышает примерно 0,025 моль/л. Наиболее известным из них является тетраборат- ион. [Б 4 О 7 ] 2− , содержится в минеральной буре:
Другие анионы, наблюдаемые в растворе, представляют собой триборат (1-) и пентаборат (1-), находящиеся в равновесии с борной кислотой и тетрагидроксиборатом в соответствии со следующими общими реакциями: [13]
- 2 Б(ОН) 3 + [Б(ОН) 4 ] − ⇌ [В 3 О 3 (ОН) 4 ] − + 3 H 2 O (быстрый, р К = —1,92)
- 4 Б(ОН) 3 + [Б(ОН) 4 ] − ⇌ [В 5 О 6 (ОН) 4 ] − + 6 Н 2 О (медленно, р К = —2,05)
В диапазоне pH от 6,8 до 8,0 любые щелочные соли анионов «оксида бора» общей формулы [B x O y (OH) z ](( q − ) , где 3 x + q = 2 y + z в конечном итоге уравновесится в растворе до смеси В(ОН) 3 , [Б(ОН) 4 ] − , [В 3 О 3 (ОН) 4 ] − , и [В 5 О 6 (ОН) 4 ] − . [13]
Эти ионы, как и упомянутые выше комплексные бораты, более кислые, чем сама борная кислота. В результате pH концентрированного раствора полибората увеличится больше, чем ожидалось, при разбавлении водой.
Боратные соли
[ редактировать ]Известен ряд боратов металлов. Их можно получить обработкой борной кислоты или оксидов бора оксидами металлов. [ нужна ссылка ]
Смешанные анионные соли
[ редактировать ]Некоторые химические вещества помимо бората содержат еще один анион. К ним относятся хлориды боратов , карбонаты боратов , нитраты боратов , сульфаты боратов , фосфаты боратов .
Сложные оксианионы, содержащие бор
[ редактировать ]Более сложные анионы могут быть образованы путем конденсации боратных треугольников или тетраэдров с другими оксианионами с образованием таких материалов, как боросульфаты , бороселенаты , боротеллураты , бороантимонаты , борофосфаты или бороселениты .
Боросиликатное стекло , также известное как пирекс , можно рассматривать как силикат , в котором некоторое количество [SiO 4 ] 4− единицы заменены на [BO 4 ] 5− центры вместе с дополнительными катионами для компенсации разницы в валентных состояниях Si(IV) и B(III). Поскольку эта замена приводит к дефектам, материал медленно кристаллизуется и образует стекло с низким коэффициентом теплового расширения , поэтому устойчивое к растрескиванию при нагревании, в отличие от натриевого стекла .
Использование
[ редактировать ]
Обычные боратные соли включают метаборат натрия (NaBO 2 ) и буру. Бура растворима в воде, поэтому отложения полезных ископаемых встречаются только в местах с очень небольшим количеством осадков. Обширные залежи были найдены в Долине Смерти и отправлены с двадцатью упряжками мулов с 1883 по 1889 год. В 1925 году залежи были обнаружены в Бороне , Калифорния, на краю пустыни Мохаве . Пустыня Атакама в Чили также содержит полезные для добычи концентрации боратов.
Метаборат лития , тетраборат лития или смесь того и другого можно использовать при подготовке боратных сплавов различных образцов для анализа методами XRF , AAS , ICP-OES и ICP-MS . Боратный синтез и энергодисперсионная рентгенофлуоресцентная спектрометрия с поляризованным возбуждением использованы при анализе загрязненных почв. [14]
октабората динатрия Тетрагидрат Na 2 B 8 O 13 ·4H 2 O (обычно сокращенно DOT) используется в качестве консерванта для древесины или фунгицида. Борат цинка используется в качестве антипирена .
Некоторые бораты с большими анионами и несколькими катионами, например К 2 Al 2 B 2 O 7 и Cs 3 Zn 6 B 9 O 21 рассматривались для применения в нелинейной оптике . [8]
Боратные эфиры
[ редактировать ]Сложные эфиры борной кислоты представляют собой органические соединения , которые удобно получать реакцией стехиометрической конденсации борной кислоты со спиртами (или их халькогенными аналогами) . [15] ).
Тонкие пленки
[ редактировать ]Тонкие пленки боратов металлов выращивались различными методами, включая жидкофазную эпитаксию (например, FeBO 3 , [16] β-BaB 2 O 4 [17] ), электронно-лучевое испарение (например, CrBO 3 , [18] β-BaB 2 O 4 [19] ), импульсное лазерное осаждение (например, β-BaB 2 O 4 , [20] Я(БО 2 ) 3 [21] ) и атомно-слоевое осаждение (ALD). Рост с помощью ALD был достигнут с использованием предшественников, состоящих из трис(пиразолил)боратного лиганда и озона или воды в качестве окислителя для осаждения CaB 2 O 4 . [22] СрБ 2 О 4 , [23] БаБ 2 О 4 , [24] Мн 3 (БО 3 ) 2 , [25] и CoB 2 O 4 [25] фильмы.
Физиология
[ редактировать ]Борат-анионы в водном растворе при физиологическом pH находятся в основном в форме недиссоциированной кислоты. Никакого дальнейшего метаболизма не происходит ни у животных, ни у растений. У животных борная кислота/боратные соли практически полностью всасываются после перорального приема. Абсорбция происходит при вдыхании, однако количественные данные отсутствуют. Ограниченные данные показывают, что борная кислота/соли не всасываются в сколько-нибудь значительной степени через неповрежденную кожу, хотя абсорбция происходит через сильно поврежденную кожу. Распределяется по всему организму, не задерживается в тканях, кроме костной, и быстро выводится с мочой. [26]
См. также
[ редактировать ]- Наноканальные стеклянные материалы
- Пористое стекло
- Викор стекло
- Глупая шпатлевка
- Слизь (игрушка)
- Трис(2,2,2-трифторэтил)борат
Ссылки
[ редактировать ]- ^ «Основы физики и механизмы поглощения звука в морской воде» . Национальная физическая лаборатория . Проверено 21 апреля 2008 г.
- ^ Аллен, А.Х.; Танкард, Арканзас (1904 г.). «Определение борной кислоты в сидре, фруктах и т. д.» . Аналитик . 29 (октябрь): 301–304. Бибкод : 1904Ана....29..301А . дои : 10.1039/an9042900301 .
- ^ «Тетраборат» .
- ^ Каррондо, MAAF де Коннектикут; Скапский, AC (1978). «Уточнение рентгенокристаллической структуры промышленного отбеливателя динатрия тетрагидроксо-ди-μ-пероксо-дибората гексагидрата Na 2 [B 2 (O 2 ) 2 (OH) 4 ]·6H 2 O». Акта Кристаллогр Б. 34 : 3551. дои : 10.1107/S0567740878011565 .
- ^ Бубнова Р.С.; Шепелев, Ю. Ф.; Сеннова Н.А.; Филатов, СК (2002). «Термическое поведение жестких бор-кислородных групп в кристаллической структуре α-Na2B8O13» . Zeitschrift für Kristallographie - Кристаллические материалы . 217 (9): 444–450. Бибкод : 2002ZK....217..444B . дои : 10.1524/zkri.217.9.444.22881 . S2CID 95388918 .
- ^ Чарльз Хатченс Берджесс и Альфред Холт (1905): «Некоторые физические характеристики боратов натрия с новым и быстрым методом определения температур плавления». Труды Лондонского королевского общества, том 74, страницы 285–295. два : 10.1098/rspl.1904.0112
- ^ Jump up to: а б Виберг Э. и Холлеман А.Ф. (2001) Неорганическая химия , Elsevier. ISBN 0-12-352651-5
- ^ Jump up to: а б с Миридинг Мутайлипу, Мин Чжан, Сяоюй Донг, Янна Чен и Шили Пан (2016): «Эффекты ориентации [B 5 O 11 ] 7– Фундаментальные строительные блоки слоистых структур на основе пентаборатов». Неорганическая химия , том 55, выпуск 20, страницы 10608–10616. doi : 10.1021/acs.inorgch
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 205. ИСБН 978-0-08-037941-8 .
- ^ Римма С. Бубнова и Станислав К. Филатов (2008): «Сильное анизотропное тепловое расширение в боратах». Basic Solid State Physics , том 245, выпуск 11, страницы 2469-2476. дои : 10.1002/pssb.200880253
- ^ Аткинс; и др. (2010). Неорганическая химия (5-е изд.). Издательство Оксфордского университета. п. 334. ИСБН 9780199236176 .
- ^ Ингри, Н. (1962). «Равновесные исследования полианионов. 8. О первых равновесных стадиях гидролиза борной кислоты. Сравнение равновесий в 0,1 М и 3,0 М NaClO4» . Acta Chemica Scandinavica . 16 (2): 439–448. doi : 10.3891/acta.chem.scand.16-0439 . ISSN 0904-213X .
- ^ Jump up to: а б с Роберт К. Момии и Норман Х. Нактриб (1967): «Исследование ядерного магнитного резонанса борат-полиборатного равновесия в водном растворе». Неорганическая химия , том 6, выпуск 6, страницы 1189-1192. дои : 10.1021/ic50052a026
- ^ Хеттипатирана, Терренс Д. (2004). «Одновременное определение содержания Cr, As, Cd и Pb, а также основных элементов в миллионных долях в слабозагрязненных почвах с использованием боратного синтеза и энергодисперсионной рентгеновской флуоресцентной спектрометрии с поляризованным возбуждением». Spectrochimica Acta Часть B: Атомная спектроскопия . 59 (2): 223–229. Бибкод : 2004AcSpB..59..223H . дои : 10.1016/j.sab.2003.12.013 .
- ^ «Эфиры» . Сборник химической терминологии ИЮПАК . 2014. doi : 10.1351/goldbook.E02219 .
- ^ Ягупов С.; Стругацкий, М.; Селезнева К.; Могиленец Ю.; Милюкова Е.; Максимова Е.; Наухацкий И.; Дровосеков А.; Крейнес, Н. (ноябрь 2016 г.). «Пленки из бората железа: синтез и характеристика» (PDF) . Журнал магнетизма и магнитных материалов . 417 : 338–343. Бибкод : 2016JMMM..417..338Y . дои : 10.1016/j.jmmm.2016.05.098 .
- ^ Лю, Цзюньфан; Хэ, Сяомин; Чжоу, Гоцин; 2+ Подложки из альфа-бората бария, легированные методом жидкофазной эпитаксии». Thin Solid Films . 510 (1–2): 251–254. Bibcode : 2006TSF...510..251L . doi : 10.1016/j.tsf.2005.12.205 .
- ^ Джа, Менака; Кширсагар, Сачин Д.; Ганашьям Кришна, М.; Гангули, Ашок К. (июнь 2011 г.). «Рост и оптические свойства тонких пленок бората хрома». Науки о твердом теле . 13 (6): 1334–1338. Бибкод : 2011SSSci..13.1334J . doi : 10.1016/j.solidstatesciences.2011.04.002 .
- ^ Майя, LJQ; Фейтоса, САС; Де Висенте, ФС; Мастеларо, VR; Ли, М. Сиу; Эрнандес, AC (сентябрь 2004 г.). «Структурные и оптические характеристики тонких пленок бета-бората бария, выращенных электронно-лучевым испарением». Журнал вакуумной науки и технологий A: Вакуум, поверхности и пленки . 22 (5): 2163–2167. Бибкод : 2004JVSTA..22.2163M . дои : 10.1116/1.1778409 . ISSN 0734-2101 .
- ^ Сяо, Р.-Ф.; Нг, ЛК; Ага.; Вонг, ГКЛ (17 июля 1995 г.). «Получение тонких пленок кристаллического бета-бората бария (β-BaB 2 O 4 ) методом импульсного лазерного осаждения» . Письма по прикладной физике . 67 (3): 305–307. Бибкод : 1995ApPhL..67..305X . дои : 10.1063/1.115426 . ISSN 0003-6951 .
- ^ Александровский, А.С.; Крылов А.С.; Поцелуйко А.М.; Середкин В.А.; Зайцев А.И.; Замков, А.В. (09.02.2006). Конов, Виталий И.; Панченко Владислав Юрьевич; Сугиока, Кодзи; Вейко, Вадим П. (ред.). «Импульсное лазерное осаждение пленок европийборатного стекла и их оптические и магнитооптические свойства» . Серия конференций Общества инженеров фотооптического приборостроения (Spie) . Слушания SPIE. 6161 : 61610A–61610A–7. Бибкод : 2006SPIE.6161E..0AA . дои : 10.1117/12.675020 . S2CID 136530746 .
- ^ Сали, Марк Дж.; Мунник, Франс; Винтер, Чарльз Х. (2010). «Атомно-слоевое осаждение пленок CaB2O4 с использованием бис(трис(пиразолил)бората)кальция в качестве высокотермостабильного источника бора и кальция». Журнал химии материалов . 20 (44): 9995. doi : 10.1039/c0jm02280b . ISSN 0959-9428 .
- ^ Сали, Марк Дж.; Мунник, Франс; Винтер, Чарльз Х. (июнь 2011 г.). «Атомно-слоевое осаждение пленок SrB 2 O 4 с использованием термостабильного предшественника бис (трис (пиразолил) бората) стронция». Химическое осаждение из паровой фазы . 17 (4–6): 128–134. дои : 10.1002/cvde.201006890 .
- ^ Сали, Марк Дж.; Мунник, Франс; Бэрд, Рональд Дж.; Винтер, Чарльз Х. (25 августа 2009 г.). «Выращивание тонких пленок BaB 2 O 4 методом атомно-слоевого осаждения из исключительно термически стабильного предшественника на основе трис(пиразолил)бората». Химия материалов . 21 (16): 3742–3744. дои : 10.1021/cm902030d . ISSN 0897-4756 . S2CID 93114230 .
- ^ Jump up to: а б Клеско, Джозеф П.; Беллоу, Джеймс А.; Сали, Марк Дж.; Винтер, Чарльз Х.; Юлин, Яакко; Саджаваара, Тимо (сентябрь 2016 г.). «Необычный контроль стехиометрии при атомно-слоевом осаждении пленок бората марганца из бис(трис(пиразолил)бората) марганца и озона» . Журнал вакуумной науки и технологий A: Вакуум, поверхности и пленки . 34 (5): 051515. Бибкод : 2016JVSTA..34e1515K . дои : 10.1116/1.4961385 . ISSN 0734-2101 .
- ^ Агентство по охране окружающей среды США (2005), «Борная кислота/соли бората натрия». Глава HED Документа о принятии решения о приемлемости повторной оценки толерантности (TRED), EPA-HQ-OPP-2005-0062-0004, стр. 11 (январь 2006 г.). По данным PubChem.