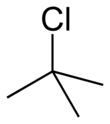
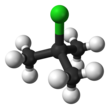
трет -Бутилхлорид
| |||

| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
2-хлор-2-метилпропан | |||
| Другие имена
1,1-диметилэтилхлорид
1-хлор-1,1-диметилэтан хлортриметилметан триметилхлорметан т -бутилхлорид | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.007.334 | ||
| Номер ЕС |
| ||
ПабХим CID
|
|||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1127 | ||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 4 Н 9 Cl | |||
| Молярная масса | 92.57 g/mol | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 0,851 г/мл | ||
| Температура плавления | -26 ° C (-15 ° F; 247 К) | ||
| Точка кипения | 51 ° С (124 ° F; 324 К) | ||
| Умеренно растворим в воде, смешивается со спиртом и эфиром. | |||
| Давление пара | 34,9 кПа (20 °С) | ||
| Опасности | |||
| СГС Маркировка : | |||

| |||
| Опасность | |||
| H225 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P280 , P303+P361+P353 , P370+P378 , P403+P235 , P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | −9 ° C (16 ° F; 264 К) (открытая чашка) −23 °C (закрытый тигель) | ||
| 540 ° C (1004 ° F; 813 К) | |||
| Родственные соединения | |||
Родственные алкилгалогениды
|
трет-Бутилбромид | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
трет -Бутилхлорид представляет собой хлорорганический соединения формулы (СН 3 ) 3 CCl . Это бесцветная, легковоспламеняющаяся жидкость. Он умеренно растворим в воде , имеет тенденцию подвергаться гидролизу до соответствующего трет -бутилового спирта. Его производят в промышленности как предшественник других органических соединений. [ 1 ]
Синтез
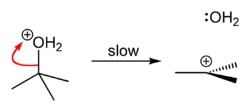
[ редактировать ]Трет -Бутилхлорид получают реакцией трет- бутилового спирта с хлористым водородом . [ 1 ] В лаборатории концентрированную соляную кислоту используют . Превращение влечет за собой реакцию S N 1, как показано ниже. [ 2 ]
| Шаг 1 | Шаг 2 | Шаг 3 |
 |
 |

|
| Кислота протонирует спирт, образуя хорошую уходящую группу (воду). | Вода покидает протонированный t -BuOH, образуя относительно стабильный третичный карбокатион . | Ион хлорида атакует карбокатион, образуя t -BuCl. |
Таким образом, общая реакция такова:
- (CH 3 ) 3 COH + HCl → (CH 3 ) 3 CCl + H 2 O
Поскольку трет -бутанол является третичным спиртом, относительная стабильность трет -бутилкарбокатиона на стадии 2 позволяет S N 1 следовать механизму , тогда как первичный спирт будет следовать механизму S N 2 .
Реакции
[ редактировать ]Когда трет -бутилхлорид растворяется в воде, он подвергается гидролизу до трет -бутилового спирта . При растворении в спиртах образуются соответствующие трет-бутиловые эфиры.
Использование
[ редактировать ]Трет -Бутилхлорид используется для получения антиоксиданта трет- бутилфенола и ароматизатора неогексилхлорида. [ 1 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с М. Россберг и др. «Хлорированные углеводороды» в Энциклопедии промышленной химии Ульмана, 2006 г., Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a06_233.pub2
- ^ Джеймс Ф. Норрис и Алансон В. Олмстед « трет -Бутилхлорид» Org. Синтез. 1928, том 8, стр. 50. дои : 10.15227/orgsyn.008.0050