4,7-дихлорхинолин

| |
| Имена | |
|---|---|
| Предпочтительное имя IUPAC
4,7-дихлорхинолин | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Химический | |
| Chemspider | |
| Echa Infocard | 100.001.559 |
| ЕС номер |
|
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 9 H 5 Cl 2 N | |
| Молярная масса | 198.05 g·mol −1 |
| Появление | Белый порошок |
| Точка плавления | 87 ° C (189 ° F; 360 K) |
| Точка кипения | 317 ° C (603 ° F; 590 К) |
| Опасности | |
| GHS Маркировка : [ 1 ] | |
 
| |
| Предупреждение | |
| H315 , H317 , H319 , H335 , H411 | |
| P261 , p264 , p271 , p272 , p273 , p280 , p302+p352 , p304+p340 , p35+p351+p32 , p312 , p321 , p332+p313 , p333+p313 , p37+p313 , p362 , p363 , p391 , p403+ P233 , P405 , P501 | |
| точка возгорания | 164 ° C (327 ° F; 437 K) |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
4,7-дихлорхинолин с двумя кольцами, представляет собой гетероциклическое соединение используемое в качестве химического промежуточного или аминокинолина противомалярийного препарата, включая амодиахин , хлорохин и гидроксихлорохин .
Синтез
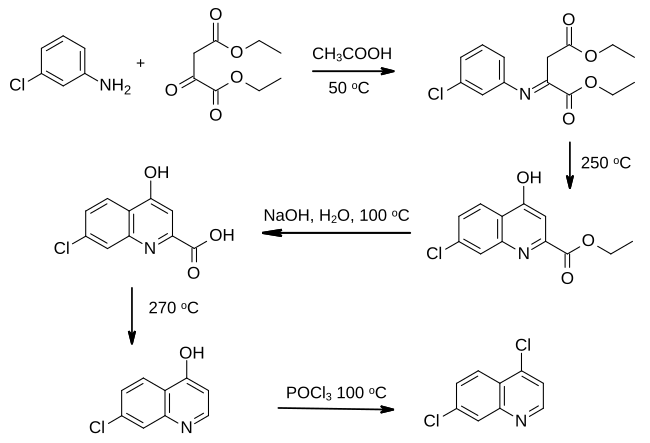
[ редактировать ]4,7-дихлорхинолин впервые сообщили в патенте, поданном IG Farben в 1937 году. [ 2 ] Тем не менее, его синтез не был подробно исследован до тех пор, пока хлорохин не был разработан в качестве противомалярийного препарата. [ 3 ] : 130–132 разработали маршрут к промежуточному, начиная с 3-хлораанилина Химики из Winthrop Chemical Co . [ 4 ]
Замесченный анилин конденсируется диэтиловым эфиром в оксалоуксусной кислоты мягко кислотных условиях, образуя имин , который велосирует для образования пиридинового кольца путем нагрева в минеральном масле. Гидролиз и декарбоксилирование следует, до того, как гидрокси группа в 4-позиции преобразуется во вторую группу хлор с использованием фосфорилхлорида . [ 4 ]
Доступность 4,7-дихлорохинолина позволила альтернативные структурные аналоги 4 -аминохинолина , что приводит к открытию гидроксихлорохина в 1949 году. исследовать [ 5 ] [ 6 ] К тому времени были созданы производственные процессы хлорохина, чтобы обеспечить его широкое использование. [ 7 ] 4,7-дихлорхинолин также был получен реакцией Гулд-Джакоба с использованием альтернативного метода построения пиридинового кольца из 3-хлораанилина. [ 8 ]
Реакция
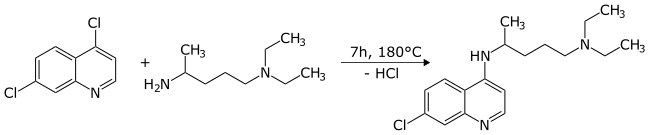
[ редактировать ]Атом хлора в 4-позиции в пиридиновом кольце является гораздо более реактивным в ароматической замещения нуклеофильных реакциях [ 9 ] Чем хлор в бензольном кольце. В результате его можно заменить избирательно для формирования производных в этой позиции. Типичная реакция с специфическим первичным амином дает хлорохин с высоким выходом: [ 6 ] [ 7 ]
Использование
[ редактировать ]Помимо его использования при производстве уже описанных противомалярийных, 4,7-дихлорохинолин представляют постоянный интерес в качестве промежуточного для новых кандидатов на лекарства. [ 10 ] [ 11 ]
Ссылки
[ редактировать ]- ^ База данных PUBCHEM. «4,7-дихлорохинолин» .
- ^ De Patent 683692 , Andersag, Hans; Breitner, Stefan & Jung, Heinrich, «процесс подготовки соединений хинолина, содержащих аминогруппы с основными заместителями в 4-позиции», выпущенный 1939-11-13, назначенный IG Farbenindustrie AG
- ^ Институт медицины (США) Комитет по экономике противомалярийных препаратов; Стрелка, KJ; Panosian, C.; Гелбанд, Х. (2004). Стрелка, KJ; Panosian, CB; Гельбан, Х. (ред.). Экономия жизни, покупка времени: экономика наркотиков малярии в эпоху сопротивления . Национальная академическая пресса. doi : 10.17226/11017 . ISBN 9780309092180 Полем PMID 25009879 .
- ^ Подпрыгнуть до: а беременный Суррей, Александр Р.; Хаммер, Генри Ф. (1946). «Некоторые 7-замещенные 4-аминохинолиновые производные». Журнал Американского химического общества . 68 : 113–116. doi : 10.1021/ja01205a036 . PMID 21008327 .
- ^ Патент США 2546658 , Суррей, Александр Р., «7-хлор-4- [5- (N-этил-N-2-гидроксиэтиламино) -2-пентиль] аминохинолин, его кислотный добавление и метод препарата», выпущен 1951 г. -03-27, назначенный в Sterling Drug Inc.
- ^ Подпрыгнуть до: а беременный Суррей, Александр Р.; Хаммер, Генри Ф. (1950). «Приготовление 7-хлор-4- (4- (N-этил-N-β-гидроксиэтиламино) -1-метилбутиламино) -quinoline и родственные соединения». Журнал Американского химического общества . 72 (4): 1814–1815. doi : 10.1021/ja01160a116 .
- ^ Подпрыгнуть до: а беременный Кеньон, RL; Виснер, JA; Kwartler, CE (1949-04-01). «Производство хлорохина». Промышленная и инженерная химия . 41 (4): 654–662. doi : 10.1021/IE50472A002 .
- ^ Прайс, Чарльз С .; Робертс, Ройстон М. (1948). «4,7-дихлорохинолин (хинолин, 4,7-дихлор)» . Органические синтезы . 28 : 38. doi : 10.15227/orgsyn.028.0038 ; Собранные объемы , вып. 3, с. 272
- ^ Рорбах, Саймон; Смит, Эндрю Дж.; Панг, Цзя Хао; Пул, Даррен Л.; Таттл, скажи; Чиба, Шунсуке; Мерфи, Джон А. (2019). «Согласованные нуклеофильные реакции ароматической замещения» . Angewandte Chemie International Edition . 58 (46): 16368–16388. doi : 10.1002/anie.201902216 . PMC 6899550 . PMID 30990931 .
- ^ Радж, Рагху; Земля, Кирквуд М.; Кумар, Випан (2015). «4-аминохинолин-гибридизация на пути к развитию рационально спроектированных противомалярийных агентов» . RSC Advances . 5 (101): 82676–82698. Bibcode : 2015rscad ... 582676R . doi : 10.1039/c5ra16361g .
- ^ Janeba, Zlatko (2015). «Разработка мелкомолекулярных антивирусных препаратов для Эболы» . Обзоры лекарственных исследований . 35 (6): 1182. DOI : 10.1002/Med.21355 . PMC 7168439 . PMID 26172225 .
Дальнейшее чтение
[ редактировать ]- Слейтер, Лео (9 января 2009 г.). Война и болезнь: биомедицинские исследования малярии в двадцатом веке . Рутгерс Университет Пресс. ISBN 9780813546469 .