ТЕРТ -Бутансульфинамид
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC
2-метилпропан-2-сульфинамид | |||
| Идентификаторы | |||
| |||
3D model ( JSmol )
|
| ||
| Echa Infocard | 100.108.188 | ||
PubChem CID
|
|||
| НЕКОТОРЫЙ |
| ||
Comptox Dashboard ( EPA )
|
|||
| Характеристики | |||
| (Ch 3 ) 3 CS (O) NH 2 | |||
| Молярная масса | 121.20 g/mol | ||
| Появление | белый и не совсем белый кристаллический твердый | ||
| Точка плавления | От 102 до 105 ° C (от 216 до 221 ° F; от 375 до 378 К) | ||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Терт -бутансульфинамид (также известный как 2-метил-2-пропанесульфинамид или сульфинамид Эллмана ) является органосульфурным соединением и членом класса сульфинамидов . Обе энантиомерные формы являются коммерчески доступными и используются в асимметричном синтезе в качестве хиральных вспомогательных услуг , часто в качестве хиральных эквивалентов аммиака для синтеза аминов . [ 1 ] [ 2 ] [ 3 ] Терт -бутансульфинамид и связанная с ними синтетическая методология были введены в 1997 году Джонатаном А. Эллманом и соавт . [ 4 ]
Синтез энантиопов
[ редактировать ]Энантиоптура Терт -Бутансульфинамид может быть приготовлен путем энантиоселективного окисления недорогого дивертилового дисульфида до тиосульфината с последующим расщеплением дисульфидной связи амидом лития . В исходной области хиральный лиганд , используемый вместе с ванадилацетилацетонатом, получали путем конденсации оптически чистого хирального аминоинданола с 3,5-динерным - трет -бутилолицилальдегидом .
 |
| ТЕРТ -Бутансульфинамид Синтез |
|---|
Энантиоселективный синтез амина
[ редактировать ]Конденсация кетонами и альдегидами дает соответствующие N - трет -бутансульфинил альдимины и ктимины . Эти промежуточные продукты более устойчивы к гидролизу, чем другие имины , но более реагирующие на нуклеофилы . Нуклеофил добавляет диастереоселективно по группе имине в электрофильном добавлении с трет -бутансульфинильной группой, действующей в качестве хирального вспомогательного. Эта трет -бутансульфинильная группа также является защитной группой . При добавлении соляной кислоты соль . удаляется трет -бутансульфинильная группа, образуя хиральную первичную аммония или амин (из предшественника альдегида) или хирального вторичного амина (предшественник кетона)
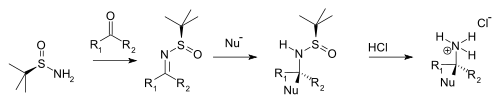 |
| ТЕРТ -Бутансульфинамид Хирал Амина Синтез амина |
|---|
Типичными нуклеофилами являются реагенты Grignard , органические соединения , органические соединения и энолаты .
Хиральные сульфинимины в качестве промежуточных соединений для асимметричного синтеза аминов также были разработаны Франклином А. Дэвисом . [ 5 ]
Приложения
[ редактировать ]Терт -бутансульфинамид использовался в качестве вспомогательного в асимметричном синтезе цетиризина (более сильной, чем раковая смесь препарата), начиная с п -глорбензальдегида и бромида фенилмагности . [ 6 ]
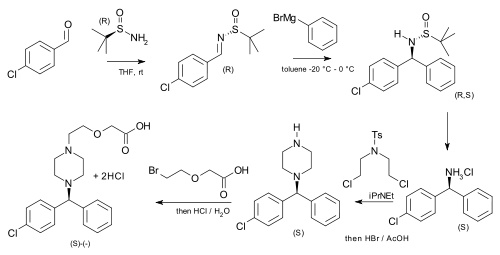 |
| Асимметричный синтез Цетиризина |
|---|
Ссылки
[ редактировать ]- ^ Эллман, JA (2003). «Применение трет-бутансульфинамида в асимметричном синтезе аминов» . Чистая и прикладная химия . 75 : 39–46. doi : 10.1351/pac200375010039 . S2CID 97201636 .
- ^ Робак, Мэринн Т.; Геред, Мелисса А.; Эллман, Джонатан А. (2010). «Синтез и применение тетрального бутансульфинамида». Химические обзоры . 110 (6): 3600–740. doi : 10.1021/cr900382t . PMID 20420386 .
- ^ Органические синтезы, вып. 82, с.157 (2005). Связь
- ^ Лю, Гуанчэн; Коган, Дерек А.; Эллман, Джонатан А. (1997). «Каталитический асимметричный синтез терра-бутансульфинамида. Применение к асимметричному синтезу аминов». Журнал Американского химического общества . 119 (41): 9913. DOI : 10.1021/ja972012Z .
- ^ Дэвис, Франклин А.; Редди, Раджаратнам Э.; Szewczyk, Joanna M.; Редди, Г. Венкат; Portonovo, Padma S.; Чжан, Хуиминг; Фанелли, Дин; Чжоу, Пинг; и др. (1997). «Асимметричный синтез и свойства сульфиниминов (тиооксиммы-оксидов)». Журнал органической химии . 62 (8): 2555–2563. doi : 10.1021/jo970077e . PMID 11671597 .
- ^ Pflum, d; Кришнамурти, D; Хан, Z; Wald, S; Senanayake, C (2002). «Асимметричный синтез цитиризина дигидрохлорида». Тетраэдр буквы . 43 (6): 923. doi : 10.1016/s0040-4039 (01) 02294-8 .

