Монофторфосфат
| |
 | |
| Имена | |
|---|---|
| Название ИЮПАК
Фтор-диоксидо-оксо- λ 5 -фосфан
| |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| ПО 3 Ф 2− | |
| Молярная масса | 97.971 g/mol |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
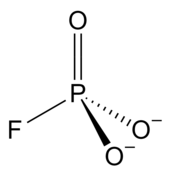
Монофторфосфат представляет собой анион формулы ПО 3 Ф 2− , который представляет собой фосфатную группу с одним атомом кислорода, замещенным атомом фторида. Заряд иона равен −2. Ион напоминает сульфат по размеру, форме и заряду и, таким образом, может образовывать соединения той же структуры, что и сульфаты. К ним относятся соли Туттона и лангбейниты . Наиболее известным соединением монофторфосфата является монофторфосфат натрия , обычно используемый в зубной пасте.
Родственные ионы включают дифторфосфат ( PO 2 F - 2 ) и гексафторфосфат ( [ПФ 6 ] − ). [ 1 ] Родственная нейтральная молекула - фторид фосфена. ПО 2 Ф .
Органические производные могут быть высокотоксичными и включают диизопропилфторфосфат . Некоторые из препаратов «Новичок» представляют собой сложные эфиры монофторфосфата. Имена им даются путем названия групп, присоединенных к сложным эфирам, с последующим добавлением «фторфосфоната» в конце названия. Могут быть присоединены две органические группы. Другие родственные вещества нервно-паралитического газа могут не быть сложными эфирами, а вместо этого иметь связи углерод-фосфор или азот-фосфор. Органические фторфосфонаты необратимо реагируют с серинэстеразами и серинпротеазами . Это препятствует функционированию этих ферментов. Таким важным ферментом является ацетилхолинэстераза , обнаруженная у большинства животных. [ 2 ] Некоторые из органических эфиров детоксифицируются у млекопитающих с помощью фермента крови и печени, называемого параоксоназа PON1 . [ 3 ]
Вилли Ланге из Берлина открыл монофторфосфат натрия в 1929 году. Он безуспешно пытался получить монофторфосфорную кислоту. Однако он обнаружил высокотоксичные органические эфиры. После этого открытия были разработаны различные нервно-паралитические газы, такие как зарин .
Фторфосфатные стекла — это виды стекла с низкой температурой плавления, которые представляют собой смеси соединений фторидов и фосфатов металлов. Например, состав 10% SnO , 40% СнФ 2 , 50% P 2 O 5 образует стекло с температурой плавления около 139°С. PbO и PbF 2 может снизить температуру плавления и повысить водостойкость. [ 4 ] Эти стекла также можно окрашивать различными другими элементами и органическими красителями.
некоторые смешанные анионные соединения Известны с другими анионами, такими как фторид , хлорид, дифторфосфат или тетрафторборат .
Производство
[ редактировать ]Гидролиз дифторфосфата щелочью дает монофторфосфат.
- ПО 2 F − 2 + 2 МОН → М 2 ПО 3 F + H 2 O + F −
Промышленное производство осуществляется путем реакции фторида с метафосфатом .
- МФ + МПО 3 → М 2 ПО 3 Ф
Динатрийгидрофосфат или тетранатрийпирофосфат могут реагировать с фтористым водородом с образованием натриевой соли.
- Na 2 HPO 4 или Na 4 P 2 O 7
Фосфорная кислота реагирует с фторидами металлов, растворенными в расплавленной мочевине, с образованием монофторфосфатов. [ 5 ]
Характеристики
[ редактировать ]Монофторфосфаты стабильны при комнатной температуре, но разлагаются при нагревании. Например, при 450 К (177 °С) монофторфосфат серебра выделяет фторид фосфорила ( POF 3 ) в виде газа, оставляющего после себя фосфат серебра ( Ag 3 PO 4 ) и пирофосфат серебра ( Ag 4 P 2 O 7 ). [ 6 ]
В неорганических соединениях ион монофторфосфата имеет среднюю длину связи P–O 1,51 Å. Связь P–F длиннее, в среднем 1,58 Å. Угол OP F составляет 104,8°, что меньше тетраэдрического 109,47°. Для компенсации валентный угол O P O в среднем составляет 113,7°. [ 7 ]
Чаще всего ион монофторфосфата относится к точечной группе 1, но значительное количество имеет точечную группу m . Известны только два с 3 м и один с 3. [ 7 ]
По сравнению с сульфатами некоторые из них изотипичны монофторфосфатам. У других есть сульфаты, которые принимают другую форму. Но большинство известных монофторфосфатов не имеют известного эквивалента сульфата. [ 7 ]
Соединения
[ редактировать ]| Имя | Формула | Кристаллическая форма | Формула веса | Плотность | Комментарий | ХимическийПаук | ПабХим | КАС |
|---|---|---|---|---|---|---|---|---|
| фторфосфорная кислота | H2POH2PO3F F | 99.986 | 22687 | 24267 | 13537-32-1 | |||
| [ 8 ] | БеПО 3 Ф-И | Pc a=4,9331 b=6,6283 c=4,7083 β= 90,2007 Z=2 | запрещенная зона 8,03 эВ, ГВГ 1,72×KDP | |||||
| [ 8 ] | БеПО 3 Ф-II | Р 6 3 а=4,9651 с=9,3236 Z=2 | ||||||
| [ 8 ] | БеПО 3 Ф-III | Cc a=4,9542 b=8,5812 c=10,0532 β=98,0674 Z=4 | ||||||
| [ 8 ] | БеПО 3 Ф-IV | Cc a=8,5892 b=4,9532 c=10,1526 β=92,4967 Z=4 | ||||||
| [ 8 ] | BePO 3 F-V | См a=9,2837 b=5,1602 c=7,1809 β=143,9321 Z=2 | ||||||
| [ 8 ] | БеПО 3 Ф-VI | P 6 3 mc а=5,1519 с=8,8598 Z=2 | ||||||
| монофторфосфат аммония [ 9 ] | (NH 4 ) 2 PO 3 F | ромбический: a = 6,29 Å, b = 8,31 Å, c = 12,70 Å, β = 99,6°, Z = 4 [ 10 ] | 134.05 | 1.633 | 8324505 | |||
| гидрат монофторфосфата аммония [ 11 ] | (NH 4 ) 2 PO 3 F·H 2 O | моноклинная: а = 7,9481 Å, b = 11,3472 Å, c = 6,0425 Å, β = 117,55°, Z = 4 моноклинная: a = 6,3042 Å, b = 8,2942 Å, c = 12,760 Å, β = 98,415°, Z = 4, V = 657,416 Å 3 [ 12 ] |
152.05 | 1.536 | ||||
| тетрафторборат-монофторфосфат аммония [ 13 ] | (NH 4 ) 3 [PO 3 F][BF 4 ] | моноклинный P 2 1 / m : a = 7,8384 Å, b = 6,0996 Å, c = 9,9079 Å, β = 111,990°, V = 439,24 Å 3 , Z = 2 | 238.91 | 1.806 | ||||
| [ 14 ] | (NH 4 ) 2 PO 3 F·NH 4 NO 3 | моноклинная P2 1 /na=10,3145 b=6,1034 c=14,3299 β= 103,885° Z=4 | 875.8 | 1.624 | @−73 | |||
| [ 14 ] | (NH 4 ) 2 PO 3 F·NH 4 NO 3 | триклинный P 1a=10,3414 b=6,1056 c=14,1704 α=91,248 β=101,016 γ=89,173 Z=4 | 877.98 | 1.620 | @−98 | |||
| [ 14 ] | (NH 4 ) 2 PO 3 F·NH 4 NO 3 | моноклинный P 2 1 ppa=10,3182 b=6,0591 c=14,3715 β=98,563 Z=4 | 888.48 | 1.601 | @−173 | |||
| [ 15 ] | (N 2 H 6 )[HPO 3 F] 2 | моноклинный C12/c1 a=14,1326 b=7,0340 c=7,9877 β =96,763 Z=4 | 788.52 | 1.954 | бесцветный; большое двойное лучепреломление | |||
| монофторфосфат натрия | Na2PONa2PO3F F | 22686 | 24266 | 10163-15-2 | ||||
| гидромонофторфосфат натрия | NaHPONaHPO3F F | 121.968 | 19860808 | 20859-36-3 | ||||
| дигидрат гидромонофторфосфата натрия [ 16 ] | NaHPO 3 F 2H 2 O | моноклинная: a = 19,112 Å, b = 5,341 Å, c = 12,72 Å, α = 110,18°, V = 1219,4 Å 3 | 167.01 | 1.819 | ||||
| монофторфосфат магния | МгПО 3 Ф | 122.28 | 23206079 | |||||
| дигидрат димонофторфосфата диаммония и марганца [ 7 ] | (NH 4 ) 2 Mg(PO 3 F) 2 ·2H 2 O | моноклинный C 2/ m : a = 13,374 Å, b = 5,3541 Å, c = 7,385 Å, β = 113,758°, V = 484,01 Å 3 , Z = 2 | 292.37 | 2.006 | ||||
| монофторфосфат калия [ 9 ] | K2POК2ПО3Ф F | ромбический: a = 7,554 Å, b = 5,954 Å, c = 10,171 Å, V = 457 Å 3 , Z = 4 (при 20 °С) [ 17 ] | 176.17 | 2.57 | 20859-37-4 14306-73-1 | |||
| К 2 ПО 3 Ф·КФ [ 18 ] | ||||||||
| Монофторфосфат калия гидрогенизированный | KHPOХПО3Ф F | моноклинная: a = 7,273 Å, b = 14,086 Å, c = 7,655 Å, β = 90,13°, Z = 8, V = 784,233 Å 3 [ 19 ] | ||||||
| Трикалий гидромонофторфосфат | К 3 Н(РО 3 F) 2 | моноклинная: а = 7,973 Å; б = 11,635 Å; c = 9,668 Å, β = 113,52°, Z = 4, V = 822,35 Å 3 [ 19 ] | ||||||
| Гидродифторфосфат аммония дикалия [ 20 ] | NH 4 K 2 H(PO 3 F) 2 | |||||||
| дигидрат монофторфосфата кальция [ 21 ] | СаРО 3 F·2H 2 O | триклинная: а = 8,6497 Å, b = 6,4614 Å, c = 5,7353 Å, α = 119,003°, β = 110,853°, γ = 94,146°, V = 249,943 Å 3 , Z = 2 [ 12 ] | 2.313 | 8096036 | 9920401 | 37809-19-1 | ||
| полугидрат монофторфосфата кальция [ 21 ] | СаРО 3 F·0,5H 2 O | |||||||
| монофторфосфат ванадия | ВПО 3 Ф | 148.91 | 20452625 | |||||
| монофторфосфат хрома(III) [ 7 ] | Cr 2 (PO 3 F) 3 ·18,8H 2 O | триклинная: а = 11,594 Å, b = 15,292 Å, c = 15,360 Å, α = 83,804°, β = 84,203, γ = 82,597, V = 2674,1 Å 3 , Z = 4 | 736.88 | 1.830 | ||||
| гексагидрат дифторфосфата аммония хрома(III) [ 7 ] | NH 4 Cr(PO 3 F) 2 ·6H 2 O | R 3 м : а = 6,5491 Å, c = 25,438 Å, Z = 3 | 9.4489 | 1.972 | зеленый | |||
| дигидрат фторфосфата марганца(II) | MnPO 3 F 2H 2 O | триклинная: а = 5,528 Å, b = 5,636 Å, c = 8,257 Å, α = 81,279°, β = 75,156°, γ = 71,722°, Z = 2 [ 22 ] | 188.94 | |||||
| монофторфосфат диаммония и марганца [ 7 ] | (NH 4 ) 2 Mn(PO 3 F) 2 ·2H 2 O | моноклинная: P 2 1 / n a = 12,558 Å, b = 5,5456 Å, c = 7,422 Å, β = 99,918°, Z = 2 | 500.9 | 2.142 | розовый | |||
| дифторфосфат дифторфосфат аммония тримарганец дифторид [ 23 ] | (NH 4 )Mn 3 (PO 3 F) 2 (PO 2 F 2 )F 2 | моноклинная: а = 20,3151 Å, b = 7,6382 Å, c = 7,8312 Å, β = 103,589°, V = 1181,16 Å 3 | 517.8 | 2.9116 | ||||
| дигидрат димонофторфосфата диаммония-кобальта [ 7 ] | (NH 4 ) 2 Co(PO 3 F) 2 ·2H 2 O | моноклинный C 2/ m : a = 13,386 Å, b = 5,3476 Å, c = 7,390 Å, β = 114,02°, V = 483,2 Å 3 , Z = 2 | 326.99 | 2.247 | ||||
| дифторфосфат дифторид трикобальта аммония [ 23 ] | (NH 4 )Co 3 (PO 3 F) 2 (PO 2 F 2 )F 2 | моноклиническая: а = 19,9678 Å, b = 7,4883 Å, c = 7,5679 Å, β = 102,676°, V = 1104,01 Å 3 | 529.7 | 3.1871 | ||||
| Гексагидрат димонофторфосфата диаммония-никеля [ 7 ] | (NH 4 ) 2 Ni(PO 3 F) 2 ·6H 2 O | моноклинная: а = 6,2700 Å, b = 12,2845 Å, c = 9,1894 Å, β = 106,033°, Z = 2 | 680.27 | 1.947 | синий туттон | |||
| монофторфосфат меди [ 24 ] | CuPO 3 F·5H 2 O | 251.59 | ||||||
| основной монофторфосфат меди и калия [ 24 ] | Cu 2 K(OH)(PO 3 F) 2 ·5H 2 O | моноклинная: а = 9,094 Å, b = 6,333 Å, c = 7,75 Å, β = 117,55°, Z = 2 | натрохальцит | |||||
| диаммоний диаквабис (монофторфосфат) медь [ 25 ] | Cu(NH 4 ) 2 (PO 3 F) 2 ·2H 2 O | моноклинная: а = 13,454 Å, b = 5,243 Å, c = 7,518 Å, β = 114,59°, V = 482,2 Å 3 , Z = 2 | 331.6 | 2.28 | ||||
| основной димонофторфосфат тетрааммония димеди [ 7 ] | NH 4 Cu 2 OH(PO 3 F) 2 ·H 2 O | C 2/ m : a = 9,1012 Å, b = 6,4121 Å, c = 7,8506 Å, β = 116,277°, Z = 2 | 410.80 | 3.040 | светло-голубой натрохальцит | |||
| монофторфосфат цинка [ 26 ] [ 7 ] | ZnPO 3 F·2,5H 2 O | триклинная: а = 7,6020 Å, b = 7,6490 Å, c = 9,4671 Å, α = 88,633°, β = 88,888°, γ = 87,182°, V = 549,58 Å 3 , Z = 4 | 163.35 | 2.518 | 20846323 | 68705-59-9 | ||
| безводный тетрамонофторфосфат цинка диаммония [ 7 ] | ( NH4 ) 2Zn3 3 ( PO3F ) 4 | кубический: а = 11,4769 Å | ||||||
| димонофторфосфат диаммония и цинка [ 7 ] | (NH 4 ) 2 Zn(PO 3 F) 2 0,2H 2 O | моноклинный C 2/ c : a = 18,936 Å, b = 7,6955 Å, c = 20,528 Å, β = 108,641° Z = 12 | 2834.4 | 2.117 | бесцветный | |||
| тетрамонофторфосфат диаммония трицинка [ 7 ] | (NH 4 ) 2 Zn 3 (PO 3 F) 4 H 2 O | кубический I 4 3 d : a = 11,3693 Å, Z = 4 | 1469.6 | 2.902 | бесцветный | |||
| монофторфосфат рубидия [ 27 ] | Rb2POРб2ПО3Ф F | орторомбический: [ 28 ] а = 7,8714 Å, b = 6,1236 Å, c = 10,5424 Å, V = 508,15 Å 3 , Z = 4 (при 17 °С) | 268.9 | 3.514 | ||||
| Гидромонофторфосфат рубидия | RbHPO 3 F | моноклинная: a = 7,465 Å, b = 15,551 Å, c = 7,563 Å, β = 105,38°, V = 846,533 Å 3 , Z = 8 [ 19 ] | ||||||
| [ 29 ] | Na 1,5 Rb 0,5 PO 3 F·H 2 O | ромбический Pmn 2 1 : a = 6,015 Å, b = 8,965 Å, c = 4,9689 Å, Z = 2 | 267.97 | 2.398 | бесцветный | |||
| монофторфосфат стронция | СРПО 3 Ф | моноклинический [ 30 ] | 185.59 | 18183579 | ||||
| гидрат монофторфосфата стронция [ 31 ] | SrPO 3 F·H 2 O | 185.59 | ||||||
| монофторфосфат серебра [ 24 ] | Ag2POAg2PO3F F | моноклинная: а = 9,245 Å, b = 5,585 Å, c = 14,784 Å, β = 90,178°, Z = 8 [ 6 ] | 313.7 | 44135907 | ||||
| трисеребряный монофторфосфат аммония | NH 4 Ag 3 (PO 3 F) 2 | моноклинная: а = 30,895 Å, b = 5,5976 Å, c = 9,7522 Å, β = 90,027°, V = 1686,6 Å 3 , Z = 8 [ 32 ] | 537.59 | 4.234 | ||||
| монофторфосфат кадмия [ 7 ] | CdPO 3 F·2H 2 O | триклинный P 1_: а = 5,2678 Å, b = 6,6697 Å, c = 7,7037 Å, α = 65,506°, β = 85,919°, γ = 75,394°, V = 238,584 Å 3 , Z = 2 | 246.40 | 3.430 | ||||
| дигидрат хлорида монофторфосфата кадмия и аммония [ 33 ] | Cd 2,5 (NH 4 ) 2 (PO 3 F) 3 Cl·2H 2 O | бесцветный | ||||||
| монофторфосфат олова | SnPO 3 F·2,5H 2 O | моноклинический | 216.68 | 44717639 | 52262-58-5 | |||
| монофторфосфат цезия | Cs 2 PO 3 F [ 27 ] | ромбический: a = 8,308 Å, b = 6,3812 Å, c = 11,036 Å, V = 585,1 Å 3 , Z = 4 (при −33 °С) | 363.8 | 4.129 | ||||
| монофторфосфат цезия гидрогенизированный | ЦГПО 3 Ф | моноклинная: а = 14,478 Å, b = 5,929 Å, c = 5,413 Å, β = 103,30°, V = 452,2 Å 3 , Z = 4 [ 34 ] | 231.89 | |||||
| гидромонофторфосфат трицезия диаммония | Cs 3 (NH 4 ) 2 H 3 (PO 3 F) 4 | моноклинная: а = 20,619 Å, b = 12,076 Å, c = 15,856 Å, β = 102,58°, V = 3853 Å 3 , Z = 8 [ 34 ] | 829.72 | |||||
| монофторфосфат бария | BaPOBaPO3F F | моноклинная: а = 11,3105 Å, b = 8,6934 Å, c = 9,2231 Å, β = 127,819°, Z = 4 орторомбический [ 35 ] |
235.299 | 20836124 | 15600-53-0 [ 36 ] | |||
| Монофторфосфат ртути | Hg2POHg2PO3F F | орторомбические: a = 9,406 Å, b = 12,145 Å, c = 8,567 Å, V = 978,7 Å 3 , Z = 8 [ 37 ] | ||||||
| монофторфосфат свинца | PbPO 3 Ф | ромбический: a = 6,95 Å, b = 8,52 Å, c = 5,47 Å [ 38 ] | 6.24 | |||||
| гидрат дихлорида монофторфосфата дисвинца [ 7 ] | Pb 2 (PO 3 F)Cl 2 ·H 2 O | ромбический Pnma : a = 20,486 Å, b = 5,3967 Å, c = 6,9722 Å, V = 770,8 Å 3 , Z = 4 | 601.27 | 5.181 | ||||
| гидромонофторфосфат дитейламмония [ 16 ] | [NH 2 (CH 2 CH 3 ) 2 ]HPO 3 F | ромбический: a = 12,892 Å, b = 9,530 Å, c = 13,555 Å, α = 90°, V = 1665 Å 3 | 173.12 | 1.381 | ||||
| монофторфосфат тетраметиламмония [ 16 ] | [N(CH 3 ) 4 ] 2 PO 3 F | 246.26 | ||||||
| монофторфосфат тетраэтиламмония [ 16 ] | [N(CH 2 CH 3 ) 4 ] 2 PO 3 F | 358.47 | ||||||
| монофторфосфат тетрабутиламмония [ 16 ] | [N(CH 2 CH 2 CH 2 CH 3 ) 4 ] 2 PO 3 F | 582.90 | ||||||
| монофторфосфат пиперазиния гидрогенизированный [ 16 ] | [ПипзХ 2 ]HPO 3 F | моноклинная: а = 6,020 Å, b = 13,012 Å, c = 7,285 Å, α = 95,09°, V = 568,4 Å 3 | 286.11 | 1.672 | ||||
| моногидрат глютамина монофторфосфата | С 5 Н 12 Н 2 О 3 ПФО 3 | 246.131 | 19989732 | |||||
| глутамина монофторфосфат динатрий дихлорид | С 10 Н 20 Cl 2 ФН 4 Na 2 О 9 П | 507.146 | 143826 | 164002 | ||||
| анилин гидромонофторфосфат [ 39 ] | [ C6H8N 8] + [ HPO3F ] − | моноклинная: a = 9,418 Å, b = 14,31 Å, c = 6,303 Å, β = 92,45°, V = 859 Å 3 , Z = 4 | 193.12 | 1.51 | ||||
| Трис(2-карбамоилгуанидиний) гидрофторфосфонат моногидрат фторфосфоната [ 40 ] | [С 2 Н 7 Н 4 О + ] 3 [ HPO3F ] − [ПО 3 Ф] 2− ·Н 2 О | триклинная: а = 6,7523 Å, b = 8,2926 Å, c = 9,7297 Å, α = 100,630°, β = 90,885°, γ = 99,168°, V = 528,05 Å 3 | ||||||
| дигидрат бис(2-карбамоилгуанидиния)фторфосфоната [ 41 ] | [С 2 Н 7 Н 4 О + ] 2 [ПО 3 Ф] 2− ·2Н 2 О |
Органический
[ редактировать ]| Имя | Формула | Формула веса | ХимическийПаук | ПабХим | КАС | ||
|---|---|---|---|---|---|---|---|
| диметилфторфосфат | (СН 3 ) 2 ПО 2 Ф | 128.039 | 72304 | 80052 | 5954-50-7 | ||
| метилэтилфторфосфат | (СН 3 )(СН 3 СН 2 )PO 2 F | ||||||
| 1-[этокси(фтор)фосфорил]оксиэтан [ 42 ] | (СН 3 СН 2 ) 2 ПО 2 Ф | 156.093 | 67752 | 358-74-7 | |||
| изофлюрофат | [(СН 3 ) 2 СН] 2 ПО 2 Ф | 184.147 | 5723 | 5936 | 55-91-4 | ||
| 1-[фтор(2-оксопропокси)фосфорил]оксипропан-2-он | 212.113 | 129718773 | |||||
| изобутилметилфторфосфат [ 43 ] | 170.12 | 129684440 | |||||
| 1-[фтор(метокси)фосфорил]оксипентан | (СН 3 )(СН 3 СН 2 СН 2 СН 2 СН 2 )PO 3 F | 184.147 | 129761096 | ||||
| 1-[фтор(пропокси)фосфорил]оксипропан | (СН 3 СН 2 СН 2 ) 2 ПО 3 Ф | 184.147 | 4954063 | 6451603 | 381-45-3 | ||
| О -изопропилпропилфторфосфонат | (СН 3 ) 2 СН(СН 3 СН 2 СН 2 )PO 3 F | 184.147 | 88538036 | ||||
| О -1-метилбутилэтилфторфосфонат | 198.174 | 129761095 | |||||
| дибутилфторфосфат | (СН 3 СН 2 СН 2 СН 2 ) 2 ПО 3 Ф | 212.201 | 11640560 | 13025172 | 674-48-6 | ||
| ди- втор -бутилфторфосфат | [СН 3 СН 2 СН(СН 3 )] 2 ПО 3 Ф | 212.201 | 92528 | 102452 | 625-17-2 | ||
| ди(1,3-диметил- н -бутил)фторфосфат | [(СН 3 ) 2 СНСН 2 СН(СН 3 )] 2 ПО 3 Ф | 268.309 | 91838 | 101643 | 311-60-4 | ||
| 1-[фтор(2-метилпентан-3-илокси)фосфорил]оксиоктан | 296.363 | 129760905 | |||||
| метиларахидоноилфторфосфонат | 400.471 | 11741711 | 9916415 | ||||
| 12-[фтор(пропан-2-илокси)фосфорил]оксидодек-1-ен | 308.374 | 129892247 | |||||
| бис(4-фенилбутил)фторфосфат | (C 6 H 5 CH 2 CH 2 CH 2 CH 2 ) 2 PO 3 F | 364.397 | 162961 | 187452 | 85473-46-7 | ||
| 3'-фтор-3'-дезокситимидин 5'-фторфосфат | 326.193 | 2339398 | 3081896 | 152829-59-9 | |||
| цитидин-5'-фторфосфат | 325.189 | 87861929 | 68521-86-8 | ||||
| хлорфторметилиденамино-2-хлорэтилфторфосфат | ClFC=NClCH 2 CH 2 PO 3 F | A-230 Novichok agent [ 44 ] | |||||
| хлорфторметилиденамино-1-метил-2-хлорэтилфторфосфат | ClFC=NClCH 2 CH(CH 3 )PO 3 F | A-232 Novichok agent | |||||
| хлорфторметилиденамино-1,2-диметил-2-хлорэтилфторфосфат | ClFC=NCl(CH 3 )CHCH(CH 3 )PO 3 F | A-234 Novichok agent |
Использование
[ редактировать ]Монофторфосфат цинка можно использовать в качестве ингибитора коррозии стали в присутствии соли. [ 45 ]
Глутамина монофторфосфат использовался в качестве фторсодержащего лекарства.
Ссылки
[ редактировать ]- ^ Коттон, Ф. Альберт; Уилкинсон, Джеффри (1966). Продвинутая неорганическая химия: подробный текст . Джон Уайли и сыновья. п. 516.
- ^ Бэйнс, Джон В.; Доминичак, Марек Х. (2018). Электронная книга по медицинской биохимии . Elsevier Науки о здоровье. п. 72. ИСБН 9780702073007 .
- ^ Зех, Рональд; Хемнитиус, ЙоргМ. (2002). «PON1 у разных видов». Параоксоназа (PON1) в здоровье и болезни . Спрингер США. стр. 137–163. дои : 10.1007/978-1-4615-1027-7_7 . ISBN 9781461353584 .
- ^ Шоу, Кэти М.; Шелби, Джеймс Э. (1988). «Влияние соединений свинца на свойства фторфосфатных стекол олова». Журнал Американского керамического общества . 71 (5): C252–C253. дои : 10.1111/j.1151-2916.1988.tb05071.x . ISSN 0002-7820 .
- ^ Шюльке, У.; Кайзер, Р. (1991). «Производство фторфосфатов, дифторфосфатов, фторфосфонатов и фторфосфитов во фторидсодержащем расплаве карбамида». Журнал неорганической и общей химии (на немецком языке). 600 (1): 221–226. дои : 10.1002/zaac.19916000130 . ISSN 0044-2313 .
- ^ Jump up to: а б Вейль, Матиас; Пухбергер, Майкл; Фюглейн, Эккехард; Баран, Энрике Дж.; Ваннаме, Джулия; Якобсен, Ханс Дж.; Скибстед, Йорген (2007). «Выращивание монокристаллов и характеристика монофторфосфата дисеребра (I) (V), Ag 2 PO 3 F: кристаллическая структура, термическое поведение, колебательная спектроскопия и твердотельное состояние». 19 Ф, 31 П и 109 Ag MAS ЯМР-спектроскопия». Неорганическая химия . 46 (3): 801–808. doi : 10.1021/ic061765w . ISSN 0020-1669 . PMID 17257023 .
- ^ Jump up to: а б с д и ж г час я дж к л м н тот п Вейль, Матиас (7 января 2021 г.). «Монофторфосфаты — новые примеры и обзор PO 3 F». 2− Анион» . Химия . 3 (1): 45–73. doi : 10.3390/chemistry3010005 .
- ^ Jump up to: а б с д и ж Ву, Мэнфан; Фэн, Цзюньвэй; Се, Цунвэй; Туди, Абудукади; Чу, Дундун; Лу, Хуанхуан; Пан, Шили; Ян, Чжихуа (31 августа 2022 г.). «От фторида фосфата к фторофосфату: разработка новых нелинейных оптических материалов для ультрафиолета и глубокого ультрафиолета для BePO 3 F с улучшением оптических свойств» . Прикладные материалы и интерфейсы ACS . 14 (34): 39081–39090. дои : 10.1021/acsami.2c12001 . ISSN 1944-8244 . ПМИД 35980008 . S2CID 251645352 .
- ^ Jump up to: а б Бхаттачарджи, Маниш; Чаудхури, Михир К. (1987). «Прямой синтез моногидрата монофторфосфата аммония, [NH4 ] 2 [ PO3F ] ·H2O и монофторфосфата калия, K2 [ PO3F ] » Журнал Химического общества, Dalton Transactions (2): 477.doi : 10.1039 /DT9870000477 . ISSN 0300-9246 .
- ^ Крупкова, Радмила; Фабри, Ян; Цисаржова, Ивана; Ванек, Пршемысл (2002). «Бис(аммоний)фторфосфат при комнатной температуре». Acta Crystallographica Раздел C. 58 (5): i66–i68. Бибкод : 2002AcCrC..58I..66K . дои : 10.1107/S010827010200553X . ISSN 0108-2701 . ПМИД 11983961 .
- ^ Берндт, А.Ф.; Сильвестр, Дж. М. (1972). «Кристаллическая структура монофторфосфата аммония: (NH 4 ) 2 PO 3 F·H2O» (PDF) . Acta Crystallographica Раздел B. 28 (7): 2191–2193. Бибкод : 1972AcCrB..28.2191B . дои : 10.1107/S0567740872005771 . ISSN 0567-7408 .
- ^ Jump up to: а б Перлофф, А. (1 июля 1972 г.). «Кристаллические структуры гидратированных монофторфосфатов кальция и аммония: CaPO 3 F·2H 2 O и (NH 4 ) 2 PO 3 F·H 2 O». Acta Crystallographica Раздел B. 28 (7): 2183–2191. дои : 10.1107/S056774087200576X .
- ^ Цю, Хаотянь; Цай, Вэньбин; Ян, Чжихуа; Лю, Янли; Мутайлипу, Миридинг; Пан, Шили (04 августа 2021 г.). «Тетрафторборат-монофторфосфат (NH 4 ) 3 [PO 3 F][BF 4 ]: первый член оксифторида со связями B–F и P–F» . ACS Органическое и неорганическое золото . 1 (1): 6–10. doi : 10.1021/acsorginorgau.1c00018 . ISSN 2694-247X . ПМЦ 9954260 . ПМИД 36855636 . S2CID 238826305 .
- ^ Jump up to: а б с Потому что, Матиас; Хойслер, Томас; Бонно, Барбара; Фюглейн, Эккехард (08 ноября 2023 г.). «Структурные фазовые переходы в двойных солях (NH4)2PO3F NH4NO3 и (NH4)2XO4 · 3NH4NO3 (X = Se, Cr)» . Неорганический . 11 (11): 433. doi : 10.3390/inorganics11110433 . ISSN 2304-6740 .
- ^ Цю, Хаотянь; Ли, Дымящийся; Цзинь, Конгконг; Лу, Хуанхуан; Ян, Чжихуа; Пан, Шили; Мутайлипу, Миридинг (2022 г.). «(N 2 H 6 )[HPO 3 F] 2 : максимизация оптической анизотропии фторфосфатов глубокого ультрафиолета» . Химические коммуникации . 58 (37): 5594–5597. дои : 10.1039/D2CC01035F . ISSN 1359-7345 . ПМИД 35437534 . S2CID 248240938 .
- ^ Jump up to: а б с д и ж Прескотт, Хиллари Энн (1 августа 2002 г.). Кристаллические структуры и термическое поведение монофторфосфатов водорода и основных монофторфосфатов с катионами щелочных металлов и N-содержащими катионами (докторская диссертация). Берлинский университет имени Гумбольдта, факультет математики и естественных наук И.п. 32. дои : 10.18452/14706 . Проверено 1 ноября 2014 г.
- ^ Пайен, Жан-Люк; Дюран, Жан; Кот, Луи; Галинь, Жан-Луи (1979). исследование монофторфосфата калия 2 PO 3 » Структурное « K F . Канадский химический журнал . 57 (8): 886–889. дои : 10.1139/v79-146 . ISSN 0008-4042 .
- ^ Гриммер, Арнд-Рюдигер; Мюллер, Дирк; Нилс, Йохен (1985). «Твердотельный ЯМР высокого разрешения K 2 PO 3 F·KF». Журнал химии фтора . 29 (1–2): 60. doi : 10.1016/S0022-1139(00)83295-9 . ISSN 0022-1139 .
- ^ Jump up to: а б с Прескотт, Хиллари А.; Троянов Сергей Иванович; Кемниц, Эрхард (1 января 2003 г.). «Кристаллические структуры гидромонофторфосфатов калия KHPO 3 F и K 3 [H(PO 3 F) 2 ] и α-модификация RbHPO3F». Журнал кристаллографии – Кристаллические материалы . 218 (9): 604. Бибкод : 2003ЗК....218..604П . дои : 10.1524/zkri.218.9.604.20681 . S2CID 100991538 .
- ^ Фабри, Ян; Крупкова, Радмила; Цисаржова, Ивана (24 января 2003 г.). «Двуфторфосфат аммония дикалия при комнатной температуре». Acta Crystallographica Раздел E. 59 (2): i14–i16. Бибкод : 2003AcCrE..59I..14F . дои : 10.1107/S160053680300117X .
- ^ Jump up to: а б Роули, Х.Х.; Стаки, Джон Э. (1956). «Получение и свойства дигидрата монофторфосфата кальция». Журнал Американского химического общества . 78 (17): 4262–4263. дои : 10.1021/ja01598a022 . ISSN 0002-7863 .
- ^ Потому что, Матиас; Баран, Энрике Дж.; Кремер, Рейнхард К.; Либовицкий, Евгений (февраль 2015 г.). «Синтез, кристаллическая структура и свойства Mn(PO3F ) (H2O ) 2 » . Журнал неорганической и общей химии . 641 (2): 184–191. дои : 10.1002/zaac.201400587 .
- ^ Jump up to: а б Цзян, Цзяньхуа; Чжу, Бэй; Чжу, Тяньюй; Ян, Хаомин; Джин, Ён; Люй, Минфэн (2020). «Фторфосфаты переходных металлов аммония с открытой структурой и сеткой решетки Кагоме: синтез, структура и магнитные свойства» . Транзакции Далтона . 49 (3): 841–849. дои : 10.1039/C9DT03370J . ISSN 1477-9226 . ПМИД 31854410 . S2CID 209418354 .
- ^ Jump up to: а б с Мевиус, Фрэнк; Цимер, Буркхард; Майзель, Манфред; Грант, Герберт (1985). «О новом типе монофторфосфата меди». Журнал химии фтора . 29 (1–2): 68. doi : 10.1016/S0022-1139(00)83303-5 . ISSN 0022-1139 .
- ^ Беррахо, М.; Вегас, А.; Мартинес Риполь, М.; Рафик, М. (1994). «Монофторфосфат меди Cu(H 2 O) 2 (NH 4 ) 2 (PO 3 F) 2 ». Acta Crystallographica Раздел C. 50 (5): 666–668. Бибкод : 1994AcCrC..50..666B . дои : 10.1107/S0108270193010789 . ISSN 0108-2701 .
- ^ Мёвиус, Ф.; Мейзель, М.; Кирк, Х.; Унгер, В.; Сипе, Д.; Мецнер, В. (1990). «Фторфосфаты — новая группа средств для консервации древесины». Дерево как сырье и материал (на немецком языке). 48 (9): 345–350. дои : 10.1007/BF02639896 . ISSN 0018-3768 . S2CID 27956978 .
- ^ Jump up to: а б Фабри, Ян; Душек, Михал; Фейфарова, Карла; Крупкова, Радмила; Ванек, Пржемысл; Цисаржова, Ивана (2006). «Фтортриоксофосфат дирубидия, Rb 2 PO 3 F, при 290 и 130 К, и фтортриоксофосфат дицезия, Cs 2 PO 3 F, при 240 и 100 К». Acta Crystallographica Раздел C. 62 (6): i49–i52. Бибкод : 2006AcCrC..62I..49F . дои : 10.1107/s0108270106016350 . ISSN 0108-2701 . ПМИД 16763294 .
- ^ «Перечень веществ» . Атомворк . Проверено 4 ноября 2014 г.
- ^ Ян, Синь-Жуй; Лю, Синь; Ван, Цзуцзянь; Дэн, Сюэбин; Лу, Хэ-Цзе; Ли, Ю-Цзя; Лонг, Сифа; Чен, Линг; Ву, Ли-Мин (2021). «Na 1,5 Rb 0,5 PO 3 F·H 2 O: синтез, свойства и ступенчатая реконструкция сети водородных связей» . Границы неорганической химии . 8 (20): 4544–4552. дои : 10.1039/D1QI00895A . ISSN 2052-1553 . S2CID 238948341 .
- ^ Рафик, М.; Дюран, Дж.; Кот, Л. (1979). «Кристаллографическое исследование фосфитов щелочноземельных металлов». Доклады Академии наук, серия С. 288 (15): 411–413.
- ^ Менц, Д.-Х.; Колдиц, Л.; Хит, К.; Кунерт, Ч.; Менсинг, Ч. (1986). «О термическом разложении 3 F 2 » H . SrPO O Журнал неорганической и общей химии . 540 (9–10): 191–197. дои : 10.1002/zaac.19865400920 . ISSN 0044-2313 .
- ^ Вейль, Матиас (14 апреля 2007 г.). «NH 4 Ag 3 (PO 3 F) 2 , слоистый монофторфосфат (V) с семью различными центрами Ag». Acta Crystallographica Раздел C. 63 (5): i31–i33. Бибкод : 2007AcCrC..63I..31W . дои : 10.1107/S0108270107008967 . ПМИД 17478892 .
- ^ Ян, Синь Жуй; Лю, Синь; Чен, Линг; Ву, Ли Мин (апрель 2022 г.). «Прозрачный для глубокого ультрафиолета двулучепреломляющий монофторфосфат: Cd2,5(NH4)2(PO3F)3Cl·2H2O» . Журнал неорганической и общей химии . 648 (15): заак.202200034. дои : 10.1002/zaac.202200034 . ISSN 0044-2313 . S2CID 247895381 .
- ^ Jump up to: а б Кемниц, Эрхард; Прескотт, Хиллари А.; Троянов, Сергей И. (1 января 2000 г.). «Кристаллические структуры двух монофторфосфатов водорода: CsHPO 3 F и Cs 3 (NH 4 ) 2 (HPO 3 F) 3 (PO 3 F)». Журнал кристаллографии - Кристаллические материалы . 215 (4): 240. Бибкод : 2000ZK....215..240K . дои : 10.1524/zkri.2000.215.4.240 . S2CID 91421180 .
- ^ Штёгер, Бертольд; Вейль, Матиас; Скибстед, Йорген (2013). «Возврат к кристаллической структуре BaPO 3 F – комбинированная рентгеноструктурная и твердотельная дифракция. 19 Ф, 31 Исследование P MAS NMR». Dalton Transactions . 42 (32): 11672–11682. doi : 10.1039/C3DT50373A . ISSN 1477-9226 . PMID 23838743 .
- ^ «15600-53-0 – QNHNZAMKMLIQRR-UHFFFAOYSA-L – Фторфосфат бария» . ХимИДплюс . Проверено 4 ноября 2014 г.
- ^ Вейль, Матиас; Пухбергер, Майкл; Баран, Энрике Дж. (декабрь 2004 г.). «Получение и характеристика монофторфосфата диртути (I) (V), Hg 2 PO 3 F: кристаллическая структура, термическое поведение, колебательные спектры и твердотельное состояние». 31 П и 19 F ЯМР Спектры». Неорганическая химия . 43 (26): 8330–8335. doi : 10.1021/ic048741e . PMID 15606179 .
- ^ Уолфорд, ЛК (1967). «Данные по монокристаллам и порошкам фторфосфата свинца» . Акта Кристаллографика . 22 (2): 324. Бибкод : 1967AcCry..22..324W . дои : 10.1107/S0365110X67000593 . ISSN 0365-110X .
- ^ Хаулани Идрисси, А.; Рафик, М.; Гужон, П.; Герен, Р. (15 июля 1995 г.). «Анилиний-водородмонофторфосфат, C 6 ЧАС 8 Н + ·ГПО 3 Ф − ". Acta Crystallographica Раздел C. 51 ( 7): 1359–1361. doi : 10.1107/S010827019401214X .
- ^ Фабри, Ян; Фридрихова, Микаэла; Душек, Михал; Фейфарова, Карла; Крупкова, Радмила (2011). «Трис(2-карбамоилгуанидин)гидрофторфосфонат моногидрат фторфосфоната» . Acta Crystallographica Раздел E. 68 (1): о47–о48. дои : 10.1107/S1600536811051683 . ISSN 1600-5368 . ПМЦ 3254407 . ПМИД 22259550 .
- ^ Фабри, Ян; Фридрихова, Микаэла; Душек, Михал; Фейфарова, Карла; Крупкова, Радмила (2012). «Два полиморфа дигидрата бис (2-карбамоилгуанидиния) фторфосфоната». Acta Crystallographica Раздел C. 68 (2): о71–о75. Бибкод : 2012AcCrC..68O..71F . дои : 10.1107/S0108270111053133 . ISSN 0108-2701 . ПМИД 22307257 .
- ^ Заворин С.И.; Лермонтов, С.А.; Мартынов И.В. (май 1988 г.). «Фторирование некоторых производных фосфорной кислоты». Вестник Отделения химических наук АН СССР . 37 (5): 1033–1035. дои : 10.1007/BF00957090 . S2CID 98659309 .
- ^ Ордентлих, Арье; Барак, Руфь; Барак, Дов; Фишер, Меир; Беншоп, Хендрик П.; Де Йонг, LeoPA; Сигалл, Йоффи; Велан, Барух; Шафферман, Авигдор (1998). «ESMS как уникальный инструмент молекулярного мониторинга реакций между HuAChE и различными ФОП-агентами». Структура и функции холинэстераз и родственных белков . Спрингер США. п. 249. дои : 10.1007/978-1-4899-1540-5_74 . ISBN 9781489915429 .
- ^ Халамек, Эмиль и Коблиха, Збинек. (2011). Потенциальные химические боевые агенты. Химические письма. 105. 323-333.
- ^ Дюпра, М.; Боннель, А.; Дабоси, Ф.; Дюран, Дж.; Кот, Л. (1983). «Монофторфосфаты цинка и калия как ингибиторы коррозии углеродистой стали в 3% растворе NaCl». Журнал прикладной электрохимии . 13 (3): 317–323. дои : 10.1007/BF00941603 . ISSN 0021-891X . S2CID 95845823 .