Фосфония


4 , родительский катион фосфония.
В химии термин фосфония (более неясно: фосфиниум ) описывает полиатомные катионы с химической формулой P r +
4 (где r - водород или алкильная , арильная или галогенная группа). Эти катионы имеют тетраэдрические структуры . Соли , как правило, бесцветны или берут цвет анионов. [ 1 ]
Типы катионов фосфония
[ редактировать ]Протонированные фосфины
[ редактировать ]Родительский фосфония - pH +
4 Как найдено в йодидной соле, йодид фосфония . Соли родительского рН +
4 редко встречаются, но этот ион является промежуточным в приготовлении промышленно полезного тетракиса (гидроксиметил) хлорид фосфония :
- PH 3 + HCl + 4 Ch 2 O → P (Ch
2 Ох) +
4 кл −
Многие соли из организма организма вырабатываются протонированием первичных, вторичных и третичных фосфинов :
- PR 3 + H + → Hpr +
3
Основность фосфинов следует обычным тенденциям, причем r = алкил является более основным, чем r = арил. [ 2 ]
Тетраорганофосфония катионов
[ редактировать ]Наиболее распространенные соединения фосфония имеют четыре органических заместителя, прикрепленных к фосфору. Катионы четвертичного фосфония включают тетрафенилфосфонию , (C 6 H 5 ) 4 P + и тетраметилфосфония P (гл
3 ) +
4 .


Четвертичные катионы фосфония ( PR +
4 ) продуцируются алкилированием органофосфинов. [ 3 ] Например, реакция трифенилфосфина с метилбромидом дает метилтрифенилфосфона бромид :
- PP 3 + CH 3 BR → [CH 3 PPP 3 ] + Бренд −
Метильная группа в таких солях фосфония слегка кисла, причем AP K оценивается около 15: [ 5 ]
- [CH 3 PPP 3 ] + + База → CH 2 = PPH 3 + [HBASE] +
Эта реакция депротонирования дает реагенты Виттига . [ 6 ]
Фосфор пентахлорид и связанные с ним соединения
[ редактировать ]Твердый фосфор пентахлорид является ионным соединением , сформулированным PCL +
4 Pcl −
6 , то есть соль, содержащая тетрахлорфосфониум. [ 7 ] [ 8 ] Разбавленные растворы диссоциируются в соответствии со следующим равновесием:
- PCL 5 ⇌ PCL +
4 + cl −
Трифенилфосфиндихлорид (pH 3 PCL 2 ) существует как в виде пентакоордината фосфорана, так и в виде хлорторифенилфосфона хлорида, в зависимости от среды. [ 9 ] Ситуация похожа на ситуацию с PCL 5 . Это ионное соединение (PPH 3 CL) + Калькуляция − в полярных растворах и молекулярных видах с тригональной бипирамидной молекулярной геометрией в аполярном растворе. [ 10 ]
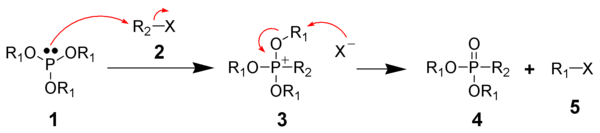
Алкоксифосфония соли: реакция Арбузова
[ редактировать ]Реакция Михаэлиса -Арбузова представляет собой химическую реакцию тривалентного вида фосфорного эфира с алкилгалогенидом с образованием пентавалентного фосфора и еще одного алкилгалогенида. Обычно подложка фосфора представляет собой фосфитный сложный эфир (P (или) 3 ), а алкилирующий агент представляет собой алкил йодид. [ 11 ]
Использование
[ редактировать ]Текстильный отдел
[ редактировать ]
Тетракис (гидроксиметил) хлорид фосфония имеет промышленное значение в производстве устойчивой к складке и пламенем отделки на хлопковом текстиле и других целлюлозных тканях. [ 12 ] [ 13 ] Пламя-отдаленная отделка может быть подготовлена из THPC с помощью вероятного процесса, [ 14 ] в котором THPC обрабатывается мочевиной. Мороженое . конденсируется гидроксиметильными группами на THPC Структура фосфония превращается в оксид фосфина в результате этой реакции. [ 15 ]
Катализаторы-переноса фазы и ускоряющие агенты
[ редактировать ]Органические катионы фосфония являются липофильными и могут быть полезны в катализе переноса фазы , очень похожий на соли четвертичного аммония. Соли или неорганические анионы и тетрафенилфосфония ( PPH +
4 ) растворимы в полярных органических растворителях. Одним из примеров является Perrhenate (PPH 4 [Reo 4 ]). [ 16 ]
Реагенты на органический синтез
[ редактировать ]Реагенты Виттига используются в органическом синтезе . Они получены из соли фосфония. сильная база, такая как бутиллит Для депротонирования требуется или амид натрия:
- [PH 3 P. + Ch 2 R] x − + C 4 H 9 li → ph 3 p = chr + lix + c 4 H 10
Одним из самых простых илидов является метилентрифенилфосфоран (pH 3 P = CH 2 ). [ 6 ]
Соединения pH 3 PX 2 (x = Cl, Br) используются в реакции кирсанов . [ 17 ] Реакция Kinnear -Perren используется для приготовления алкилфосфонильных дихлоридов (RP (O) Cl 2 ) и сложных эфиров (RP (O) (или ′) 2 ). Ключевым промежуточным соединением являются алкилтрихлорфосфониумные соли, полученные алкилированием фосфора трихлорида : [ 18 ]
- RCL + PCL 3 + ALCL 3 → [RPCL 3 ] + Алкл −
4
Производство аммиака для "зеленого водорода"
[ редактировать ]Основной промышленной процедурой для производства аммиака сегодня является процесс теплового габера-боша , который обычно использует ископаемый газ в качестве источника водорода, который затем объединяется с азотом для получения аммиака. В 2021 году профессор Дуг Макфарлейн и соавторы Александр Симонов и Брайан Сурьянто из Университета Монаш разработали метод производства зеленого аммиака, который может сделать устаревшие растения Хабер-Боша. [ 19 ] Их процесс похож на подход электролиза для производства водорода. Работая с зеленой местной компанией, которая хотела сделать отбеливатель из соленой воды путем электролиза, Суританто обнаружил, что соль тетраалкилфосфония позволила эффективному производству аммиака при комнатной температуре. [ 20 ]
Смотрите также
[ редактировать ]- Аммоний ( NH +
4 ) - Подряд ( пепел +
4 ) - Гидроний (H 3 O + )
- Святые соединения
- Органофосфоровый химия
Ссылки
[ редактировать ]- ^ Corbridge, Dec (1995). Phosphorus: план его химии, биохимии и технологий (5 -е изд.). Амстердам: Elsevier. ISBN 978-0-444-89307-9 .
- ^ Li, T.; Lough, AJ; Моррис, RH (2007). «Шкала кислотности тетрафлороборативных солей соединений фосфония и гидридов железа в [D 2 ] дихлорметане». Химический Евро. Дж . 13 (13): 3796–3803. doi : 10.1002/chem.200601484 . PMID 17245785 .
- ^ Jump up to: а беременный H.-F. Кляйн (1978). «Триметилфосфония метилд (триметилметиленфосфоран)». Неорганические синтезы . Неорганические синтезы. Тол. 18. С. 138–140. doi : 10.1002/9780470132494.CH23 . ISBN 9780470132494 .
- ^ Финч, А.; Fitch, an; Gates, PN (1993). «Кристаллическая и молекулярная структура метастабильной модификации фосфора пентахлорида». Журнал химического общества, химическая связь (11): 957–958. doi : 10.1039/c39930000957 .
- ^ Линг-Чунг, Сим; Продажи, Кит Д.; Утли, Джеймс Х.П. (1990). «Измерение значений P для a солей фосфония посредством кинетики переноса протона в электрогензируемое основание». Журнал химического общества, химическая связь (9): 662. doi : 10.1039/c39900000662 .
- ^ Jump up to: а беременный Виттиг; Schoellkopf, U. (1960). «Метиленциклогексан». Органические синтезы . 40 : 66. doi : 10.15227/orgsyn.040.0066 . Полем Описывает PH 3 P = CH 2 .
- ^ Холмен, AF; Wiber, E.; Wiberg, N. (2001). Неорганическая химия . Академическая пресса. ISBN 978-0-12-352651-9 .
- ^ Сутер, RW; Кначел, HC; Петро, вице -президент; Howatson, JH & Shore, SG (1978). «Природа фосфора (v) хлорида в ионизирующих и неионизирующих растворителях». Журнал Американского химического общества . 95 (5): 1474–1479. doi : 10.1021/ja00786a021 .
- ^ SM Годфри; CA McAuliffe; RG Pritchard; JM Шеффилд (1996). "Рентгеновское кристаллорграфическое исследование реагента pH 3 PCL 2 ; не трансфер заряд, R 3 P-Cl-Cl, тригональный бипирамидальный или [R 3 Pcl] Cl, но необычные динуклеарные ионные виды, [pH 3 pcl + ⋯Cl – ⋯ + CIPPH 3 ] CL, содержащий длинные контакты CL -CL ». Химическая связь (22): 2521–2522. DOI : 10.1039/CC9960002521 .
- ^ Дженнингс, ЭВ; Никитин, K; Ортин, y; Gilheany, DG (2014). «Вырожденная нуклеофильная замещение в солях фосфония». J. Am. Химический Соц 136 (46): 16217–16226. doi : 10.1021/ja507433g . PMID 25384344 .
- ^ Bhattacharya, AK; Tyagarajan, G. (1981). «Миачаэлис - Арбузов перестарается». Химический Преподобный 81 (4): 415–430. вам 10.10
- ^ Вейл, Эдвард Д.; Levchik, Sergei V. (2008). «Огнестипения в коммерческом использовании или разработке для текстиля». J. Fire Sci. 26 (3): 243–281. doi : 10.1177/0734904108089485 . S2CID 98355305 .
- ^ Свара, Юрген; Указку, Норберт; Хофманн, Томас. Соединения фосфора, органические. Энциклопедия промышленной химии Уллмана. John Wiley & Sons, Inc., 2008 Два : 10.1002/14356007.a19_545.pub2
- ^ "Часто задаваемые вопросы: что такое процесс Proban®?" Полем Rhodia percan. Архивировано из оригинала 7 декабря 2012 года . Получено 25 февраля 2013 года .
- ^ Ривз, Уилсон А.; Гатри, Джон Д. (1956). «Промежуточные для пламен-резистентных полимеров-реакций тетракиса (гидроксиметил) хлорид фосфония». Промышленная и инженерная химия . 48 (1): 64–67. doi : 10.1021/IE50553A021 .
- ^ Дилворт, младший; Хуссейн, W.; Хатсон, AJ; Джонс, CJ; McQuillan, FS (1996). «Тетрахало оксоренатные анионы». Неорганические синтезы . Неорганические синтезы. Тол. XXXI. С. 257–262. doi : 10.1002/9780470132623.ch42 . ISBN 9780470132623 .
- ^ Исследования по химии органофосфора. I. Преобразование спиртов и фенолов в галогениды третичными фосфиновыми дихалидами Ga Wiley, RL Hershkowitz, BM Rein, BC Chung J. Am. Химический Соц , 1964 , 86 (5), стр. 964–965 два : 10.1021/ja01059a073
- ^ Свара, Дж.; Взвешивание, н.; Хофманн Т. Энциклопедия Вейнхайм: Wiley-VCH doi : 10.1002/ 1436000 ISBN 978-3527306732 .
- ^ Прорыв приближает производство зеленого аммиака ближе к реальности
- ^ Снижение азота до аммиака с высокой эффективностью и скоростями на основе протона фосфония