Галоформная реакция
| Галоформная реакция | |
|---|---|
| Назван в честь | Адольф Либен |
| Тип реакции | Реакция замещения |
| Идентификаторы | |
| Портал органической химии | галоформная реакция |
| RSC Идентификатор онтологии | RXNO: 0000689 |
В химии галоформная реакция (также называемая галоформной реакцией Либена ) — химическая реакция , в которой галоформ ( CHX 3 , где X — галоген ) получают исчерпывающим галогенированием группы ацетильной ( R-C(=O)CH 3 , где R может быть атомом водорода, алкильной или арильной группой ), в присутствии основания . [ 1 ] [ 2 ] [ 3 ] Реакцию можно использовать для превращения ацетильных групп в карбоксильные группы ( R-C(=O)OH ) или для получения хлороформа ( CHCl 3 ), bromoform ( CHBr 3 ), или йодоформ ( ЧИ 3 ). Обратите внимание, что фтороформ ( CHF 3 ) невозможно приготовить таким образом.

Механизм
[ редактировать ]На первом этапе галоген диспропорционируется в присутствии гидроксида с образованием галогенида и гипогалогенита.
Если присутствует вторичный спирт, он окисляется до кетона гипогалитом:

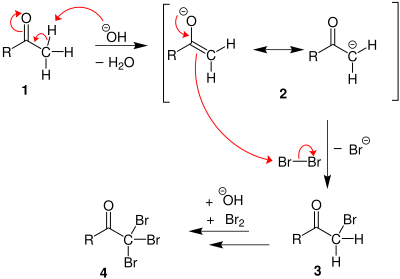
Если присутствует метилкетон, он реагирует с гипогалитом в три этапа:
1. В основных условиях кетон подвергается кето-енольной таутомеризации. Енолят подвергается электрофильной атаке со стороны гипогалогенита (содержащего галоген с формальным зарядом +1).
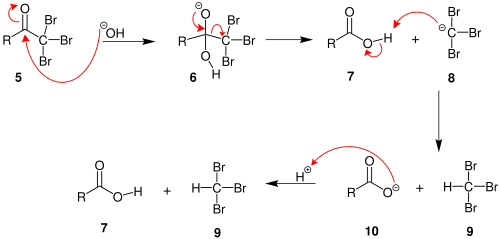
2. Когда положение α(альфа) полностью галогенировано, молекула претерпевает нуклеофильное ацильное замещение гидроксидом с − CX 3 — уходящая группа , стабилизированная тремя электроноакцепторными группами . На третьем этапе − Анион CX 3 отрывает протон либо от растворителя, либо от карбоновой кислоты, образовавшейся на предыдущем этапе, и образует галоформ. По крайней мере, в некоторых случаях ( хлоралгидрат ) реакция может быть остановлена и промежуточный продукт выделен, если условия кислые и используется гипогалит.
Объем
[ редактировать ]Субстраты в широком смысле ограничены метилкетонами и вторичными спиртами, окисляемыми до метилкетонов, такими как изопропанол . Единственными первичными спиртами и альдегидами , вступающими в эту реакцию, являются этанол и ацетальдегид соответственно. 1,3-Дикетоны, такие как ацетилацетон, также подвергаются этой реакции. β-кетокислоты, такие как ацетоуксусная кислота, также будут подвергаться тесту при нагревании. Ацетилхлорид и ацетамид в этой реакции не вступают. Используемый галоген может представлять собой хлор , бром , йод или гипохлорит натрия . [ 4 ] Фтороформ (CHF 3 ) не может быть получен этим методом, поскольку для этого потребуется присутствие очень нестабильного иона гипофторита . Однако кетоны структуры RCOCF 3 при обработке основанием расщепляются с образованием фтороформа; это эквивалентно второму и третьему шагам процесса, показанного выше.
Приложения
[ редактировать ]Лабораторный масштаб
[ редактировать ]
Эта реакция составляет основу йодоформного теста, который в истории широко использовался в качестве химического теста для определения присутствия метилкетона или вторичного спирта, окисляющегося до метилкетона. Когда в качестве реагентов используются йод и гидроксид натрия, положительная реакция дает йодоформ , который при комнатной температуре является твердым и имеет тенденцию выпадать в осадок из раствора, вызывая характерное помутнение.
В органической химии эту реакцию можно использовать для превращения концевого метилкетона в аналогичную карбоновую кислоту.
Промышленно
[ редактировать ]Раньше его использовали для промышленного производства йодоформа, бромоформа и даже хлороформа. [ нужна ссылка ]
Вариант этой реакции используется для производства дейтерированного хлороформа при реакции гексахлорацетона с тяжелой водой, катализируемой основанием: [ 5 ] [ 6 ]
- O=C(CCl 3 ) 2 + D 2 O → 2 CDCl 3 + CO 2
В дальнейшем варианте используется разложение трихлорацетата кальция в тяжелой воде: [ 7 ]
- Ca(CCl 3 CO 2 ) 2 + D 2 O → 2 CDCl 3 + CaCO 3 + CO 2
Как побочный продукт хлорирования воды.
[ редактировать ]Хлорирование воды может привести к образованию галоформ, если вода содержит подходящие химически активные примеси (например, гуминовую кислоту ). [ 8 ] [ 9 ] Существует опасение, что такие реакции могут привести к присутствию канцерогенных соединений. [ который? ] в питьевой воде. [ 10 ]
История
[ редактировать ]Галоформная реакция — одна из старейших известных органических реакций . [ 11 ] В 1822 году Жорж-Симон Серуллас добавил металлический калий к раствору йода в этаноле и воде с образованием формиата калия и йодоформа, называемых на языке того времени гидроиодидом углерода . [ 12 ] В 1832 году Юстус фон Либих сообщил о реакции хлораля с гидроксидом кальция с образованием хлороформа и формиата кальция. [ 13 ] Реакция была заново открыта Адольфом Либеном в 1870 году. [ 14 ] Йодоформный тест также называют йодоформной реакцией Либена . Обзор галоформной реакции с историческим разделом был опубликован в 1934 году. [ 2 ]
Ссылки
[ редактировать ]- ^ Марш, Джерри; Смит, Майкл Б. (2007). Найп, AC (ред.). Реакции, механизмы и структура расширенной органической химии марта (6-е изд.). Хобокен: Джон Уайли и сыновья. п. 484. ИСБН 9780470084946 .
- ^ Jump up to: а б Рейнольд К. Фьюсон и Бентон А. Булл (1934). «Галоформная реакция». Химические обзоры . 15 (3): 275–309. дои : 10.1021/cr60052a001 .
- ^ Чакрабартти, Трахановский, Окисление в органической химии , стр. 343–370, Academic Press, Нью-Йорк, 1978.
- ^ Бейн, Райан М.; Пуллиам, Кристофер Дж.; Рааб, Шеннон А.; Кукс, Р. Грэм (2016). «Химический синтез, ускоренный бумажным распылением: галоформная реакция». Журнал химического образования . 93 (2): 340–344. Бибкод : 2016ЖЧЭд..93..340Б . doi : 10.1021/acs.jchemed.5b00263 . ISSN 0021-9584 .
- ^ Полсен, П.Дж.; Кук, У.Д. (1 сентября 1963 г.). «Приготовление дейтерированных растворителей для спектрометрии ядерного магнитного резонанса». Аналитическая химия . 35 (10): 1560. doi : 10.1021/ac60203a072 .
- ^ Захарани, Лия; Йохан, Мохд Рафи Бин; Халиг, Надер Гаффари (2022). «Процесс экономии и энергосбережения при лабораторном производстве хлороформа-d». Исследования и разработки органических процессов . 26 (11): 3126–3129. дои : 10.1021/acs.oprd.2c00260 . S2CID 253071632 .
- ^ Иринг, Мейсон Х.; Клоук, Джон Б. (1951). «Новый синтез хлороформа-d1». Журнал Американского химического общества . 73 (2): 769–770. дои : 10.1021/ja01146a080 .
- ^ Рук, Йоханнес Дж. (1977). «Реакции хлорирования фульвокислот в природных водах». Экологические науки и технологии . 11 (5): 478–482. Бибкод : 1977EnST...11..478R . дои : 10.1021/es60128a014 . ISSN 0013-936X .
- ^ Рекхау, Дэвид А.; Певец, Филип С.; Малькольм, Рональд Л. (1990). «Хлорирование гуминовых материалов: образование побочных продуктов и химическая интерпретация». Экологические науки и технологии . 24 (11): 1655–1664. Бибкод : 1990EnST...24.1655R . дои : 10.1021/es00081a005 . ISSN 0013-936X .
- ^ Бурман, Джорджия (февраль 1999 г.). «Побочные продукты дезинфекции питьевой воды: обзор и подход к оценке токсичности» . Перспективы гигиены окружающей среды . 107 (Приложение 1): 207–17. дои : 10.1289/ehp.99107s1207 . ПМК 1566350 . ПМИД 10229719 .
- ^ Ласло Курти и Барбара Чако (2005). Стратегическое применение названных реакций в органическом синтезе . Амстердам: Эльзевир. ISBN 0-12-429785-4 .
- ^ Суреллас, Жорж-Симон (май 1822 г.). Примечания к гидриодату калия и гидриодической кислоте. – карбоновая кислота; moyen d'obtenir, à l'instant, ce composé тройной [ Заметки о йодистоводородном калии и о йодистоводородной кислоте – йодистоводородном; средства мгновенного получения этого соединения трех элементов ] (на французском языке). Мец, Франция: Антуан. На страницах 17–20 Суреллас получил йодоформ, пропуская смесь паров йода и пара над раскаленными углями. Однако позже, на страницах 28–29, он получил йодоформ, добавив металлический калий к раствору йода в этаноле (который также содержал немного воды).
- ^ Либих, Юстус фон (1832). «О соединениях, образующихся при реакции хлора с основанием [этанолом], эфиром [диэтиловым эфиром], нефтеобразующим газом [этиленом] и уксусным спиртом [ацетоном]». Анналы физики и химии . 2-я серия. 100 (2): 243–295. Бибкод : 1832АнП...100..243Л . дои : 10.1002/andp.18321000206 .
На стр. 259–265 Либих описывает хлоруглерод («хлорид углерода», хлороформ), но на стр. 264, Либих ошибочно утверждает, что брутто-формула хлороформа — C 2 Cl 5 . Из стр. 259: «Хлористый углерод. Это новое соединение получают путем смешивания хлораля с едкими щелочами, избытком известкового молока или баритовой воды и перегонки смеси». (Хлороформ. Это новое соединение получается, если смешать хлораль с избытком едких щелочей, известкового молока [раствор гидроксида кальция] или баритовой воды [раствор гидроксида бария] и [затем] перегнать смесь.) - ^ См.:
- Либен, Адольф (1870). «Об образовании йодоформа и применении этой реакции к химическому анализу» . Анналы химии. Дополнительный объем. (на немецком языке). 7 :218-236.
- Либен, Адольф (1870). «Постскриптум к статье об образовании йодоформа и применении этой реакции к химическому анализу» . Анналы химии. Дополнительный объем. (на немецком языке). 7 :377-378.