Саркопения
| Саркопения | |
|---|---|
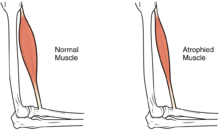 | |
| Разница между нормальной мышцей и атрофированной мышцей | |
| Специальность | Гериатрия Ревматология |
Саркопения ( код МКБ-10 M62.84) — это тип потери мышечной массы , который возникает с возрастом и/или неподвижностью . Он характеризуется дегенеративной потерей скелетных мышц массы, качества и силы . Скорость потери мышечной массы зависит от уровня физической нагрузки, сопутствующих заболеваний, питания и других факторов. Потеря мышечной массы связана с изменениями в сигнальных путях мышечного синтеза. Это отличается от кахексии , при которой мышцы разрушаются за счет деградации, опосредованной цитокинами , хотя эти два состояния могут сосуществовать. Саркопения считается компонентом синдрома слабости . [1] Саркопения может привести к снижению качества жизни, падениям, переломам и инвалидности. [2] [3]
Саркопения является фактором изменения состава тела . Когда это связано со старением населения, ожидается, что в первую очередь будут затронуты определенные области мышц, в частности, передняя часть бедра и мышцы живота. [2] [4] По данным популяционных исследований, индекс массы тела (ИМТ) снижается у стареющего населения, в то время как анализ биоэлектрического импеданса (BIA) показывает увеличение доли жира в организме. [5]
Этимология
[ редактировать ]Термин саркопения происходит от греческого σάρξ sarx , «плоть» и πενία penia , «бедность». Впервые это было предложено Розенбергом в 1989 году, который написал, что «возможно, не существует какой-либо одной особенности возрастного снижения, которая могла бы более существенно повлиять на передвижение, мобильность, потребление калорий, а также общее потребление питательных веществ и статус, независимость, дыхание и т. д.». [ нужна ссылка ]
Саркопения отличается от кахексии , при которой мышцы разрушаются за счет цитокин -опосредованной деградации, хотя эти два состояния могут сосуществовать.
Признаки и симптомы
[ редактировать ]Отличительным признаком саркопении является потеря мышечной массы или атрофия мышц . Изменение состава тела может быть трудно обнаружить из-за ожирения , изменений жировой массы или отеков . Изменения веса, окружности конечностей или талии не являются надежными индикаторами изменений мышечной массы. Саркопения также может вызывать снижение силы, функциональное снижение и повышенный риск падения. Саркопения также может не иметь симптомов, пока не станет тяжелой и часто не распознается. [1] Однако исследования показали, что гипертрофия может возникнуть в верхних частях тела, чтобы компенсировать потерю мышечной массы. [2] [6] Таким образом, одним из ранних индикаторов возникновения саркопении может быть значительная потеря мышечной массы в передней части бедра и мышцах живота. [2]
Причины
[ редактировать ]Существует множество предполагаемых причин саркопении, и она, вероятно, является результатом множества взаимодействующих факторов. Понимание причин саркопении является неполным, однако гормональные изменения, неподвижность, возрастные изменения мышц, питание и нейродегенеративные изменения признаны потенциальными причинными факторами. [7]
Степень саркопении определяется двумя факторами: исходным количеством мышечной массы и скоростью снижения мышечной массы. Из-за различий в этих факторах среди населения скорость прогрессирования и порог, при котором становится очевидной потеря мышечной массы, варьируются. [8] Неподвижность резко увеличивает скорость потери мышечной массы даже у молодых людей. Другие факторы, которые могут увеличить скорость прогрессирования саркопении, включают снижение потребления питательных веществ, низкую физическую активность или хронические заболевания. [1] Кроме того, эпидемиологические исследования показали, что раннее воздействие окружающей среды может иметь долгосрочные последствия для здоровья мышц. Например, низкий вес при рождении, маркер плохой окружающей среды в раннем возрасте, связан со снижением мышечной массы и силы во взрослой жизни. [9] [10] [11]
Патофизиология
[ редактировать ]Существует множество теорий, предложенных для объяснения механизмов мышечных изменений при саркопении, включая изменения в рекрутировании миосателлитных клеток , изменения в анаболической передаче сигналов, окислении белков, воспалении и факторах развития. Патологические изменения при саркопении включают снижение качества мышечной ткани, что выражается в замене мышечных волокон жиром, усиление фиброза , изменения мышечного метаболизма, окислительный стресс и дегенерацию нервно-мышечного соединения . [12] Считается, что неспособность активировать сателлитные клетки при травме или физической нагрузке способствует патофизиологии саркопении. [12] Кроме того, окисленные белки могут приводить к накоплению липофусцина и перекрестно-сшитых белков, вызывая накопление несократительного материала в скелетных мышцах и способствуя развитию саркопении мышц. [8]
В саркопенических мышцах распределение типов мышечных волокон меняется с уменьшением мышечных волокон типа II , или «быстросокращающихся», с незначительным уменьшением или отсутствием сокращения мышечных волокон типа I , или «медленно сокращающихся» мышечных волокон. Деиннервированные волокна II типа часто преобразуются в волокна I типа путем реиннервации медленными двигательными нервами волокон I типа. [13] Мужчины, возможно, более восприимчивы к этому связанному со старением переключению типа миофибрилл, поскольку недавнее исследование показало более высокий процент «медленно сокращающихся» мышечных волокон у пожилых мужчин по сравнению с молодыми мужчинами, но не у пожилых по сравнению с молодыми женщинами. [14]
Старение саркопенических мышц демонстрирует накопление мутаций митохондриальной ДНК , что также было продемонстрировано в различных других типах клеток. [15] Клоны с митохондриальными мутациями накапливаются в определенных участках мышцы, что сопровождается примерно пятикратным увеличением абсолютного числа копий мтДНК, то есть эти участки более плотные. [16] Очевидным защитным фактором, предотвращающим накопление поврежденных митохондрий в клетках, является достаточный уровень белка BNIP3 . Дефицит BNIP3 приводит к воспалению и атрофии мышц. [17]
Более того, не каждая мышца так восприимчива к атрофическим эффектам старения. Например, у обоих людей [18] и мыши [19] Было показано, что мышцы голени не так подвержены старению, как мышцы верхней части ног. Возможно, это можно объяснить различным распределением типов миофибрилл внутри каждой группы мышц, но это неизвестно.
Диагностика
[ редактировать ]Различные экспертные группы предложили множество диагностических критериев и продолжают оставаться областью исследований и дискуссий. Несмотря на отсутствие общепринятого определения, в 2016 году саркопении был присвоен код МКБ-10 (M62.84), признавший ее болезненным состоянием. [20]
Саркопению можно диагностировать, если у пациента мышечная масса по крайней мере на два стандартных отклонения ниже среднего значения для соответствующей популяции и медленная скорость ходьбы . [21] Европейская рабочая группа по саркопении у пожилых людей (EWGSOP) разработала широкое клиническое определение саркопении, обозначаемое как наличие низкой мышечной массы и либо низкой мышечной силы, либо низкой физической работоспособности. [7] Другие международные группы предложили критерии, включающие показатели скорости ходьбы, расстояния, пройденного за 6 минут, или силы хвата . [20] Сама по себе сила захвата руки также пропагандируется как клинический маркер саркопении, который является простым, экономически эффективным и имеет хорошую прогностическую силу, хотя и не дает исчерпывающей информации. [22]
Существуют инструменты скрининга саркопении, которые оценивают сообщаемые пациентами трудности при выполнении повседневных действий, таких как ходьба, подъем по лестнице или вставание со стула, и, как было показано, позволяют прогнозировать саркопению и плохие функциональные результаты. [23]
Биомаркеры
[ редактировать ]Поскольку саркопения представляет собой сложный клинический диагноз, циркулирующие биомаркеры были предложены в качестве индикаторов для ранней диагностики и прогнозирования, а также для последующего наблюдения и последовательной оценки реакции на вмешательства.
Старение и саркопения связаны с увеличением маркеров воспаления («воспалительное старение»), включая: С-реактивный белок , фактор некроза опухоли , интерлейкин-8 , интерлейкин-6 , гранулоцитарно-моноцитарный колониестимулирующий фактор , интерфероны и сериновую протеазу. А1 . [24]
Изменения гормонов, связанные со старением и саркопенией, включают снижение уровня половых гормонов тестостерона и сульфата дегидроэпиандростерона . [25] а также снижение уровня циркулирующего гормона роста и IGF-1 . [26]
Было обнаружено, что циркулирующие C-концевые фрагменты агрина (CAF) выше у пациентов с ускоренной саркопенией. [27]
Более низкие уровни в плазме аминокислот лейцина и изолейцина , а также других незаменимых аминокислот были обнаружены у ослабленных пожилых людей по сравнению с контрольной группой. [28] [29]
Аланинаминотрансфераза (АЛТ) отвечает за перенос α-аминогруппы от α-аминокислоты к α-кетокислоте, превращая пируват в аланин в скелетных мышцах. Низкая циркулирующая АЛТ является маркером низкой мышечной массы и саркопении. [30] а также для повышения активности заболевания у пациентов с воспалительными заболеваниями кишечника . [31]
Управление
[ редактировать ]Упражнение
[ редактировать ]Физические упражнения остаются методом выбора при саркопении, но внедрение результатов исследований в клиническую практику является сложной задачей. Тип, продолжительность и интенсивность упражнений различаются в разных исследованиях, что не позволяет назначать стандартизированные упражнения при саркопении. [32] Отсутствие физических упражнений является значительным фактором риска развития саркопении, а физические упражнения могут значительно замедлить скорость потери мышечной массы. [33] Физические упражнения могут быть эффективным вмешательством, поскольку стареющие скелетные мышцы сохраняют способность синтезировать белки в ответ на кратковременные упражнения с отягощениями. [34] Прогрессивная тренировка с отягощениями у пожилых людей может улучшить физическую работоспособность (скорость походки) и мышечную силу. [35] [36] [37] Увеличение физических упражнений может привести к увеличению количества клеточных митохондрий, увеличению плотности капилляров, а также увеличению массы и прочности соединительной ткани. [38]
Медикамент
[ редактировать ]В настоящее время не существует одобренных препаратов для лечения саркопении. [39] Тестостерон или другие анаболические стероиды также исследовались для лечения саркопении и, по-видимому, оказывают некоторое положительное влияние на мышечную силу и массу, но вызывают ряд побочных эффектов и вызывают опасения по поводу рака простаты у мужчин и вирилизации у женщин. [40] [41] Кроме того, недавние исследования показывают, что лечение тестостероном может вызывать неблагоприятные сердечно-сосудистые события. [42] [43] [44]
DHEA и гормон роста человека Было показано, что практически не оказывают никакого эффекта в этих условиях. Гормон роста увеличивает синтез мышечного белка и увеличивает мышечную массу, но в большинстве исследований не приводит к увеличению силы и функций. [40] Это, а также аналогичная недостаточная эффективность его эффектора инсулиноподобного фактора роста 1 (IGF-1) может быть связано с местной резистентностью к IGF-1 в стареющих мышцах, возникающей в результате воспаления и других возрастных изменений. [40]
Другие препараты, изучаемые в качестве возможных методов лечения саркопении, включают грелин , витамин D , ингибиторы ангиотензинпревращающего фермента и эйкозапентаеновую кислоту . [40] [41]
Питание
[ редактировать ]Потребление калорий и белка является важным стимулом для синтеза мышечного белка. [45] Пожилые люди могут не использовать белок так эффективно, как молодые люди, и им может потребоваться большее количество белка для предотвращения атрофии мышц. [21] Ряд экспертных групп предложили увеличить рекомендуемую норму потребления белка для старших возрастных групп до 1,0–1,2 г/кг массы тела в день. [46] [47] Обеспечение адекватного питания пожилых людей представляет интерес для профилактики саркопении и слабости, поскольку это простой и недорогой подход к лечению без серьезных побочных эффектов. [48]
Добавки
[ редактировать ]Компонентом саркопении является потеря способности стареющих скелетных мышц реагировать на анаболические стимулы, такие как аминокислоты , особенно в более низких концентрациях. Однако стареющие мышцы сохраняют способность анаболического ответа на белок или аминокислоты в больших дозах. что добавление больших доз аминокислот, особенно лейцина, противодействует потере мышечной массы с возрастом. Сообщалось, [49] Упражнения могут работать синергетически с добавками аминокислот. [39]
β-гидрокси β-метилбутират (HMB) представляет собой метаболит лейцина, который действует как сигнальная молекула, стимулируя синтез белка. [21] [39] Сообщается, что он имеет несколько целей, включая стимуляцию mTOR и снижение экспрессии протеасом. Его использование для предотвращения потери мышечной массы у пожилых людей постоянно подтверждается клиническими испытаниями. [50] [51] [52] Необходимы дополнительные исследования, чтобы определить точное влияние HMB на мышечную силу и функцию в этой возрастной группе. [51]
Эпидемиология
[ редактировать ]Распространенность саркопении зависит от определения, используемого в каждом эпидемиологическом исследовании. По оценкам, распространенность среди людей в возрасте 60–70 лет составляет 5–13% и увеличивается до 11–50% у людей старше 80 лет. Это соответствует >50 миллионам человек и, по прогнозам, затронет >200 миллионов в ближайшие 40 лет, учитывая рост численности пожилых людей. [7]
Влияние на общественное здравоохранение
[ редактировать ]Саркопения становится серьезной проблемой общественного здравоохранения, учитывая увеличение продолжительности жизни промышленно развитых групп населения и рост численности пожилых людей. Саркопения является предиктором многих неблагоприятных исходов, включая повышенную инвалидность, падения и смертность. [53] [54] Неподвижность или постельный режим в группах населения, предрасположенных к саркопении, могут оказать существенное влияние на функциональные результаты. У пожилых людей это часто приводит к снижению биологического резерва и повышенной уязвимости к стрессорам, известным как « синдром слабости ». Потеря мышечной массы тела также связана с повышенным риском инфекций, снижением иммунитета и плохим заживлением ран. Слабость, которая сопровождает мышечную атрофию, приводит к более высокому риску падений, переломов, физической инвалидности, потребности в стационарном уходе, снижению качества жизни, увеличению смертности и увеличению затрат на здравоохранение. [21] Это представляет собой значительное бремя для личности и общества, и его влияние на общественное здравоохранение получает все большее признание. [7]
Направления исследований
[ редактировать ]Существуют значительные возможности лучше понять причины и последствия саркопении и помочь в оказании клинической помощи. Это включает в себя выяснение молекулярных и клеточных механизмов саркопении, дальнейшее уточнение референтных популяций по этническим группам, проверку диагностических критериев и клинических инструментов, а также отслеживание частоты госпитализаций, заболеваемости и смертности. Также необходимы выявление и исследование потенциальных терапевтических подходов и сроков вмешательства. [55]
По состоянию на 2020 год [update], не существует лекарств, одобренных для лечения атрофии мышц у людей с хроническими заболеваниями, и поэтому существует неудовлетворенная потребность в анаболических препаратах с небольшим количеством побочных эффектов. Одним из аспектов, препятствующих одобрению лекарств для лечения кахексии и саркопении, являются разногласия в конечных результатах. Несколько клинических испытаний показали, что селективные модуляторы андрогенных рецепторов (SARM) улучшают мышечную массу у людей, но неясно, улучшаются ли также сила и физические функции. После многообещающих результатов исследования фазы II было доказано, что исследование остарина SARM фазы III увеличивает мышечную массу тела , но не показало значительного улучшения функций. [56] Ему и другим препаратам, таким как , стимулирующий секрецию гормона роста анаморелин , было отказано в одобрении регулирующих органов, несмотря на значительное увеличение мышечной массы из-за отсутствия доказательств того, что они повышают физическую работоспособность. не считало предотвращение снижения функциональности приемлемым конечным результатом Управление по санитарному надзору за качеством пищевых продуктов и медикаментов . Неизвестно, как SARM взаимодействуют с потреблением белка и тренировками с отягощениями у людей с атрофией мышц. [57] [58]
См. также
[ редактировать ]- Старение – биологический процесс старения.
- Кахексия – синдром, вызывающий потерю мышечной массы, не полностью обратимый.
- Динапения – потеря мышечной силы, не вызванная неврологическими или мышечными заболеваниями.
- Синдром слабости – слабость у пожилого человека.
- Гериатрия - специальность, которая занимается оказанием медицинской помощи пожилым людям.
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Петерсон С.Дж., Мозер М. (февраль 2017 г.). «Дифференциация саркопении и кахексии у онкологических больных». Питание в клинической практике . 32 (1): 30–39. дои : 10.1177/0884533616680354 . ПМИД 28124947 . S2CID 206555460 .
- ^ Перейти обратно: а б с д Ата А.М., Кара М., Каймак Б., Озчакар Л. (октябрь 2020 г.). «Саркопения – это не любовь: нужно посмотреть, где вы ее потеряли!». Американский журнал физической медицины и реабилитации . 99 (10): е119–е120. дои : 10.1097/PHM.0000000000001391 . ПМИД 32084033 . S2CID 211245329 .
- ^ Бодар С., Заария М., Пасло Ф., Реджинстер Ж.Ю., Брюйер О. (2017). «Исходы саркопении для здоровья: систематический обзор и метаанализ» . ПЛОС ОДИН . 12 (1): e0169548. Бибкод : 2017PLoSO..1269548B . дои : 10.1371/journal.pone.0169548 . ПМК 5240970 . ПМИД 28095426 .
- ^ Ата А.М., Кара М., Каймак Б., Гюрчай Э., Чакыр Б., Юнлю Х. и др. (2019). «Региональная и общая мышечная масса, мышечная сила и физическая работоспособность: потенциальное использование ультразвуковой визуализации при саркопении». Архив геронтологии и гериатрии . 83 : 55–60. дои : 10.1016/j.archger.2019.03.014 . ПМИД 30953961 . S2CID 96463073 .
- ^ Ранасингхе С., Гамаге П., Катуланда П., Андравира Н., Тилакаратне С., Таранга П. (сентябрь 2013 г.). «Взаимосвязь между индексом массы тела (ИМТ) и процентным содержанием жира в организме, оцененным с помощью биоэлектрического импеданса, в группе взрослых жителей Шри-Ланки: поперечное исследование» . BMC Общественное здравоохранение . 13 : 797. дои : 10.1186/1471-2458-13-797 . ПМЦ 3766672 . ПМИД 24004464 .
- ^ Озкал О, Кара М, Топуз С, Каймак Б, Баки А, Озчакар Л (ноябрь 2019 г.). «Оценка мышц корпуса и нижних конечностей на предмет статического/динамического баланса у пожилых людей: ультразвуковое исследование» . Возраст и старение . 48 (6): 881–887. doi : 10.1093/ageing/afz079 . ПМИД 31268513 .
- ^ Перейти обратно: а б с д Круз-Джентофт А.Дж., Байенс Дж.П., Бауэр Дж.М., Бойри И., Седерхольм Т., Ланди Ф. и др. (июль 2010 г.). «Саркопения: Европейский консенсус по определению и диагностике: Отчет Европейской рабочей группы по саркопении у пожилых людей» . Возраст и старение . 39 (4): 412–423. doi : 10.1093/ageing/afq034 . ПМК 2886201 . ПМИД 20392703 .
- ^ Перейти обратно: а б Марсель Т.Дж. (октябрь 2003 г.). «Саркопения: причины, последствия и профилактика» . Журналы геронтологии. Серия А, Биологические и медицинские науки (обзор). 58 (10): М911–М916. дои : 10.1093/gerona/58.10.m911 . ПМИД 14570858 .
- ^ Сэйер А.А., Сиддалл Х.Э., Гилбоди Х.Дж., Деннисон Э.М., Купер С. (сентябрь 2004 г.). «Происходит ли саркопения в раннем возрасте? Результаты когортного исследования в Хартфордшире» . Журналы геронтологии. Серия А, Биологические и медицинские науки . 59 (9): М930–М934. дои : 10.1093/gerona/59.9.M930 . ПМИД 15472158 .
- ^ Гейл С.Р., Мартин С.Н., Келлингрей С., Истелл Р., Купер С. (январь 2001 г.). «Внутриутробное программирование состава тела взрослого человека» . Журнал клинической эндокринологии и метаболизма . 86 (1): 267–272. дои : 10.1210/jcem.86.1.7155 . ПМИД 11232011 .
- ^ Юлихарсила Х., Каянти Э., Осмонд С., Форсен Т., Баркер Д.Д., Эрикссон Дж.Г. (сентябрь 2007 г.). «Размер при рождении, состав тела взрослого человека и мышечная сила в дальнейшей жизни» . Международный журнал ожирения . 31 (9): 1392–1399. дои : 10.1038/sj.ijo.0803612 . ПМИД 17356523 .
- ^ Перейти обратно: а б Райалл Дж.Г., Шерцер Дж.Д., Линч Г.С. (август 2008 г.). «Клеточные и молекулярные механизмы, лежащие в основе возрастного истощения и слабости скелетных мышц». Биогеронтология (обзор). 9 (4): 213–228. дои : 10.1007/s10522-008-9131-0 . ПМИД 18299960 . S2CID 8576449 .
- ^ Доэрти Ти Джей (октябрь 2003 г.). «Приглашенный обзор: Старение и саркопения». Журнал прикладной физиологии (обзор). 95 (4): 1717–1727. doi : 10.1152/jappl Physiol.00347.2003 . ПМИД 12970377 .
- ^ де Йонг Дж.К., Аттема Б.Дж., ван дер Хук, доктор медицинских наук, Вершурен Л., Касперс М.П., Климанн Р. и др. (август 2023 г.). «Половые различия в траектории старения скелетных мышц: те же процессы, но с разным рейтингом» . GeroScience (оригинальные исследования). 45 (4): 2367–2386. дои : 10.1007/s11357-023-00750-4 . ПМЦ 10651666 . ПМИД 36820956 .
- ^ Кауппила Т.Э., Кауппила Дж.Х., Ларссон Н.Г. (январь 2017 г.). «Митохондрии млекопитающих и старение: обновленная информация» . Клеточный метаболизм . 25 (1): 57–71. дои : 10.1016/j.cmet.2016.09.017 . ПМИД 28094012 . S2CID 21609241 .
- ^ Инсалата Ф., Хойцинг Х., Арьяман Дж., Джонс Н.С. (декабрь 2022 г.). «Стохастическое выживание самой плотной и клональной экспансии митохондриальной ДНК при старении» . Труды Национальной академии наук Соединенных Штатов Америки . 119 (49): e2122073119. Бибкод : 2022PNAS..11922073I . дои : 10.1073/pnas.2122073119 . ПМЦ 9894218 . ПМИД 36442091 .
- ^ Иразоки А., Мартинес-Висенте М., Апарисио П., Арис С., Алибахши Е., Рубио-Валера М. и др. (апрель 2022 г.). «Координация митохондриального и лизосомального гомеостаза смягчает воспаление и атрофию мышц при старении» . Стареющая клетка . 21 (4): e13583. дои : 10.1111/acel.13583 . ПМК 9009131 . ПМИД 35263007 .
- ^ Нарусэ М., Траппе С., Траппе Т.А. (апрель 2023 г.). «Специфическая атрофия скелетных мышц человека с возрастом: всесторонний обзор» . Журнал прикладной физиологии (оригинальные исследования). 134 (4): 900–914. doi : 10.1152/jappl Physiol.00768.2022 . ПМК 10069966 . ПМИД 36825643 .
- ^ де Йонг Дж.К., Касперс М.П., Вормс Н., Кейзер Н., Климанн Р., Менке А.Л. и др. (июнь 2024 г.). «Переносимость старения мышц мышей на человека: роль пола» . GeroScience (оригинальные исследования). 46 (3): 3341–3360. дои : 10.1007/s11357-024-01082-7 . ПМЦ 11009184 . ПМИД 38265577 .
- ^ Перейти обратно: а б Анкер С.Д., Морли Дж.Э., фон Хэлинг С. (декабрь 2016 г.). «Добро пожаловать в код саркопении МКБ-10» . Журнал кахексии, саркопении и мышц . 7 (5): 512–514. дои : 10.1002/jcsm.12147 . ПМК 5114626 . ПМИД 27891296 .
- ^ Перейти обратно: а б с д Аргилес Х.М., Кампос Н., Лопес-Педроса Х.М., Руэда Р., Родригес-Маньяс Л. (сентябрь 2016 г.). «Скелетные мышцы регулируют обмен веществ посредством межорганных перекрестных помех: роль в здоровье и заболеваниях» . Журнал Американской ассоциации медицинских директоров . 17 (9): 789–796. дои : 10.1016/j.jamda.2016.04.019 . ПМИД 27324808 .
- ^ Сайер А.А. (август 2010 г.). «Саркопения». БМЖ . 341 (10 2 августа): c4097. дои : 10.1136/bmj.c4097 . ПМИД 20699307 . S2CID 220113690 .
- ^ Мальмстрем Т.К., Миллер Д.К., Саймонсик Э.М., Ферруччи Л., Морли Дж.Е. (март 2016 г.). «SARC-F: оценка симптомов для прогнозирования лиц с саркопенией с риском плохих функциональных результатов» . Журнал кахексии, саркопении и мышц . 7 (1): 28–36. дои : 10.1002/jcsm.12048 . ПМЦ 4799853 . ПМИД 27066316 .
- ^ Пан Л., Се В., Фу Икс, Лу В., Цзинь Х., Лай Дж. и др. (октябрь 2021 г.). «Воспаление и саркопения: внимание к циркулирующим воспалительным цитокинам». Экспериментальная геронтология . 154 : 111544. doi : 10.1016/j.exger.2021.111544 . ПМИД 34478826 .
- ^ Шин М.Дж., Чон Ю.К., Ким И.Дж. (сентябрь 2018 г.). «Тестостерон и саркопения» . Всемирный журнал мужского здоровья . 36 (3): 192–198. дои : 10.5534/wjmh.180001 . ПМК 6119844 . ПМИД 29756416 .
- ^ Бартке А. (январь 2019 г.). «Гормон роста и старение: обновленный обзор» . Всемирный журнал мужского здоровья . 37 (1): 19–30. дои : 10.5534/wjmh.180018 . ПМК 6305861 . ПМИД 29756419 .
- ^ Кайсар Р., Карим А., Мухаммад Т., Шах I, Хан Дж (апрель 2021 г.). «Прогнозирование саркопении с использованием батареи циркулирующих биомаркеров» . Научные отчеты . 11 (1): 8632. doi : 10.1038/s41598-021-87974-6 . ПМК 8060253 . ПМИД 33883602 .
- ^ Адав СС, Ван Ю (апрель 2021 г.). «Метаболомные признаки старения: последние достижения» . Старение и болезни . 12 (2): 646–661. дои : 10.14336/AD.2020.0909 . ПМК 7990359 . ПМИД 33815888 .
- ^ Кальвани Р., Пикка А., Марини Ф., Бьянколильо А., Джервасони Дж., Персичилли С. и др. (ноябрь 2018 г.). «Особый характер циркулирующих аминокислот характеризует пожилых людей с физической слабостью и саркопенией: результаты исследования БИОСФЕРА» . Питательные вещества . 10 (11): 1691. дои : 10.3390/nu10111691 . ПМК 6265849 . ПМИД 30404172 .
- ^ Портал Д., Хофстеттер Л., Эшед И., Дан-Ланцман С., Селла Т., Урбан Д. и др. (1 апреля 2019 г.). «Индекс скелетных мышц L3 (L3SMI) является суррогатным маркером саркопении и слабости у пациентов с немелкоклеточным раком легких» . Управление раком и исследования . 11 : 2579–2588. дои : 10.2147/CMAR.S195869 . ПМК 6497853 . ПМИД 31114324 .
- ^ Шафрир А., Кац Л.Х., Шаули-Ахаронов М., Зингер А., Сафади Р., Стокар Дж. и др. (март 2024 г.). «Низкий уровень АЛТ связан с ВЗК и активностью заболевания: результаты общенационального исследования» . Журнал клинической медицины . 13 (7): 1869. doi : 10.3390/jcm13071869 . ПМЦ 11012492 . ПМИД 38610634 .
- ^ Сайер А.А. (ноябрь 2014 г.). «Саркопения – новый гериатрический гигант: время воплотить результаты исследований в клиническую практику» . Возраст и старение . 43 (6): 736–737. дои : 10.1093/старение/afu118 . ПМИД 25227204 .
- ^ Абате М., Ди Иорио А., Ди Ренцо Д., Паганелли Р., Сагини Р., Абате Дж. (сентябрь 2007 г.). «Слабость пожилых людей: физическое измерение» . Европа Медикофизика . 43 (3): 407–415. ПМИД 17117147 .
- ^ Ярашеский К.Е. (октябрь 2003 г.). «Упражнения, старение и метаболизм мышечного белка» . Журналы геронтологии. Серия А, Биологические и медицинские науки (обзор). 58 (10): М918–М922. дои : 10.1093/gerona/58.10.m918 . ПМИД 14570859 .
- ^ Лю CJ, Latham NK (июль 2009 г.). «Прогрессивная силовая тренировка с отягощениями для улучшения физических функций у пожилых людей» . Кокрановская база данных систематических обзоров . 2009 (3): CD002759. дои : 10.1002/14651858.cd002759.pub2 . ПМЦ 4324332 . ПМИД 19588334 .
- ^ Валенсуэла П.Л., Кастильо-Гарсия А., Моралес Х.С., Искьердо М., Серра-Рексак Х.А., Сантос-Лозано А. и др. (сентябрь 2019 г.). Терджунг Р. (ред.). «Физические упражнения в пожилом возрасте». Комплексная физиология . 9 (4) (1-е изд.). Уайли: 1281–1304 гг. дои : 10.1002/cphy.c190002 . ISBN 978-0-470-65071-4 . ПМИД 31688965 .
- ^ Фрагала М.С., Кадоре Э.Л., Дорго С., Искьердо М., Кремер В.Дж., Петерсон М.Д. и др. (август 2019 г.). «Тренировки с отягощениями для пожилых людей: заявление о позиции Национальной ассоциации силовой и физической подготовки». Журнал исследований силы и физической подготовки . 33 (8): 2019–2052. doi : 10.1519/JSC.0000000000003230 . ПМИД 31343601 .
- ^
 В эту статью включен текст , доступный по лицензии CC BY 4.0 . Беттс Дж.Г., Дезе П., Джонсон Э., Джонсон Дж.Е., Корол О., Круз Д. и др. (8 июня 2023 г.). Анатомия и физиология . Хьюстон: OpenStax CNX. 10.6. Упражнения и мышечная работоспособность. ISBN 978-1-947172-04-3 .
В эту статью включен текст , доступный по лицензии CC BY 4.0 . Беттс Дж.Г., Дезе П., Джонсон Э., Джонсон Дж.Е., Корол О., Круз Д. и др. (8 июня 2023 г.). Анатомия и физиология . Хьюстон: OpenStax CNX. 10.6. Упражнения и мышечная работоспособность. ISBN 978-1-947172-04-3 . - ^ Перейти обратно: а б с Филлипс С.М. (июль 2015 г.). «Пищевые добавки в поддержку упражнений с отягощениями для борьбы с возрастной саркопенией» . Достижения в области питания . 6 (4): 452–460. дои : 10.3945/ан.115.008367 . ПМЦ 4496741 . ПМИД 26178029 .
- ^ Перейти обратно: а б с д Сакума К., Ямагути А (28 мая 2012 г.). «Саркопения и возрастная эндокринная функция» . Международный журнал эндокринологии . 2012 : 127362. doi : 10.1155/2012/127362 . ПМЦ 3368374 . ПМИД 22690213 .
- ^ Перейти обратно: а б Вакабаяши Х., Сакума К. (май 2014 г.). «Комплексный подход к лечению саркопении». Современная клиническая фармакология . 9 (2): 171–180. дои : 10.2174/1574884708666131111192845 . ПМИД 24219006 .
- ^ Финкл В.Д., Гренландия С., Риджуэй Г.К., Адамс Дж.Л., Фраско М.А., Кук М.Б. и др. (29 января 2014 г.). «Повышенный риск несмертельного инфаркта миокарда после назначения терапии тестостероном у мужчин» . ПЛОС ОДИН . 9 (1): е85805. Бибкод : 2014PLoSO...985805F . дои : 10.1371/journal.pone.0085805 . ПМЦ 3905977 . ПМИД 24489673 .
- ^ Виген Р., О'Доннелл С.И., Барон А.Е., Грюнвальд Г.К., Мэддокс Т.М., Брэдли С.М. и др. (ноябрь 2013 г.). «Связь терапии тестостероном со смертностью, инфарктом миокарда и инсультом у мужчин с низким уровнем тестостерона». ДЖАМА . 310 (17): 1829–1836. дои : 10.1001/jama.2013.280386 . ПМИД 24193080 .
- ^ Басария С., Ковьелло А.Д., Трэвисон Т.Г., Сторер Т.В., Фарвелл В.Р., Джетт А.М. и др. (июль 2010 г.). «Нежелательные явления, связанные с приемом тестостерона» . Медицинский журнал Новой Англии . 363 (2): 109–122. дои : 10.1056/NEJMoa1000485 . ПМК 3440621 . ПМИД 20592293 .
- ^ Робинсон С.М., Реджинстер Дж.Й., Риццоли Р., Шоу С.К., Канис Дж.А., Баутманс И. и др. (август 2018 г.). «Играет ли питание роль в профилактике и лечении саркопении?» . Клиническое питание . 37 (4): 1121–1132. дои : 10.1016/j.clnu.2017.08.016 . ПМК 5796643 . ПМИД 28927897 .
- ^ Бауэр Дж., Биоло Дж., Седерхольм Т., Чезари М., Круз-Джентофт А.Дж., Морли Дж.Э. и др. (август 2013 г.). «Обоснованные фактические данные рекомендации по оптимальному потреблению белка в рационе пожилых людей: позиционный документ исследовательской группы PROT-AGE» . Журнал Американской ассоциации медицинских директоров . 14 (8): 542–559. дои : 10.1016/j.jamda.2013.05.021 . ПМИД 23867520 .
- ^ Дойц Н.Е., Бауэр Дж.М., Бараццони Р., Биоло Г., Бойри И., Боси-Вестфаль А. и др. (декабрь 2014 г.). «Потребление белка и физические упражнения для оптимальной мышечной функции при старении: рекомендации экспертной группы ESPEN» . Клиническое питание . 33 (6): 929–936. дои : 10.1016/j.clnu.2014.04.007 . ПМК 4208946 . ПМИД 24814383 .
- ^ Тессье А.Ж., Шевалье С. (август 2018 г.). «Обновленная информация о белке, лейцине, жирных кислотах омега-3 и витамине D в профилактике и лечении саркопении и функционального упадка» . Питательные вещества . 10 (8): 1099. дои : 10.3390/nu10081099 . ПМК 6116139 . ПМИД 30115829 .
- ^ Фудзита С., Вольпи Е (январь 2006 г.). «Аминокислоты и потеря мышечной массы с возрастом» . Журнал питания . 136 (1 доп.): 277S–280S. дои : 10.1093/jn/136.1.277S . ПМК 3183816 . ПМИД 16365098 .
- ^ Brioche T, Pagano AF, Py G, Chopard A (август 2016 г.). «Мышечное истощение и старение: экспериментальные модели, жировые инфильтраты и профилактика» (PDF) . Молекулярные аспекты медицины . 50 : 56–87. дои : 10.1016/j.mam.2016.04.006 . ПМИД 27106402 . S2CID 29717535 .
- ^ Перейти обратно: а б У Х, Ся Ю, Цзян Дж, Ду Х, Го X, Лю X и др. (сентябрь 2015 г.). «Влияние добавок бета-гидрокси-бета-метилбутирата на потерю мышечной массы у пожилых людей: систематический обзор и метаанализ». Архив геронтологии и гериатрии . 61 (2): 168–175. дои : 10.1016/j.archger.2015.06.020 . ПМИД 26169182 .
- ^ Голечек М. (август 2017 г.). «Добавка бета-гидрокси-бета-метилбутирата и скелетные мышцы в здоровых условиях и в условиях истощения мышц» . Журнал кахексии, саркопении и мышц . 8 (4): 529–541. дои : 10.1002/jcsm.12208 . ПМЦ 5566641 . ПМИД 28493406 .
- ^ Ся Л., Чжао Р., Ван Ц, Ву Ю, Чжоу Ю, Ван Ю и др. (ноябрь 2020 г.). «Саркопения и неблагоприятные последствия для здоровья: общий обзор метаанализа обсервационных исследований» . Раковая медицина . 9 (21): 7964–7978. дои : 10.1002/cam4.3428 . ПМЦ 7643685 . ПМИД 32924316 .
- ^ Родригеш Ф., Домингуш К., Монтейру Д., Мороусу П. (январь 2022 г.). «Обзор старения, саркопении, падений и тренировок с отягощениями у пожилых людей, проживающих в сообществе» . Международный журнал экологических исследований и общественного здравоохранения . 19 (2): 874. doi : 10.3390/ijerph19020874 . ПМЦ 8775372 . ПМИД 35055695 .
- ^ Сэйер А.А., Робинсон С.М., Патель Х.П., Шавлакадзе Т., Купер С., Граундс MD (март 2013 г.). «Новые горизонты патогенеза, диагностики и лечения саркопении» . Возраст и старение . 42 (2): 145–150. doi : 10.1093/ageing/afs191 . ПМЦ 3575121 . ПМИД 23315797 .
- ^ Роллан Ю., Дрей С., Веллас Б., Баррето П.С. (декабрь 2023 г.). «Современные и исследуемые препараты для лечения саркопении». Метаболизм . 149 : 155597. doi : 10.1016/j.metabol.2023.155597 . ПМИД 37348598 . S2CID 259232987 .
- ^ Фонсека Г.В., Дворацек Э., Эбнер Н., Фон Хэлинг С. (август 2020 г.). «Селективные модуляторы андрогенных рецепторов (SARM) как фармакологическое лечение атрофии мышц в текущих клинических испытаниях». Экспертное заключение об исследуемых препаратах . 29 (8): 881–891. дои : 10.1080/13543784.2020.1777275 . ПМИД 32476495 . S2CID 219174372 .
- ^ Кристиансен А.Р., Липшульц Л.И., Хоталинг Ю.М., Пастушак А.В. (март 2020 г.). «Селективные модуляторы андрогенных рецепторов: будущее андрогенной терапии?» . Трансляционная андрология и урология . 9 (Приложение 2): S135–S148. дои : 10.21037/tau.2019.11.02 . ПМК 7108998 . ПМИД 32257854 .
Дальнейшее чтение
[ редактировать ]- Фудзита С., Вольпи Е (январь 2006 г.). «Аминокислоты и потеря мышечной массы с возрастом» . Журнал питания (обзор). 136 (1 доп.): 277S–280S. дои : 10.1093/jn/136.1.277S . ПМК 3183816 . ПМИД 16365098 .
- Рубенофф Р. (декабрь 2007 г.). «Физическая активность, воспаление и потеря мышечной массы». Обзоры питания . 65 (12, часть 2): S208–S212. дои : 10.1111/j.1753-4887.2007.tb00364.x . ПМИД 18240550 .
- Шарло К., Тыганов С.А., Томиловская Е, Попов Д.В., Савеко А.А., Шенкман Б.С. (декабрь 2021 г.). «Влияние различных состояний бездействия мышц и меры противодействия на молекулярную передачу сигналов в мышцах» . Международный журнал молекулярных наук . 23 (1): 468. doi : 10.3390/ijms23010468 . ПМЦ 8745071 . ПМИД 35008893 .