Эйкозапентаеновая кислота
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК (5 Z ,8 Z ,11 Z ,14 Z ,17 Z )-икоза-5,8,11,14,17-пентаеновая кислота | |
| Другие имена (5 Z ,8 Z ,11 Z ,14 Z ,17 Z )-5,8,11,14,17-эйкозапентаеновая кислота | |
| Идентификаторы | |
3D model ( JSmol ) | |
| 3DMeet | |
| 1714433 | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.117.069 |
| КЕГГ | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 20 Н 30 О 2 | |
| Молярная масса | 302.451 g/mol |
| Опасности | |
| СГС Маркировка : | |
 | |
| Опасность | |
| H314 | |
| P260 , P264 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P321 , P363 , P405 , P501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
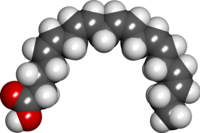
Эйкозапентаеновая кислота ( EPA ; также икозапентаеновая кислота ) представляет собой жирную кислоту омега-3 . В физиологической литературе ему присвоено название 20:5(n-3). Она также имеет тривиальное название тимнодоновая кислота . По химической структуре ЭПК представляет собой карбоновую кислоту с 20- углеродной цепью и пятью двойными цис -связями ; первая двойная связь расположена у третьего углерода от омега-конца.
ЭПК представляет собой полиненасыщенную жирную кислоту (ПНЖК), которая действует как предшественник простагландина-3 (который ингибирует агрегацию тромбоцитов ), тромбоксана-3 и лейкотриена-5 эйкозаноидов . ЭПК является одновременно предшественником и продуктом гидролитического распада эйкозапентаеноилэтаноламида (ЭПЭА: C 22 H 35 NO 2 ; 20:5,n-3). [1] Хотя исследования добавок рыбьего жира , которые содержат как докозагексаеновую кислоту (DHA), так и EPA, не подтвердили заявления о предотвращении сердечных приступов или инсультов . [2] [3] [4] Недавнее многолетнее исследование Vascepa ( этилэйкозапентаеноат ) , этиловый эфир свободной жирной кислоты , отпускаемого по рецепту препарата, содержащего только ЭПК, показало снижение сердечного приступа, инсульта и смертности от сердечно-сосудистых заболеваний на 25% по сравнению с плацебо у этих пациентов. при статин-резистентной гипертриглицеридемии. [5] [6]
Источники
[ редактировать ]ЭПК поступает в рацион человека при употреблении жирной рыбы , например, печени трески , сельди , скумбрии , лосося , менхадена и сардины , различных видов съедобных водорослей или при приеме дополнительных форм рыбьего жира или масла водорослей. Он также содержится в грудном молоке человека .
Рыбы, как и большинство позвоночных, могут синтезировать очень мало ЭПК из пищевой альфа-линоленовой кислоты (АЛК). [7] Из-за чрезвычайно низкой степени конверсии рыбы получают его в основном из водорослей . потребляемых ими [8] Он доступен для человека из некоторых источников неживотного происхождения (например, из Yarrowia lipolytica , [9] и из микроводорослей, таких как Nannochromis oculata , Monodus subterraneus , Chlorella minutissima и Phaeodactylum tricornutum , [10] [11] которые разрабатываются как коммерческий источник). [12] ЭПК обычно не обнаруживается в высших растениях, но в следовых количествах она обнаружена в портулаке . [13] В 2013 году сообщалось, что генетически модифицированная форма растения рыжика производит значительное количество ЭПК. [14] [15]
Организм человека преобразует часть поглощенной альфа-линоленовой кислоты (АЛК) в ЭПК. АЛК сама по себе является незаменимой жирной кислотой, и людям необходимо ее достаточное количество. Однако эффективность преобразования АЛК в ЭПК намного ниже, чем абсорбция ЭПК из содержащей ее пищи. Поскольку ЭПК также является предшественником докозагексаеновой кислоты (ДГК), обеспечить достаточный уровень ЭПК в рационе, не содержащем ни ЭПК, ни ДГК, труднее как из-за дополнительной метаболической работы, необходимой для синтеза ЭПК, так и из-за использования ЭПК для метаболизма в ДГК. Медицинские состояния, такие как диабет или некоторые аллергии, могут значительно ограничивать способность человеческого организма метаболизировать ЭПК из АЛК.
Формы
[ редактировать ]Коммерчески доступные пищевые добавки чаще всего производятся из рыбьего жира и обычно поставляются в форме триглицеридов, этиловых эфиров или фосфолипидов ЭПК. Среди производителей добавок ведутся споры об относительных преимуществах и недостатках различных форм. Было показано, что одна форма, обнаруженная в природе в водорослях, форма полярного липида, имеет улучшенную биодоступность по сравнению с формой этилового эфира или триглицерида. [16] было обнаружено, что DHA или EPA в форме лизофосфатидилхолина (LPC) более эффективны, чем триглицерид и фосфатидилхолины (PC). Аналогичным образом, в исследовании 2020 года [17]
| База | Агентство по охране окружающей среды |
|---|---|
| Этиловый эфир | Этиловый эфир Агентства по охране окружающей среды (EPA) |
| Лизофосфатидилхолин (LPC или лизоPC) | LPC-EPA или лизоPC-EPA |
| Фосфатидилхолин (ПК) | EPA-ПК |
| Фосфолипид (PL) | Агентство по охране окружающей среды-PL |
| Триглицерид (ТГ) или триацилглицерин (ТАГ) | EPA-TG или EPA-TAG |
| Реэтерифицированный триглицерид (rTG) или реэтерифицированный триацилглицерин (rTAG) | EPA ртг или р-ТАГ |
Биосинтез
[ редактировать ]Аэробный путь эукариот
[ редактировать ]
Аэробные эукариоты, в частности микроводоросли, мхи , грибы и большинство животных (включая человека), осуществляют биосинтез ЭПК обычно в виде серии реакций десатурации и элонгазы, катализируемых последовательным действием ферментов десатуразы и элонгазы . Этот путь, первоначально выявленный у Thraustochytrium , применим к следующим группам: [18]
- десатурация шестого атома углерода альфа-линоленовой кислоты с помощью Δ6-десатуразы с образованием стеаридоновой кислоты (SDA, 18:4 ω-3),
- элонгация стеаридоновой кислоты элонгазой Δ6 с образованием эйкозатетраеновой кислоты (ЭТА, 20:4 ω-3),
- десатурация пятого атома углерода эйкозатетраеновой кислоты с помощью Δ5-десатуразы с образованием эйкозапентаеновой кислоты (EPA, 20:5 ω-3),
Поликетидсинтазный путь
[ редактировать ]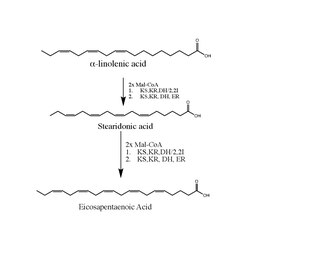
Морские бактерии и микроводоросли Schizochytrium используют анаэробный путь поликетидсинтазы (PKS) для синтеза DHA. [18] Путь PKS включает шесть ферментов, а именно: 3-кетоацилсинтаза (KS), 2-кетоацил -АПБ -редуктаза (KR), дегидраза (DH), еноилредуктаза (ER), дегидратаза/2-транс-3-коз-изомераза (DH/2). ,3I), дегидратаза/2-транс и 2-цис-изомераза (DH/2,2I). Биосинтез ЭПК варьируется у морских видов, но большая часть способности морских видов превращать ПНЖК C18 в ДЦ-ПНЖК зависит от ферментов жирноацилдесатуразы и элонгазы. Молекулярная основа ферментов будет определять, где в полученной молекуле образуется двойная связь. [19]
Предлагаемый путь синтеза поликетидов ЭПК у Shewanella (морской бактерии) представляет собой повторяющуюся реакцию восстановления, дегидратации и конденсации, в которой в качестве строительных блоков используются ацетил-КоА и малонил-КоА. Механизм превращения α-линоленовой кислоты в ЭПК включает конденсацию малонил-КоА в уже существующую α-линоленовую кислоту под действием KS. Полученная структура преобразуется НАДФН-зависимой редуктазой, KR, с образованием промежуточного продукта, который дегидратируется ферментом DH. Последним этапом является НАДФН-зависимое восстановление двойной связи в транс-2-еноил-АСР посредством активности фермента ER. Процесс повторяется для образования EPA. [20]
Клиническое значение
[ редактировать ]
США В MedlinePlus Национального института здравоохранения перечислены заболевания, при которых EPA (отдельно или в сочетании с другими источниками ω-3) считается эффективным средством лечения. [21] Большинство из них связано с его способностью снижать воспаление .
Для достижения значительного (> 15%) снижения триглицеридов обычно требуется прием больших доз (от 2,0 до 4,0 г/день) длинноцепочечных жирных кислот омега-3 в виде рецептурных лекарств или пищевых добавок, и в этих дозах эффекты могут быть выражены. значительная (от 20% до 35% и даже до 45% у лиц с уровнем выше 500 мг/дл).
Диетические добавки, содержащие ЭПК и ДГК, снижают уровень триглицеридов дозозависимым образом; однако DHA, по-видимому, повышает уровень липопротеинов низкой плотности (вариант, который вызывает атеросклероз, иногда неточно называемый «плохим холестерином») и уровень холестерина ЛПНП (измерение/оценка массы холестерина в частицах ЛПНП), а ЭПК этого не делает. Этот эффект был замечен в нескольких мета-анализах , которые объединили сотни отдельных клинических исследований, в которых как ЭПК, так и ДГК были частью добавки с высокими дозами омега-3, но разницу можно увидеть только тогда, когда ЭПК и ДГК назначаются отдельно. четко. [22] [23] Например, в исследовании Шефера и его коллег из Медицинской школы Тафтса пациентам давали либо 600 мг/день только ДГК, 600 или 1800 мг/день только ЭПК или плацебо в течение шести недель. В группе, принимавшей DHA, наблюдалось значительное снижение уровня триглицеридов на 20% и увеличение уровня LDL-C на 18%, но в группах, принимавших EPA, умеренное снижение уровня триглицеридов не считалось статистически значимым, и никаких изменений уровней LDL-C не было обнаружено ни при одной дозе. [24]
Обычные потребители обычно получают ЭПК и ДГК из таких продуктов, как жирная рыба, [а] пищевые добавки с рыбьим жиром, [б] и реже из с маслом водорослей добавок [с] в которых дозы омега-3 ниже, чем в клинических экспериментах. Продольное исследование Центра Купера, в котором приняли участие 9253 здоровых мужчин и женщин в течение 10 лет, показало, что у тех, кто принимал добавки с рыбьим жиром, не наблюдалось повышения уровня холестерина ЛПНП. [25] Фактически, наблюдалось очень незначительное снижение уровня холестерина ЛПНП, которое было статистически значимым, но слишком небольшим, чтобы иметь какое-либо клиническое значение. Эти люди принимали добавки с рыбьим жиром по своему выбору, и следует признать, что количества и соотношения EPA и DHA варьируются в зависимости от источника рыбьего жира.
Жирные кислоты омега-3, особенно ЭПК, изучались на предмет их влияния на расстройства аутистического спектра (РАС). Некоторые предполагают, что, поскольку уровень жирных кислот омега-3 у детей с аутизмом может быть низким, прием добавок может привести к улучшению симптомов. В то время как некоторые неконтролируемые исследования сообщили об улучшении, хорошо контролируемые исследования не показали статистически значимого улучшения симптомов в результате приема высоких доз омега-3. [26] [27]
Кроме того, исследования показали, что жирные кислоты омега-3 могут быть полезны при лечении депрессии . [28] [29]
ЭПК и ДГК Этиловые эфиры (все формы) могут хуже всасываться и, следовательно, действовать хуже, если их принимать натощак или с нежирной пищей. [30]
Примечания
[ редактировать ]- ^ Приготовленный лосось содержит 500–1500 мг DHA и 300–1000 мг EPA на 100 граммов рыбы. См. страницу: Лосось в пищу .
- ^ В пищевых добавках с маслом омега-3 нет стандартных доз, и обычно в лососевом масле больше DHA, чем EPA, в то время как в других видах белой рыбы больше EPA, чем DHA. Один производитель, Trident Food's Pure Alaska , например, сообщает о 220 мг DHA и 180 мг EPA на порцию лососевого масла (общее содержание омега-3 = 600 мг), а в рыбьем жире минтая 144 мг и 356 мг EPA (общее содержание омега-3) 3 = 530 мг). Аналогичные продукты от другого производителя, Fish Oils, Puritan's Pride , сообщают о 180 мг DHA и 150 мг EPA для продукта из лососевого масла (общее содержание омега-3 = 420 мг), но 204 мг DHA и 318 мг EPA для рыбьего жира, полученного из анчоусов. сардина и скумбрия (всего омега-3 = 600 мг). Только в целях информации и сравнения, никакие одобрения не подразумеваются.
- ^ Многие растительные источники омега-3 богаты АЛК, но полностью лишены ЭПК и ДГК. Исключением являются масла, полученные из водорослей. Поскольку существует больше коммерческих источников DHA из водорослей, чем из EPA, добавки из водорослей омега-3 обычно содержат больше DHA, чем EPA. Например, Nordic Naturals сообщает о 390 мг DHA и 195 мг EPA на порцию (общее количество омега-3 = 715 мг), Calgee сообщает о 300 мг DHA и 150 мг EPA (общее количество омега-3 = 550 мг) и так далее, а iwi сообщает ЭПК 250 мг (всего омега-3 = 254 мг). Только в целях информации и сравнения, никаких одобрений не подразумевается.
Ссылки
[ редактировать ]- ^ Луканик М., Хелд Дж.М., Вантипалли М.К., Кланг И.М., Грэм Дж.Б., Гибсон Б.В., Литгоу Г.Дж., Гилл М.С. (май 2011 г.). «Передача сигналов N-ацилэтаноламина опосредует влияние диеты на продолжительность жизни Caenorhabditis elegans» . Природа . 473 (7346): 226–9. Бибкод : 2011Natur.473..226L . дои : 10.1038/nature10007 . ПМК 3093655 . ПМИД 21562563 .
- ^ Циммер С (17 сентября 2015 г.). «Исследование инуитов вносит изюминку в историю здоровья жирных кислот омега-3» . Нью-Йорк Таймс . Архивировано из оригинала 9 января 2019 года . Проверено 11 октября 2015 г.
- ^ О'Коннор А. (30 марта 2015 г.). «Заявления о рыбьем жире не подтверждены исследованиями» . Нью-Йорк Таймс . Архивировано из оригинала 28 мая 2018 года . Проверено 11 октября 2015 г.
- ^ Грей А., Болланд М. (март 2014 г.). «Доказательства клинических испытаний и использование добавок с рыбьим жиром» . JAMA Внутренняя медицина . 174 (3): 460–2. doi : 10.1001/jamainternmed.2013.12765 . ПМИД 24352849 . Архивировано из оригинала 8 июня 2016 г. Проверено 12 октября 2015 г.
- ^ Бхатт Д.Л., Стег П.Г., Миллер М., Бринтон Э.А., Джейкобсон Т.А., Кетчам С.Б., Дойл Р.Т., Джулиано Р.А., Цзяо Л., Грановиц С., Тардиф Дж.К., Баллантайн СМ (3 января 2019 г.). «Снижение сердечно-сосудистого риска с помощью икосапент-этила при гипертриглицеридемии» . Медицинский журнал Новой Англии . 380 (1): 11–22. дои : 10.1056/NEJMoa1812792 . ПМИД 30415628 .
- ^ «Васкепа® (икозапент этил) снижает на 26% ключевую вторичную комбинированную конечную точку сердечно-сосудистой смерти, сердечных приступов и инсульта, продемонстрированную в REDUCE-IT™» . 10 ноября 2018 года. Архивировано из оригинала 23 мая 2019 года . Проверено 21 января 2019 г.
- ^ Комитет по потребностям рыбы и креветок в питательных веществах; Национальный исследовательский совет (2011). Потребность рыбы и креветок в питательных веществах . Вашингтон, округ Колумбия: Издательство национальных академий. ISBN 978-0-309-16338-5 .
- ^ Бишоп-Уэстон Ю. «Растительные источники веганской и вегетарианской докозагексаеновой кислоты – DHA и эйкозапентаеновой кислоты, EPA и незаменимых жиров» . Архивировано из оригинала 22 мая 2013 г. Проверено 5 августа 2008 г.
- ^ Се, Дунмин; Джексон, Этель Н.; Чжу, Куинн (февраль 2015 г.). «Устойчивый источник эйкозапентаеновой кислоты омега-3 из метаболически модифицированной Yarrowia lipolytica: от фундаментальных исследований до коммерческого производства» . Прикладная микробиология и биотехнология . 99 (4): 1599–1610. дои : 10.1007/s00253-014-6318-y . ISSN 0175-7598 . ПМЦ 4322222 . ПМИД 25567511 .
- ^ Важаппилли Р., Чен Ф (1998). «Потенциал микроводорослей по производству эйкозапентаеновой кислоты и докозагексаеновой кислоты и их гетеротрофный рост». Журнал Американского общества нефтехимиков . 75 (3): 393–397. дои : 10.1007/s11746-998-0057-0 . S2CID 46917269 .
- ^ Ратха С.К., Прасанна Р. (февраль 2012 г.). «Биоразведка микроводорослей как потенциальный источник «зеленой энергии» — проблемы и перспективы». Прикладная биохимия и микробиология . 48 (2): 109–125. дои : 10.1134/S000368381202010X . ПМИД 22586907 . S2CID 18430041 .
- ^ Холлидей Дж. (12 января 2007 г.). «Water 4 представляет водоросли DHA/EPA в качестве пищевого ингредиента» . Архивировано из оригинала 16 января 2007 г. Проверено 9 февраля 2007 г.
- ^ Симопулос АП (2002). «Жирные кислоты Омега-3 в дикорастущих растениях, орехах и семенах» (PDF) . Азиатско-Тихоокеанский журнал клинического питания . 11 (Приложение 2): С163–73. дои : 10.1046/j.1440-6047.11.s.6.5.x . Архивировано из оригинала (PDF) 17 декабря 2008 г.
- ^ Руис-Лопес Н., Хаслам Р.П., Напье Х.А., Саянова О. (январь 2014 г.). «Успешное накопление высокого уровня длинноцепочечных полиненасыщенных жирных кислот омега-3 рыбьего жира в трансгенных масличных культурах» . Заводской журнал . 77 (2): 198–208. дои : 10.1111/tpj.12378 . ПМЦ 4253037 . ПМИД 24308505 .
- ^ Коглан А. (4 января 2014 г.). «Спроектированное растение выделяет жизненно важный рыбий жир» . Новый учёный . 221 (2950): 12. дои : 10.1016/s0262-4079(14)60016-6 . Архивировано из оригинала 1 июня 2015 года . Проверено 26 августа 2017 г.
- ^ Каган, ML; Уэст, Алабама; Занте, К.; Колдер, ПК (2013). «Острое появление жирных кислот в плазме человека - сравнительное исследование богатого полярными липидами масла из микроводорослей Nannochromis oculata и масла криля у здоровых молодых мужчин» . Липиды в здоровье и болезни . 12 :102. дои : 10.1186/1476-511X-12-102 . ПМЦ 3718725 . ПМИД 23855409 .
- ^ Сугасини, Д; Красный, ПЦР; Гоггин, А; Тай, LM; Суббайя, ПВ (декабрь 2019 г.). «Обогащение мозговой докозагексаеновой кислоты (DHA) сильно зависит от молекулярного носителя пищевой DHA: лизофосфатидилхолин более эффективен, чем фосфатидилхолин или триацилглицерин» . Журнал пищевой биохимии . 74 : 108231 дои : 10.1016/jnutbio.2019.108231 . ПМЦ 6885117 . ПМИД 31665653 .
- ^ Перейти обратно: а б Цю, Сяо (01 февраля 2003 г.). «Биосинтез докозагексаеновой кислоты (DHA, 22:6-4, 7,10,13,16,19): два разных пути». Простагландины, лейкотриены и незаменимые жирные кислоты . 68 (2): 181–186. дои : 10.1016/S0952-3278(02)00268-5 . ISSN 0952-3278 . ПМИД 12538082 .
- ^ Монройг, Оскар; Точер, Дуглас; Наварро, Хуан (21 октября 2013 г.). «Биосинтез полиненасыщенных жирных кислот у морских беспозвоночных: последние достижения в области молекулярных механизмов» . Морские наркотики . 11 (10): 3998–4018. дои : 10.3390/md11103998 . ПМЦ 3826146 . ПМИД 24152561 .
- ^ Мои, Ибрагим Муса; Леу, Адам Теан Чор; Али, Мохд Шукури Мохамад; Рахман, Раджа Нур Залиха Раджа Абд.; Саллех, Абу Бакар; Сабри, Суриана (июль 2018 г.). «Полиненасыщенные жирные кислоты в морских бактериях и стратегии увеличения их производства» . Прикладная микробиология и биотехнология . 102 (14): 5811–5826. дои : 10.1007/s00253-018-9063-9 . ПМИД 29749565 . S2CID 13680225 .
- ^ НИЗ Медлайн Плюс. «MedlinePlus Herbs and Supplements: жирные кислоты омега-3, рыбий жир, альфа-линоленовая кислота» . Архивировано из оригинала 8 февраля 2006 года . Проверено 14 февраля 2006 г.
- ^ АбуМвейс, С; Еврей, С; Тайем, Р; Аграиб, Л. (февраль 2018 г.). «Добавки, содержащие эйкозапентаеновую кислоту и докозагексаеновую кислоту, модулируют факторы риска сердечно-сосудистых заболеваний: метаанализ рандомизированных плацебо-контролируемых клинических исследований на людях» . Журнал человеческого питания и диетологии . 31 (1): 67–84. дои : 10.1111/jhn.12493 . ПМИД 28675488 . S2CID 8793334 .
- ^ Чен, Х; Дэн, Г; Чжоу, Q; Чу, X; Су, М; Вэй, Ю; Ли, Л; Чжан, Z (26 марта 2020 г.). «Влияние эйкозапентаеновой кислоты и докозагексаеновой кислоты по сравнению с добавками α-линоленовой кислоты на кардиометаболические факторы риска: метаанализ рандомизированных контролируемых исследований». Еда и функции . 11 (3): 1919–1932. дои : 10.1039/c9fo03052b . ПМИД 32175534 . S2CID 212730542 .
- ^ Асталос, ИБ; Глисон, Дж.А.; Север, С; Гедик, Р; Асталос, Б.Ф.; Хорват, КВ; Дансингер, ML; Ламон-Фава, С; Шефер, Э.Дж. (ноябрь 2016 г.). «Влияние эйкозапентаеновой кислоты и докозагексаеновой кислоты на факторы риска сердечно-сосудистых заболеваний: рандомизированное клиническое исследование». Метаболизм: клинический и экспериментальный . 65 (11): 1636–1645. дои : 10.1016/j.metabol.2016.07.010 . ПМИД 27733252 .
- ^ Харрис, WS; Леонард, Д; Рэдфорд, Северная Каролина; Барлоу, CE; Стил, MR; Фаррелл, Юго-Запад; Павлович, А; Уиллис, БЛ; ДеФина, LF (январь 2021 г.). «Увеличение уровня DHA в эритроцитах не связано с увеличением уровня холестерина ЛПНП: продольное исследование Центра Купера». Журнал клинической липидологии . 15 (1): 212–217. doi : 10.1016/j.jacl.2020.11.011 . ПМИД 33339757 . S2CID 229325648 .
- ^ Бент С., Бертольо К., Хендрен Р.Л. (август 2009 г.). «Жирные кислоты омега-3 при расстройствах аутистического спектра: систематический обзор» . Журнал аутизма и нарушений развития . 39 (8): 1145–54. дои : 10.1007/s10803-009-0724-5 . ПМК 2710498 . ПМИД 19333748 .
- ^ Манкад Д., Дюпюи А., Смайл С., Робертс В., Брайан Дж., Луи Т., Дженор Л., Заглул Д., Ябони А., Маркон П.М., Анагносту Э (21 марта 2015 г.). «Рандомизированное плацебо-контролируемое исследование жирных кислот омега-3 при лечении маленьких детей с аутизмом» . Молекулярный аутизм . 6:18 . дои : 10.1186/s13229-015-0010-7 . ПМЦ 4367852 . ПМИД 25798215 .
- ^ Фриман, Марлен П.; Хиббельн, Джозеф Р.; Виснер, Кэтрин Л.; Дэвис, Джон М.; Мишулон, Дэвид; Пит, Малькольм; Кек, Пол Э.; Марангелл, Лорен Б.; Ричардсон, Александра Дж.; Лейк, Джеймс; Столл, Эндрю Л. (декабрь 2006 г.). «Жирные кислоты омега-3: доказательная база для лечения и будущие исследования в психиатрии» . Журнал клинической психиатрии . 67 (12): 1954–1967. дои : 10.4088/jcp.v67n1217 . ISSN 1555-2101 . ПМИД 17194275 . Архивировано из оригинала 20 сентября 2020 г. Проверено 13 октября 2022 г.
- ^ Иларди, Стивен (28 апреля 2015 г.). «Терапевтическое изменение образа жизни. Новое лечение депрессии» . Терапевтическое изменение образа жизни (TLC) . Архивировано из оригинала 9 ноября 2019 года . Проверено 9 ноября 2019 г.
Мы никогда не были созданы для сидячего, замкнутого, лишенного сна, социально изолированного, перегруженного фаст-фудом и безумного ритма современной жизни.
- ^ Джейкобсон Т.А., Маки К.С., Орринджер С.Э., Джонс П.Х., Крис-Этертон П., Сиканд Дж., Ла Форж Р., Дэниелс С.Р., Уилсон Д.П., Моррис П.Б., Уайлд Р.А., Гранди С.М., Давиглус М., Фердинанд К.К., Виджаярагаван К., Дидвания ПК , Аберг Дж.А., Ляо К.П., Маккенни Дж.М., Росс Дж.Л., Браун Л.Т., Ито М.К., Бэйс Х.Э., Браун В.В., Андерберг Дж.А. (2015). «Рекомендации Национальной липидной ассоциации по лечению дислипидемии, ориентированному на пациента: Часть 2» . Журнал клинической липидологии . 9 (6 Приложение): S1–122.e1. дои : 10.1016/j.jacl.2015.09.002 . ПМИД 26699442 .
Внешние ссылки
[ редактировать ]- EPA связана с белками в PDB
- Эйкозапентаеноилэтаноламид ; Анандамид (20:5, n-3); ЭПЭА. - ПабХим