Взаимодействие незаменимых жирных кислот
Эта статья требует внимания эксперта в области биологии . Добавьте в этот шаблон причину или параметр обсуждения , чтобы объяснить проблему со статьей. ( декабрь 2022 г. ) |

В природе существует большое разнообразие жирных кислот . Два класса жирных кислот считаются незаменимыми: жирные кислоты омега-3 и омега-6 . Незаменимые жирные кислоты необходимы человеку, но не могут синтезироваться организмом и поэтому должны поступать с пищей. Омега-3 и омега-6 используются в некоторых клеточных сигнальных путях и участвуют в опосредовании воспаления , синтеза белка и метаболических путей в организме человека.
Арахидоновая кислота (АК) представляет собой 20-углеродную незаменимую жирную кислоту омега-6. [1] Он находится во главе «каскада арахидоновой кислоты», который инициирует 20 различных сигнальных путей , которые контролируют широкий спектр биологических функций, включая воспаление , рост клеток и центральную нервную систему . [2] [3] Большая часть АК в организме человека образуется из пищевой линолевой кислоты (18:2 ω-6), которая содержится в орехах , семенах , растительных маслах и животных жирах . [4] [5] [6]
Другие незаменимые жирные кислоты, поступающие с пищей, участвуют в передаче воспалительных сигналов и могут противодействовать воздействию каскада арахидоновой кислоты. Например, ЭПК (20:5 ω-3) конкурирует с АК и поступает с жирной рыбой , маслом водорослей или альфа-линоленовой кислотой (полученной из грецких орехов , конопляного масла и льняного масла). Другим примером является DGLA (20:3 ω-6) , полученная из пищевой GLA (18:3 ω-6) , которая содержится в масле огуречника и также может его использовать. Эти два параллельных каскада смягчают воспалительное действие специфических эйкозаноидов , полученных из АК.
В рационе людей столетней давности было гораздо меньше ω-3, чем в рационе первых охотников-собирателей , и он вызывал гораздо меньше загрязнения, чем современный рацион. [7] что вызывает воспалительную реакцию. Мы также можем посмотреть на соотношение ω-3 и ω-6 в сравнении с их рационом. Эти изменения сопровождаются увеличением заболеваемости многими заболеваниями — так называемыми болезнями цивилизации , — которые связаны с воспалительными процессами. Теперь есть очень убедительные доказательства [8] что некоторые из этих заболеваний можно улучшить за счет увеличения потребления ω-3. Есть также более предварительные данные, показывающие, что диетический ω-3 может облегчить симптомы некоторых психических расстройств. [9]
Номенклатура серий эйкозаноидов
[ редактировать ]Эйкозаноиды — это сигнальные молекулы, полученные из незаменимых жирных кислот (НЖК). Они являются основным путем действия НЖК в организме. Существует четыре класса эйкозаноидов и две или три серии внутри каждого класса.
Плазматические мембраны клеток жирнокислотных содержат фосфолипиды , состоящие из гидрофильной фосфатной головки и двух гидрофобных хвостов . незаменимые жирные кислоты с 20 атомами углерода Некоторые из этих жирных кислот представляют собой полиненасыщенные (АК, ЭПК или ДГЛК). [ нужна ссылка ] В ответ на различные воспалительные сигналы эти НЖК отщепляются от фосфолипида и высвобождаются в виде свободных жирных кислот. Затем НЖК насыщаются кислородом (любым из двух путей) и далее модифицируются, образуя эйкозаноиды. [ нужна ссылка ] Окисление циклооксигеназы (ЦОГ) удаляет две двойные связи C=C , что приводит к образованию серий TX , PG и PGI . Окисление липоксигеназы не удаляет двойные связи C=C и приводит к образованию LK . [10]
После окисления эйкозаноиды дополнительно модифицируются, образуя ряд . Члены ряда различаются буквой и нумеруются по числу двойных связей, которое не меняется внутри ряда. Например, действие циклооксигеназы на АК 2-го ряда. (с 4 двойными связями) приводит к образованию тромбоксанов [3] (TXA 2 , TXB 2 ... ), каждый с двумя двойными связями. Действие циклооксигеназы на ЭПК (с 5 двойными связями) приводит к образованию тромбоксанов третьего ряда (TXA 3 , TXB 3 и др.), каждый с тремя двойными связями. Есть исключения из этой закономерности, некоторые из которых указывают на стереохимию (PGF 2α ).
В таблице (1) показаны эти последовательности для AA (20:4 ω-6). Последовательности EPA (20:5 ω-3) и DGLA (20:3 ω-6) аналогичны.
| Диетический Незаменимые жирные кислоты | Аббревиатура | Формула атомы углерода: двойные связи ω | Серия продуктов эйкозаноидов | ||
|---|---|---|---|---|---|
| Техас PG ЗГУ | ЛК | Эффекты | |||
| Гамма-линоленовая кислота через дигомо-гамма-линоленовую кислоту | ГЛА ДГЛА | 18:3ч6 20:3ч6 | серия-1 | серия-3 | менее воспалительный |
| Арахидоновая кислота | АА | 20:4ч6 | серия-2 | серия-4 | более воспалительный |
| Эйкозапентаеновая кислота | Агентство по охране окружающей среды | 20:5х3 | серия-3 | серия-5 | менее воспалительный |
Все простаноиды представляют собой замещенные простаноевые кислоты .Страница «Простеноид» Киберлипид-центра [11] иллюстрирует исходное соединение и кольца, связанные с каждой буквой серии.
IUPAC IUBMB и икозаноид используют эквивалентный . термин [11]
Каскад арахидоновой кислоты при воспалении
[ редактировать ]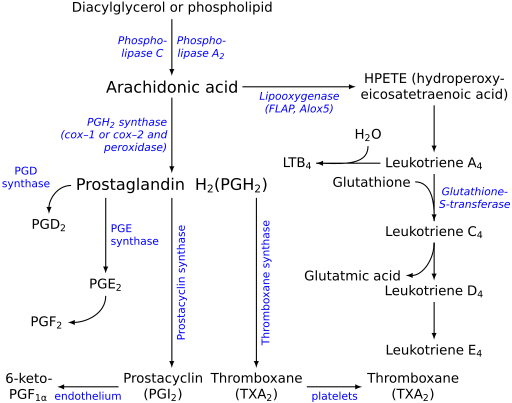
В каскаде арахидоновой кислоты пищевая линолевая кислота (18:2 ω-6) денасыщена и удлиняется с образованием арахидоновой кислоты (и других кислот омега-6), которая затем этерифицируется в фосфолипид в клеточной мембране . [12] Затем, в ответ на многие воспалительные раздражители , такие как загрязнение воздуха , курение , пассивное курение , гидрогенизированные растительные масла и другие экзогенные токсины, фосфолипаза генерируется , которая расщепляет этот фосфолипид, высвобождая АК в виде свободной жирной кислоты . [ нужна ссылка ] Затем АК можно насыщать кислородом, а затем модифицировать с образованием эйкозаноидов — аутокринных и паракринных агентов , которые связывают рецепторы на клетке или ее соседях, чтобы предупредить иммунную систему о повреждении клеток. Альтернативно, АК может диффундировать в ядро клетки и взаимодействовать с транскрипции , контролируя транскрипцию ДНК цитокинов факторами или других гормонов.
Механизмы действия эйкозаноида ω-3
[ редактировать ]
Было обнаружено, что эйкозаноиды из АК способствуют воспалению. Препараты из GLA ( через DGLA) и EPA, как правило, менее воспалительные, неактивные или противовоспалительные. (Это обобщение является обоснованным: эйкозаноиды могут быть провоспалительными в одной ткани и противовоспалительными в другой. ( См. обсуждение PGE 2 в Calder [13] или Тилли. [14] )
На рисунке 2 показаны цепочки синтеза ω-3 и -6, а также основные эйкозаноиды из АК, ЭПК и ДГЛК.
Диетические ω-3 и GLA противодействуют воспалительному эффекту эйкозаноидов АК тремя способами: вытеснением, конкурентным ингибированием и прямым противодействием.
Смещение
[ редактировать ]Диетический ω-3 снижает концентрацию АК в тканях.Исследования на животных показывают, что увеличение потребления ω-3 снижает содержание АК в мозге и других тканях. [15] Альфа -линоленовая кислота (18:3 ω-3) способствует вытеснению линолевой кислоты (18:2 ω-6) из ферментов элонгазы и десатуразы , которые производят АК. ЭПК ингибирует высвобождение АК фосфолипазой А2 из клеточной мембраны. [16] Другие механизмы, включающие транспорт НЖК, также могут играть роль.
Верно обратное: высокое содержание линолевой кислоты в рационе снижает преобразование в организме α-линоленовой кислоты в ЭПК. Однако эффект не такой сильный; десатураза имеет более высокое сродство к α-линоленовой кислоте, чем к линолевой кислоте. [17]
Конкурентное торможение
[ редактировать ]DGLA и EPA конкурируют с АК за доступ к ферментам циклооксигеназы и липоксигеназы. Таким образом, присутствие DGLA и EPA в тканях снижает выработку эйкозаноидов АК . Например, пищевая ГЛК увеличивает тканевую ДГЛК и снижает TXB2 . [18] [19] Аналогичным образом, EPA ингибирует выработку PG и TX серии-2. [13] Хотя DGLA не образует LT, производное DGLA блокирует трансформацию AA в LT. [20]
Противодействие
[ редактировать ]Некоторые эйкозаноиды, полученные из DGLA и EPA, противодействуют своим аналогам, полученным из AA. Например, DGLA дает PGE 1 , который мощно противодействует PGE 2 . [21] EPA производит антиагрегационный простациклин PGI 3. [22] . Он также дает лейкотриен LTB 5 полученного из АК , который нарушает действие LTB 4 , . [23]
Парадокс диетической ГЛК
[ редактировать ]Исследования показали, что пищевая окисленная линолевая кислота (LA, 18:2 ω-6) обладает воспалительными свойствами. В организме LA денасыщается с образованием GLA (18:3 ω-6), однако поступающая с пищей GLA обладает противовоспалительным действием. Некоторые наблюдения частично объясняют этот парадокс: ЛА конкурирует с α-линоленовой кислотой (АЛК, 18:3 ω-3) за Δ6-десатуразу и тем самым в конечном итоге ингибирует образование противовоспалительной ЭПК (20:5 ω-3). Напротив, GLA не конкурирует за Δ6-десатуразу. Продукт элонгации GLA, DGLA (20:3 ω-6), конкурирует с 20:4 ω-3 за Δ5-десатуразу, и можно было бы ожидать, что это вызовет воспалительную реакцию GLA, но это не так, возможно, потому, что этот шаг не Это не является определяющим фактором . Δ6-десатураза, по-видимому, действительно является стадией, лимитирующей скорость; 20:4 ω-3 незначительно накапливается в липидах организма.
DGLA ингибирует воспаление посредством как конкурентного ингибирования, так и прямого противодействия (см. выше ). Диетическая ГЛК приводит к резкому увеличению ДГЛК в мембранах лейкоцитов, тогда как ЛА этого не делает. Это может отражать недостаток десатуразы в лейкоцитах. Добавление пищевой ГЛК увеличивает уровень ДГЛК в сыворотке без увеличения содержания АК в сыворотке. [21] [24]
Вполне вероятно, что некоторые пищевые ГЛК в конечном итоге образуют АК и способствуют воспалению. Исследования на животных показывают, что эффект невелик. [19] Эмпирические наблюдения за фактическими эффектами ГЛК доказывают, что противовоспалительный эффект ДГЛК доминирует. [25]
Сложность путей
[ редактировать ]Сигнальные пути эйкозаноидов сложны.Поэтому трудно охарактеризовать действие какого-либо конкретного эйкозаноида.Например, PGE 2 связывает четыре рецептора, получивших название EP 1–4 .Каждый из них кодируется отдельным геном, а некоторые существуют в нескольких изоформах .Каждый рецептор EP, в свою очередь, соединяется с G-белком .EP 2 , EP 4 и одна изоформа EP 3 рецепторов соединяются с G s .Это увеличивает внутриклеточный цАМФ и оказывает противовоспалительное действие.EP 1 и другие изоформы EP 3 соединяются с G q .Это приводит к увеличению внутриклеточного кальция и является провоспалительным.Наконец, еще одна изоформа EP 3 соединяется с G i , что одновременно снижает уровень цАМФ и увеличивает содержание кальция.Многие клетки иммунной системы экспрессируют множество рецепторов, которые соединяют эти явно противоположные пути. [14] полученный из EPA, Предположительно, PGE 3, оказывает несколько иное влияние на эту систему, но оно недостаточно четко охарактеризовано.
Каскад арахидоновой кислоты в центральной нервной системе
[ редактировать ]Каскад арахидоновой кислоты, возможно, является самой сложной сигнальной системой, с которой приходится иметь дело нейробиологам.
Даниэле Пиомелли Арахидоновая кислота [3]
Несколько иначе протекает каскад арахидоновой кислоты в центральной нервной системе (ЦНС). Нейрогормоны , нейромодуляторы или нейротрансмиттеры действуют как первые мессенджеры. Они активируют фосфолипиды, высвобождая АК из мембран нейронных клеток в виде свободной жирной кислоты. [ нужна ссылка ] нейронов За свою короткую жизнь свободная АК может влиять на активность ионных каналов и протеинкиназ . Или он может метаболизироваться с образованием эйкозаноидов, эпоксиэйкозатриеновых кислот (ЭЕТ), нейропротектина D или различных эндоканнабиноидов ( анандамида и его аналогов).
Действия эйкозаноидов в мозге не так хорошо изучены, как при воспалении. Исследования показывают, что они действуют как вторичные мессенджеры внутри нейрона, возможно, контролируя пресинаптическое торможение и активацию протеинкиназы С. Они также действуют как паракринные медиаторы, действуя через синапсы на близлежащие клетки. Эффекты этих сигналов недостаточно изучены. (Piomelli, 2000) утверждает, что доступной информации мало.
Нейроны в ЦНС организованы как взаимосвязанные группы функционально связанных клеток (например, в сенсорных системах). Диффузионный фактор, высвобождаемый из нейрона в интерстициальную жидкость и способный взаимодействовать с мембранными рецепторами соседних клеток, в идеале мог бы использоваться для «синхронизации» активности ансамбля взаимосвязанных нервных клеток. Более того, во время развития и в определенных формах обучения постсинаптические клетки могут секретировать регуляторные факторы, которые диффундируют обратно к пресинаптическому компоненту, определяя его выживание в качестве активного терминала, амплитуду его прорастания и эффективность в секреции нейротрансмиттеров — явление, известное как ретроградное регулирование. Исследования показали, что метаболиты арахидоновой кислоты участвуют в ретроградной передаче сигналов и других формах локальной модуляции активности нейронов.
| Каскад арахидоновой кислоты | ||
|---|---|---|
| При воспалении | В мозгу | |
| Основное влияние на | Воспаление в тканях | Возбудимость нейронов |
| АА выпущен из | Белые кровяные тельца | Нейроны |
| Триггеры для выпуска AA | Воспалительные раздражители | Нейромедиаторы, нейрогормоны и нейромодуляторы |
| Внутриклеточное воздействие на | Транскрипция ДНК цитокинов и других медиаторы воспаления | Активность ионных каналов и белка киназы |
| Метаболизируется с образованием | Эйкозаноиды, резольвины, изофураны, изопростаны, липоксины, эпоксиэйкозатриеновые кислоты (ЭЭТ) | Эйкозаноиды, нейропротектин D, EET и некоторые эндоканнабиноиды |
Каскады EPA и DGLA также присутствуют в мозге, и были обнаружены их эйкозаноидные метаболиты. Влияние каскадов EPA и DGLA на психические и нервные процессы изучено не так хорошо, как их влияние на воспаление.
Дальнейшее обсуждение
[ редактировать ]На рисунке 2 показаны два пути от ЭПК к ДГК , включая исключительный шунт Спречера .
5-LO действует при пятом углероде карбоксильной группы .Другие липоксигеназы — 8-LO, 12-LO и 15-LO — продуцируют другие эйкозаноидные продукты. , активирующий ядерную мембрану Для своего действия 5-LO использует белок 5-липоксигеназу ( FLAP ), сначала с гидропероксиэйкозатетраеновой кислотой ( HPETE ), а затем с первым лейкотриеном, LTA.
См. также
[ редактировать ]- Незаменимая жирная кислота
- Омега-3 жирные кислоты
- Омега-6 жирные кислоты
- Соотношение жирных кислот в продуктах питания
- Эйкозаноид
- Докозаноид
Ссылки
[ редактировать ]- ^ Куннейн СК (ноябрь 2003 г.). «Проблемы с незаменимыми жирными кислотами: время для новой парадигмы?». Прогресс в исследованиях липидов . 42 (6): 544–568. дои : 10.1016/S0163-7827(03)00038-9 . ПМИД 14559071 .
- ^ де Мело Рейс Р.А., Исаак А.Р., Фрейтас Х.Р., де Алмейда М.М., Шук П.Ф., Феррейра Г.К. и др. (2021). «Качество жизни и надзорная эндоканнабиноидная система» . Границы в неврологии . 15 : 747229. дои : 10.3389/fnins.2021.747229 . ПМЦ 8581450 . ПМИД 34776851 .
- ^ Jump up to: а б с Пиомелли, Даниэле (2000). «Арахидоновая кислота» . Нейропсихофармакология: пятое поколение прогресса . Архивировано из оригинала 15 июля 2006 г. Проверено 3 марта 2006 г.
- ^ Фрейтас ХР (25 августа 2017 г.). «Хлорелла обыкновенная как источник незаменимых жирных кислот и микроэлементов: краткий комментарий». Открытый научный журнал о растениях . 10 (1): 92–99. doi : 10.2174/1874294701710010092 (неактивен 24 апреля 2024 г.). ISSN 1874-2947 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка ) - ^ Фрейтас Х.Р., Исаак А.Р., Малчер-Лопес Р., Диас Б.Л., Тревензоли И.Х., Де Мело Рейс Р.А. (декабрь 2018 г.). «Полиненасыщенные жирные кислоты и эндоканнабиноиды в здоровье и болезни». Пищевая неврология . 21 (10): 695–714. дои : 10.1080/1028415X.2017.1347373 . ПМИД 28686542 . S2CID 40659630 .
- ^ Фрейтас ХР, Феррейра Г.Д., Тревензоли И.Х., Оливейра К.Дж., де Мело Рейс Р.А. (ноябрь 2017 г.). «Жирные кислоты, антиоксиданты и физическая активность при старении мозга» . Питательные вещества . 9 (11): 1263. дои : 10.3390/nu9111263 . ПМК 5707735 . ПМИД 29156608 .
- ^ Симопулос А (2001). «Эволюционные аспекты диеты и незаменимых жирных кислот». Жирные кислоты и липиды – новые открытия (PDF) . Мировой обзор питания и диетологии. Том. 88. стр. 18–27. дои : 10.1159/000059742 . ISBN 978-3-8055-7182-1 . ПМИД 11935953 . Архивировано из оригинала (PDF) 26 сентября 2006 г.
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Национальный институт здравоохранения (01 августа 2005 г.). «Омега-3 жирные кислоты, рыбий жир, альфа-линоленовая кислота» . Архивировано из оригинала 8 февраля 2006 года . Проверено 21 августа 2010 г.
- ^ Де Катерина Р., Баста Г (2001). «n-3 жирные кислоты и воспалительная реакция — биологическая основа» . Дополнения к Европейскому кардиологическому журналу . 3 (приложение D): D42–D49. дои : 10.1016/S1520-765X(01)90118-X .
- ^ Киберлипидный центр. «Полиеновые жирные кислоты» . Архивировано из оригинала 30 сентября 2018 года . Проверено 11 февраля 2006 г.
- ^ Jump up to: а б Киберлипидный центр. «Простаноиды» . Архивировано из оригинала 8 февраля 2007 года . Проверено 11 февраля 2006 г.
- ^ Уилан Дж., Фриче К. (май 2013 г.). «Линолевая кислота» . Достижения в области питания . 4 (3): 311–312. дои : 10.3945/ан.113.003772 . ПМК 3650500 . ПМИД 23674797 .
- ^ Jump up to: а б Колдер, Филип К. (сентябрь 2004 г.). «Жирные кислоты n-3 и воспаление – новые повороты в старой сказке» . Архивировано из оригинала 16 марта 2006 года . Проверено 8 февраля 2006 г.
- Приглашенная обзорная статья, Информационный бюллетень PUFA.
- ^ Jump up to: а б Тилли С.Л., Коффман Т.М., Коллер Б.Х. (июль 2001 г.). «Смешанные сообщения: модуляция воспаления и иммунных реакций простагландинами и тромбоксанами» . Журнал клинических исследований . 108 (1): 15–23. дои : 10.1172/JCI13416 . ПМК 209346 . ПМИД 11435451 .
- ^ Новости медицинских исследований (25 мая 2005 г.). «Уровень жирных кислот в мозге связан с депрессией» . Проверено 10 февраля 2006 г.
- Которые, в свою очередь, цитировали Грин П., Гиспан-Херман И., Ядид Г. (июнь 2005 г.). «Повышенная концентрация арахидоновой кислоты в мозгу крыс Flinders Sensitive Line, животной модели депрессии» . Журнал исследований липидов . 46 (6): 1093–1096. doi : 10.1194/jlr.C500003-JLR200 . ПМИД 15805551 .
- ^ КП Су; С.Ю. Хуан; СС Чиу; WW Шен (2003). «Омега-3 жирные кислоты при большом депрессивном расстройстве. Предварительное двойное слепое плацебо-контролируемое исследование?» (PDF) . Архивировано из оригинала (PDF) 8 февраля 2005 г. Проверено 22 февраля 2006 г.
- ^ Финни С.Д., Один Р.С., Джонсон С.Б., Холман Р.Т. (март 1990 г.). «Понижение содержания арахидоната в сывороточных фосфолипидах и эфирах холестерина, связанное с вегетарианской диетой у людей» . Американский журнал клинического питания . 51 (3): 385–392. дои : 10.1093/ajcn/51.3.385 . ПМИД 2106775 . Архивировано из оригинала 12 февраля 2007 года . Проверено 11 февраля 2006 г.
- «[Д]иетарная арахидоновая кислота обогащает свой циркулирующий пул в организме человека; однако 20:5n-3 не реагирует аналогичным образом на диетические ограничения».
- ^ Гивернау М., Меза Н., Барха П., Роман О. (ноябрь 1994 г.). «Клиническое и экспериментальное исследование долгосрочного воздействия пищевой гамма-линоленовой кислоты на липиды плазмы, агрегацию тромбоцитов, образование тромбоксана и выработку простациклина». Простагландины, лейкотриены и незаменимые жирные кислоты . 51 (5): 311–316. дои : 10.1016/0952-3278(94)90002-7 . ПМИД 7846101 .
- ГЛК снижает уровень триглицеридов, ЛПНП, повышает ЛПВП, снижает TXB 2 и другие маркеры воспаления. Обзорная статья; исследования на людях и крысах.
- ^ Jump up to: а б Карлстад, доктор медицинских наук, ДеМишель С.Дж., Литем В.Д., Петерсон М.Б. (ноябрь 1993 г.). «Влияние внутривенных липидных эмульсий, обогащенных гамма-линоленовой кислотой, на жирные кислоты n-6 плазмы и биосинтез простагландинов после ожогов и повреждений эндотоксином у крыс». Медицина критических состояний . 21 (11): 1740–1749. дои : 10.1097/00003246-199311000-00025 . ПМИД 8222692 . S2CID 36538810 .
- IV Прием гамма-линоленовой кислоты увеличивал уровень GLA в сыворотке, но не увеличивал содержание арахидоновой кислоты в плазме (исследование на крысах), снижал TXB 2 .
- ^ Белч Джей Джей, Хилл А (январь 2000 г.). «Масло вечерней примулы и масло огуречника при ревматологических заболеваниях» . Американский журнал клинического питания . 71 (1 доп.): 352S–356S. дои : 10.1093/ajcn/71.1.352s . ПМИД 10617996 .
- «Сама по себе DGLA не может быть преобразована в LT, но может образовывать 15-гидроксильное производное, которое блокирует трансформацию арахидоновой кислоты в LT. Увеличение потребления DGLA может позволить DGLA действовать как конкурентный ингибитор PG 2-й серии и LT 4-й серии и, таким образом, подавлять воспаление».
- ^ Jump up to: а б Фан Ю.Ю., Чапкин Р.С. (сентябрь 1998 г.). «Значение пищевой гамма-линоленовой кислоты для здоровья и питания человека» . Журнал питания . 128 (9): 1411–1414. дои : 10.1093/jn/128.9.1411 . ПМИД 9732298 .
- «[D]Пищевая ГЛК увеличивает содержание своего продукта элонгазы, дигомо-гамма-линоленовой кислоты (ДГЛК), в клеточных мембранах без сопутствующих изменений в арахидоновой кислоте (АК). Впоследствии, при стимуляции, ДГЛК может быть преобразована воспалительными клетками в 15 -(S)-гидрокси-8,11,13-эйкозатриеновая кислота и простагландин Е1. Это примечательно, поскольку эти соединения обладают как противовоспалительными, так и антипролиферативными свойствами».
- ^ Фишер С., Вебер ПК (сентябрь 1985 г.). «Тромбоксан (TX)A3 и простагландин (PG)I3 образуются у человека после приема с пищей эйкозапентаеновой кислоты: идентификация и количественное определение методом капиллярной газовой хроматографии-электронно-ударной масс-спектрометрии». Биомедицинская масс-спектрометрия . 12 (9): 470–476. дои : 10.1002/bms.1200120905 . ПМИД 2996649 .
- ^ Прескотт С.М. (июнь 1984 г.). «Влияние эйкозапентаеновой кислоты на продукцию лейкотриена B нейтрофилами человека» . Журнал биологической химии . 259 (12): 7615–7621. дои : 10.1016/S0021-9258(17)42835-3 . ПМИД 6330066 .
- ^ Джонсон М.М., Свон Д.Д., Суретт М.Э., Стегнер Дж., Чилтон Т., Фонтех А.Н., Чилтон Ф.Х. (август 1997 г.). «Пищевые добавки с гамма-линоленовой кислотой изменяют содержание жирных кислот и выработку эйкозаноидов у здоровых людей» . Журнал питания . 127 (8): 1435–1444. дои : 10.1093/jn/127.8.1435 . ПМИД 9237935 .
- ^ Стоун К.Дж., Уиллис А.Л., Харт В.М., Киртланд С.Дж., Кернофф П.Б., Макникол Г.П. (февраль 1979 г.). «Метаболизм дигомо-гамма-линоленовой кислоты у человека». Липиды . 14 (2): 174–180. дои : 10.1007/BF02533869 . ПМИД 423720 . S2CID 41372225 .