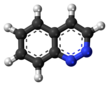
Циннолин

| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Циннолин [ 1 ] | |||
| Другие имена
Бензопиридазин
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.005.423 | ||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 8 Ч 6 Н 2 | |||
| Молярная масса | 130.150 g·mol −1 | ||
| Температура плавления | 39 ° С (102 ° F; 312 К) | ||
| Кислотность ( pKa ) | 2.64 [ 2 ] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Циннолин представляет собой ароматическое гетероциклическое соединение формулы C 8 H 6 N 2 . Он изомерен другим нафтиридинам, включая хиноксалин , фталазин и хиназолин .
Характеристики
[ редактировать ]Свободное основание можно получить в виде масла обработкой гидрохлорида основанием . Он сокристаллизуется с одной молекулой эфира в виде белых шелковистых иголок (т.пл. 24–25 °C) при охлаждении эфирных растворов. Свободное основание плавится при 39°С. По вкусу напоминает хлоралгидрат и на некоторое время оставляет резкое раздражение.
Открытие и синтез
[ редактировать ]Соединение было впервые получено в нечистой форме циклизацией алкина о - C 6 H 4 (NH 2 )C≡CCO 2 H в воде с образованием 4-гидроксициннолин-3-карбоновой кислоты. Этот материал можно декарбоксилировать и восстановить гидроксильную группу с образованием исходного гетероцикла. Эта реакция называется синтезом циннолина Рихтера . [ 3 ] Существуют усовершенствованные методы его синтеза. получить дегидрированием дигидроциннолина свежеосажденной . окисью ртути Его можно Его можно выделить в виде гидрохлорида . [ 4 ]
Циннолины – производные циннолина. Классической органической реакцией синтеза циннолинов является синтез Видмана-Штермера . [ 5 ] реакция замыкания цикла α-виниланилина с соляной кислотой и нитритом натрия :

Нитрит натрия сначала превращается в азотистую кислоту , которая затем образует электрофильный промежуточный триоксид азота . Следующим промежуточным соединением является стабильный нитрозамин , который теряет воду с образованием соли диазония , которая затем реагирует с винильной группой на стадии замыкания кольца. Концептуально связанной реакцией является синтез триазина Бамбергера с образованием триазинов.
Другой метод циннолина — синтез циннолина Борше .
Безопасность
[ редактировать ]Циннолин токсичен. [ нужна ссылка ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 212. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ Браун, Х.К., и др., Бауде, Э.А. и Наход, Ф.К., Определение органических структур физическими методами , Academic Press, Нью-Йорк, 1955.
- ^ Виктор фон Рихтер (1883). «О производных циннолина» . Химические отчеты . 16 :677-683. дои : 10.1002/cber.188301601154 .
- ^ Паррик, Дж.; Шоу, CJG; Мехта, Л.К. (2000). «Пиридазины, циннолины, бензоциннолины и фталазины». Химия углеродных соединений Родда . Том. 4 (2-е изд.). стр. 1–69.
- ^ Брэдфорд П. Манди; Майкл Г. Эллерд; Фрэнк Дж. Младший Фавалоро (2005). Назовите реакции и реагенты в органическом синтезе . ISBN 0-471-22854-0 .