Циклическое соединение
Циклическое соединение (или кольцевое соединение ) — это термин для соединения в области химии , в котором один или несколько рядов атомов соединения соединены с образованием кольца . Кольца могут различаться по размеру от трех до многих атомов и включают примеры, когда все атомы являются углеродом (т. е. являются карбоциклами ), ни один из атомов не является углеродом (неорганические циклические соединения) или где присутствуют как углеродные, так и неуглеродные атомы. ( гетероциклические соединения , кольца которых содержат как углерод, так и неуглерод). В зависимости от размера кольца, порядка связи отдельных звеньев между атомами кольца и их расположения внутри колец карбоциклические и гетероциклические соединения могут быть ароматическими или неароматическим; в последнем случае они могут варьироваться от полностью насыщенных до различного количества кратных связей между атомами кольца. Из-за огромного разнообразия, допускаемого в сочетании с валентностью общих атомов и их способностью образовывать кольца, число возможных циклических структур даже небольшого размера (например, <17 атомов) исчисляется многими миллиардами.
- Примеры циклических соединений: полностью углеродные (карбоциклические) и более сложные природные циклические соединения.
-
Ингенол , сложный терпеноидный природный продукт , родственный, но более простой, чем следующий за ним паклитаксел , который имеет сложную кольцевую структуру, включающую 3-, 5- и 7-членные неароматические карбоциклические кольца.
-
Циклоалканы , простейшие карбоциклы, в том числе циклопропан , циклобутан , циклопентан и циклогексан . Обратите внимание: в других местах используется сокращение из органической химии , где предполагается, что атомы водорода присутствуют для заполнения валентности углерода 4 (вместо того, чтобы они были показаны явно).
-
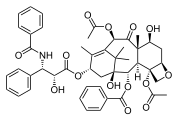
Паклитаксел растительного происхождения , еще один сложный терпеноид , также природный продукт, имеющий сложную многокольцевую структуру, включающую 4-, 6- и 8-членные кольца (карбоциклические и гетероциклические, ароматические и неароматические).
В дополнение к их сложности и количеству замыкание атомов в кольца может блокировать отдельные атомы с четким замещением ( функциональными группами ), так что в результате получается стереохимия и хиральность соединения, включая некоторые проявления, уникальные для колец (например, конфигурационные изомеры ). Кроме того, в зависимости от размера кольца трехмерные формы конкретных циклических структур – обычно колец из пяти атомов и больше – могут варьироваться и взаимопревращаться, так что конформационная изомерия проявляется . Действительно, развитие этой важной химической концепции исторически возникло в связи с циклическими соединениями. Наконец, циклические соединения из-за уникальной формы, реакционной способности, свойств и биологической активности , которые они порождают, составляют большинство всех молекул, участвующих в биохимии, структуре и функциях живых организмов , а также в искусственных молекулах, таких как лекарства, пестициды и т.д.
Структура и классификация
[ редактировать ]Циклическое соединение или кольцевое соединение — это соединение , в котором по крайней мере некоторые его атомы соединены с образованием кольца. [1] Кольца различаются по размеру от трех до многих десятков и даже сотен атомов. Примеры кольцевых соединений легко включают случаи, когда:
- все атомы — углеродные (т. е. являются карбоциклами ),
- ни один из атомов не является углеродом (неорганические циклические соединения), [2] или где
- присутствуют как углеродные, так и неуглеродные атомы ( гетероциклические соединения с кольцами, содержащими как углерод, так и неуглерод).
Общие атомы могут (в зависимости от их валентности ) образовывать различное количество связей, и многие общие атомы легко образуют кольца. Кроме того, в зависимости от размера кольца, порядка связи отдельных звеньев между атомами кольца и их расположения внутри колец циклические соединения могут быть ароматическими или неароматическим; в случае неароматических циклических соединений они могут варьироваться от полностью насыщенных до имеющих различное количество кратных связей. Вследствие конституционной изменчивости, которая термодинамически возможна в циклических структурах, число возможных циклических структур даже небольшого размера (например, <17 атомов) исчисляется многими миллиардами. [3]
Более того, замыкание атомов в кольца может зафиксировать определенную функциональную группу – замещенные атомы на месте, в результате чего стереохимия и хиральность с соединением связаны , включая некоторые проявления, уникальные для колец (например, конфигурационные изомеры ); [4] Кроме того, в зависимости от размера кольца трехмерные формы конкретных циклических структур — обычно колец из пяти атомов и больше — могут варьироваться и взаимопревращаться, так что конформационная изомерия . проявляется [4]
Карбоциклы
[ редактировать ]Подавляющее большинство циклических соединений являются органическими , и из них значительная и концептуально важная часть состоит из колец, состоящих только из атомов углерода (т. е. они являются карбоциклами). [ нужна ссылка ]
Неорганические циклические соединения
[ редактировать ]Неорганические атомы также образуют циклические соединения. Примеры включают серу и азот (например, имид гептасеры). S 7 NH , тритиазилтрихлорид (NSCl) 3 , тетранитрид тетрасеры S 4 N 4 ), кремний (например, циклопентасилан (SiH 2 ) 5 ), фосфор и азот (например, гексахлорфосфазен (NPCl 2 ) 3 ), фосфор и кислород (например, метафосфаты (PO − 3 ) 3 и другие производные циклической фосфорной кислоты ), бор и кислород (например, метаборат натрия Na 3 (BO 2 ) 3 , бура ), бор и азот (например, боразин (БН 3Н6 ) . ) [ нужна ссылка ] Когда углерод в бензоле «замещается» другими элементами, например, как в борабензоле , силабензоле , германабензоле , оловобензоле и фосфорине , ароматичность сохраняется, и поэтому ароматические неорганические циклические соединения также известны и хорошо охарактеризованы. [ нужна ссылка ]
Гетероциклические соединения
[ редактировать ]Гетероциклическое соединение представляет собой циклическое соединение, которое имеет атомы по меньшей мере двух разных элементов в качестве членов своего кольца(ов). [5] Циклические соединения, в которых присутствуют как углеродные, так и неуглеродные атомы, являются гетероциклическими углеродными соединениями, и это название относится также к неорганическим циклическим соединениям (например, силоксанам только кремний и кислород , которые содержат в кольцах , и боразинам , которые содержат только бор и азот в кольцах). [5] Номенклатура Ханча-Видмана рекомендована ИЮПАК для обозначения гетероциклов, но многие общие названия по-прежнему используются регулярно. [ нужна ссылка ]
Макроциклы
[ редактировать ]
Термин макроцикл используется для соединений, имеющих кольца из 8 или более атомов. [6] [7] Макроциклы могут быть полностью карбоциклическими (кольца содержат только атомы углерода, например циклооктан ), гетероциклическими, содержащими как углеродные, так и неуглеродные атомы (например, лактоны и лактамы, содержащие кольца из 8 или более атомов), или неуглеродными (содержащими только неуглеродные атомы). в кольцах, например гексасульфид диселена ). Гетероциклы с углеродом в кольцах могут иметь ограниченное количество неуглеродных атомов в своих кольцах (например, в лактонах и лактамах, кольца которых богаты углеродом, но имеют ограниченное количество неуглеродных атомов) или быть богаты неуглеродными атомами и иметь значительная симметрия (например, в случае хелатирующих макроциклов). Макроциклы могут иметь доступ к ряду стабильных конформаций , предпочитая находиться в конформациях, которые минимизируют трансаннулярные несвязанные взаимодействия внутри кольца (например, при этом стул и стул-лодочка более стабильны, чем конформация лодка-лодка для циклооктана , из-за изображенных взаимодействий). по показанным дугам). [ нужна ссылка ] Средние кольца (8–11 атомов) являются наиболее напряженными, с энергией деформации 9–13 (ккал/моль), и анализ факторов, важных для конформаций более крупных макроциклов, можно смоделировать с использованием конформаций среднего кольца. [8] Конформационный анализ нечетных колец предполагает, что они имеют тенденцию существовать в менее симметричных формах с меньшими различиями в энергии между стабильными конформациями. [9]

Номенклатура
[ редактировать ]Номенклатура ИЮПАК содержит обширные правила, охватывающие наименование циклических структур, как основных структур, так и заместителей, присоединенных к алициклическим структурам. [ нужна ссылка ] Термин макроцикл используется, когда кольцо, содержащее соединение, имеет кольцо из 12 или более атомов. [6] [7] Термин полициклический используется, когда в одной молекуле присутствует более одного кольца. Нафталин формально является полициклическим соединением, но более конкретно его называют бициклическим соединением. Несколько примеров макроциклических и полициклических структур приведены в последней галерее ниже.
Атомы, входящие в состав кольцевой структуры, называются кольцевыми атомами. [10]
Изомерия
[ редактировать ]Стереохимия
[ редактировать ]Замыкание атомов в кольца может блокировать отдельные атомы с четким замещением функциональными группами, так что в результате возникает стереохимия и хиральность соединения, включая некоторые проявления, уникальные для колец (например, конфигурационные изомеры ). [4]
Конформационная изомерия
[ редактировать ]В зависимости от размера кольца трехмерные формы определенных циклических структур - обычно колец из 5 атомов и более - могут варьироваться и взаимно преобразовываться, так что конформационная изомерия . проявляется [4] Действительно, развитие этой важной химической концепции исторически возникло в связи с циклическими соединениями. Например, циклогексаны — шестичленные карбоциклы без двойных связей, к которым могут быть присоединены различные заместители, см. изображение — демонстрируют равновесие между двумя конформациями, стулом и лодочкой, как показано на изображении.
Конформация кресла является предпочтительной конфигурацией, поскольку в этой конформации стерическая деформация , затмевающая деформация и угловая деформация , которые в противном случае возможны, сведены к минимуму. [4] Какая из возможных конформаций стула преобладает в циклогексанах, несущих один или несколько заместителей, зависит от заместителей и того, где они расположены в кольце; как правило, «объемные» заместители - группы с большими объемами или группы, которые в противном случае отталкиваются в своих взаимодействиях. [ нужна ссылка ] — предпочитают занимать экваториальное положение. [4] Примером взаимодействий внутри молекулы, которые могут привести к стерическому напряжению , приводящему к сдвигу равновесия от лодки к стулу, является взаимодействие между двумя метильными группами в цис -1,4-диметилциклогексане. В этой молекуле две метильные группы находятся в противоположных положениях кольца (1,4-), и их цис -стереохимия смещает обе эти группы к одной и той же стороне кольца. Следовательно, если эти метильные группы вынуждены принять форму лодки с более высокой энергией, они находятся в стерическом контакте, отталкивают друг друга и смещают равновесие в сторону конформации кресла. [4]
Ароматность
[ редактировать ] этой статьи История редактирования не полная. Часть истории редактирования текста статьи существует в Aromaticity из-за копирования и вставки между статьями. Это может быть нарушением CC BY-SA и/или GFDL , если в сводке редактирования или на странице обсуждения не было указано правильное указание авторства. |
Циклические соединения могут проявлять или не проявлять ароматичность ; бензол является примером ароматического циклического соединения, а циклогексан является неароматическим. В органической химии термин ароматичность используется для описания циклической (кольцеобразной) плоской (плоской) молекулы, которая демонстрирует необычайную стабильность по сравнению с другими геометрическими или соединительными расположениями того же набора атомов. Из-за их стабильности очень трудно заставить ароматические молекулы распасться и вступить в реакцию с другими веществами. Органические соединения, не являющиеся ароматическими, относятся к алифатическим соединениям — они могут быть циклическими, но особой стабильностью (низкой реакционной способностью) обладают только ароматические кольца.
Поскольку одна из наиболее часто встречающихся ароматических систем соединений в органической химии основана на производных прототипного ароматического соединения бензола (ароматического углеводорода, распространенного в нефти и ее дистиллятах), слово «ароматический» иногда используется для неофициального обозначения производных бензола. , и именно так оно было впервые определено. Тем не менее, существует множество небензольных ароматических соединений. Например, в живых организмах наиболее распространенными ароматическими кольцами являются основания с двойным кольцом в РНК и ДНК. Функциональная группа или другой ароматический заместитель называется арильной группой.
Самое раннее использование термина «ароматический» было в статье Августа Вильгельма Хофмана в 1855 году. Хофманн использовал этот термин для обозначения класса бензольных соединений, многие из которых действительно имеют запахи (ароматы), в отличие от чистых насыщенных углеводородов. Сегодня не существует общей связи между ароматичностью как химическим свойством и обонятельными свойствами таких соединений (то, как они пахнут), хотя в 1855 году, до того, как была понята структура бензола или органических соединений, такие химики, как Гофман, начали понимать, что пахучие вещества Молекулы растений, такие как терпены, имели химические свойства, которые, как мы сегодня знаем, аналогичны ненасыщенным нефтяным углеводородам, таким как бензол.
С точки зрения электронной природы молекулы ароматичность описывает сопряженную систему, часто состоящую из чередующихся одинарных и двойных связей в кольце. Эта конфигурация позволяет электронам в пи-системе молекулы делокализоваться вокруг кольца, увеличивая стабильность молекулы. Молекула не может быть представлена одной структурой, а скорее представляет собой резонансный гибрид разных структур, например, с двумя резонансными структурами бензола. Эти молекулы нельзя найти ни в одном из этих представлений: с более длинными одинарными связями в одном месте и более короткими двойными связями в другом (см. Теорию ниже). Скорее, молекула имеет длину связей между одинарными и двойными связями. Эта широко распространенная модель ароматических колец, а именно идея о том, что бензол образуется из шестичленного углеродного кольца с чередующимися одинарными и двойными связями (циклогексатриен), была развита Августом Кекуле (см. раздел «История» ниже). Модель бензола состоит из двух резонансных форм, что соответствует наложению двойных и одинарных связей с образованием шести полуторных связей. Бензол — более стабильная молекула, чем можно было бы ожидать без учета делокализации заряда. [ нужна ссылка ]
Основное использование
[ редактировать ]Из-за уникальной формы, реакционной способности, свойств и биологической активности , которую они порождают, циклические соединения составляют подавляющее большинство всех молекул, участвующих в биохимии, структуре и функциях живых организмов , а также в искусственных молекулах (например, лекарствах, гербициды и т. д.), с помощью которых человек пытается осуществлять контроль над природой и биологическими системами.
Синтетические реакции
[ редактировать ]Важные общие реакции образования колец
[ редактировать ]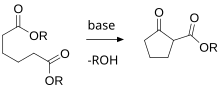
Существует множество специализированных реакций, в которых используется исключительно образование колец, и они будут обсуждаться ниже. В дополнение к этому существует широкий спектр общих органических реакций, которые исторически сыграли решающую роль в развитии, во-первых, понимания концепций кольцевой химии, а во-вторых, надежных методов получения кольцевых структур с высоким выходом и с определенными ориентация заместителей в кольце (т.е. определенная стереохимия ). Эти общие реакции включают в себя:
- Ацилоиновая конденсация ;
- Анодное окисление ; и
- Конденсация Дикмана применительно к образованию колец.
Реакции замыкания кольца
[ редактировать ]В органической химии различные синтетические вещества особенно полезны для замыкания карбоциклических и других колец; они называются реакциями замыкания цикла . Примеры включают в себя:
- алкиновая тримеризация ;
- бергмановская циклизация эндиина ;
- реакции Дильса -Альдера между сопряженным диеном и замещенным алкеном и другие циклоприсоединения ; реакции
- реакция циклизации Назарова , первоначально представлявшая собой циклизацию дивинилкетона;
- различные радикальные циклизации ;
- реакции метатезиса с замыканием цикла , которые также можно использовать для осуществления определенного типа полимеризации ;
- , Синтез больших колец Ружички при котором две карбоксильные группы объединяются с образованием карбонильной группы с потерей СО 2 и Н 2 О ;
- превращающий Синтез Венкера, бета- аминоспирт в азиридин
- другие реакции, такие как реакция аминогруппы с гидроксигруппой , как при биосинтезе соланина
Реакции раскрытия кольца
[ редактировать ]Различные дополнительные синтетические процедуры особенно полезны для раскрытия карбоциклических и других колец, обычно которые содержат двойную связь или другую функциональную группу «ручку» для облегчения химического процесса; они называются реакциями раскрытия цикла . Примеры включают в себя:
- метатезис раскрытия кольца , который также может быть использован для осуществления определенного типа полимеризации .
Реакции расширения и сжатия кольца.
[ редактировать ]Реакции расширения и сжатия кольца широко распространены в органическом синтезе и часто встречаются в перициклических реакциях . Расширение и сжатие кольца может включать в себя вставку функциональной группы, как в случае с по Байеру-Виллигеру окислением циклических кетонов , перегруппировку циклических карбоциклов, как это видно во внутримолекулярных реакциях Дильса-Альдера , или коллапс или перегруппировку бициклических соединений , как несколько примеров.
Примеры
[ редактировать ]Простые моноциклические примеры
[ редактировать ]Ниже приведены примеры простых и ароматических карбоциклов, неорганических циклических соединений и гетероциклов:
- Простые моноциклические соединения: карбоциклические, неорганические и гетероциклические (ароматические и неароматические) примеры.
-
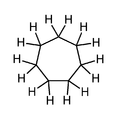
Циклогептан , простое 7-членное карбоциклическое соединение, показаны водороды метилена (неароматические).
-
Бензол – шестичленное карбоциклическое органическое соединение. Показаны метиновые водороды, а 6 электронов показаны как делокализованные посредством рисунка кружка (ароматические).
-
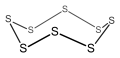
Цикло - октасера , 8-членное неорганическое циклическое соединение (неароматическое).
-
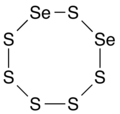
Диселен гексасульфид , 8-членное неорганическое гетероциклическое соединение (неароматическое).
-
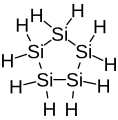
Циклопентасилан — 5-членное неорганическое циклическое соединение (неароматическое).
-
Гексаметилциклотрисилоксан — 6-членное органическое гетероциклическое соединение (неароматическое).
-
Гексахлорфосфазен — 6-членное неорганическое гетероциклическое соединение (ароматическое).
-
Боразин , 6-членное неорганическое гетероциклическое соединение (может быть ароматическим).
-
Пентазол , 5-членное неорганическое циклическое соединение (ароматическое).
-
Азетидин , 4-членное азотистое (аза) гетероциклическое соединение, подразумеваются атомы водорода метилена , не показаны (неароматические).
-
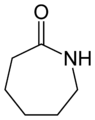
Капролактам , 7-членное гетероциклическое органическое соединение (неароматическое).
-
Пиридин , 6-членное гетероциклическое соединение, атомы водорода метина подразумеваются (не показаны), а делокализованные π-электроны показаны как дискретные связи (ароматические).
Сложные и полициклические примеры
[ редактировать ]Ниже приведены примеры циклических соединений, демонстрирующих более сложные кольцевые системы и стереохимические особенности:
- Сложные циклические соединения: макроциклические и полициклические примеры.
-
Нафталин , технически полициклическое, а точнее бициклическое соединение, с кружками, показывающими делокализацию π-электронов (ароматические).
-
Декалин (декагидронафталин), полностью насыщенное производное нафталина , демонстрирующее две стереохимии, возможные для «слияния» двух колец вместе, и то, как это влияет на формы, доступные для этого бициклического соединения (неароматического).
-
Паклитаксел , полициклический природный продукт с трициклическим ядром: с гетероциклическим 4-членным кольцом D, присоединенным к дополнительным 6- и 8-членным карбоциклическим (A/C и B) кольцам (неароматическим) и с тремя дополнительными подвесками. фенильные кольца на его «хвосте» и присоединены к C-2 (сокр. Ph, C 6 H 5 ; ароматические соединения).
-
Репрезентативная трехмерная форма, принятая паклитакселом в результате его уникальной циклической структуры. [11]
-
Холестерин , еще один терпеновый природный продукт, в частности, стероид , класс тетрациклических молекул (неароматических).
-
Бензо[a]пирен , пентациклическое соединение, как природное, так и искусственное, и делокализованные π-электроны, представленные в виде дискретных связей (ароматические).
-
Пагодан — сложное высокосимметричное искусственное полициклическое соединение (неароматическое).
-
Бреветоксин А , природный продукт с десятью кольцами, полностью слитыми и полностью гетероциклическими , токсичный компонент, связанный с организмами, ответственными за красные приливы . Группа R справа относится к одной из нескольких возможных четырехуглеродных боковых цепей (см. основную статью о Бреветоксине ; неароматическая).
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Марч, Джерри (1985), Продвинутая органическая химия: реакции, механизмы и структура, 3-е издание , Нью-Йорк: Wiley, ISBN 9780471854722 , OCLC 642506595 [ нужна страница ]
- ^ Халдук, И. (1961). «Классификация неорганических циклических соединений». Журнал структурной химии . 2 (3): 350–8. дои : 10.1007/BF01141802 . S2CID 93804259 .
- ^ Реймонд, Жан-Луи (2015). «Химический космический проект» . Отчеты о химических исследованиях . 48 (3): 722–30. дои : 10.1021/ar500432k . ПМИД 25687211 .
- ^ Перейти обратно: а б с д и ж г Уильям Ройш (2010). «Стереоизомеры. Часть I» в виртуальном учебнике органической химии . Мичиганский государственный университет. Архивировано из оригинала 10 марта 2015 года . Проверено 7 апреля 2015 г.
- ^ Перейти обратно: а б Золотой книги ИЮПАК Гетероциклические соединения
- ^ Перейти обратно: а б Тем не менее, У. Кларк; Галинкер, Игорь (1981). «Химические последствия конформации макроциклических соединений». Тетраэдр . 37 (23): 3981–96. дои : 10.1016/S0040-4020(01)93273-9 .
- ^ Перейти обратно: а б Дж. Д. Дуниц (1968). Дж. Д. Дуниц и Дж. А. Иберс (ред.). Перспективы структурной химии . Том. 2. Нью-Йорк: Уайли. стр. 1–70.
- ^ Элиэль, Э.Л., Вилен, С.Х. и Мандер, Л.С. ( 1994 ) Стереохимия органических соединений, John Wiley and Sons, Inc., Нью-Йорк. [ нужна страница ]
- ^ Анет, ФАЛ; Сен-Жак, М.; Хенрикс, премьер-министр; Ченг, АК; Крейн, Дж.; Вонг, Л. (1974). «Конформационный анализ кетонов среднего кольца». Тетраэдр . 30 (12): 1629–37. дои : 10.1016/S0040-4020(01)90685-4 .
- ^ Моррис, Кристофер Г.; Пресс, Академик (1992). Академический словарь прессы по науке и технологиям . Профессиональное издательство Персидского залива. п. 120. ИСБН 9780122004001 . Архивировано из оригинала 13 апреля 2021 г. Проверено 14 сентября 2020 г.
- ^ Лёве, Дж; Ли, Х; Даунинг, К.Х.; Ногалес, Э (2001). «Уточненная структура αβ-тубулина с разрешением 3,5 Å» . Журнал молекулярной биологии . 313 (5): 1045–57. дои : 10.1006/jmbi.2001.5077 . ПМИД 11700061 . Архивировано из оригинала 22 января 2021 г. Проверено 14 сентября 2020 г.
Дальнейшее чтение
[ редактировать ]- Юрген-Хинрих Фурхоп и Густав Пенцлин, 1986, «Органический синтез: концепции, методы, исходные материалы», Вайнхайм, BW, DEU:VCH, ISBN 0895732467 , см . [1] , по состоянию на 19 июня 2015 г.
- Майкл Б. Смит и Джерри Марч, 2007 г., «Продвинутая органическая химия Марта: реакции, механизмы и структура», 6-е изд., Нью-Йорк, штат Нью-Йорк, США: Wiley & Sons, ISBN 0470084944 , см . [2] , по состоянию на 19 июня 2015 г.
- Фрэнсис А. Кэри и Ричард Дж. Сундберг, 2006 г., «Название «Продвинутая органическая химия: Часть A: Структура и механизмы», 4-е изд., Нью-Йорк, штат Нью-Йорк, США: Springer Science & Business Media, ISBN 0306468565 , см . [3] , по состоянию на 19 июня 2015 г.
- Майкл Б. Смит, 2011, «Органическая химия: кислотно-основной подход», Бока-Ратон, Флорида, США: CRC Press, ISBN 1420079212 , см. [4] , по состоянию на 19 июня 2015 г. [Возможно, это не самый необходимый материал для этой статьи, но значительный контент здесь доступен в Интернете.]
- Джонатан Клейден, Ник Гривз и Стюарт Уоррен, 2012, «Органическая химия», Оксфорд, Оксон, GBR: Oxford University Press, ISBN 0199270295 , см . [5] , по состоянию на 19 июня 2015 г.
- Ласло Курти и Барбара Чако, 2005, «Стратегическое применение названных реакций в органическом синтезе: предыстория и подробные механизмы», Амстердам, Нью-Хэмпшир, НЛД: Elsevier Academic Press, 2005ISBN 0124297854, см. [6] , по состоянию на 19 июня 2015 г.
Внешние ссылки
[ редактировать ]- Полициклические + соединения Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
- Макроциклические + соединения Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)















![Репрезентативная трехмерная форма, принятая паклитакселом в результате его уникальной циклической структуры.[11]](http://upload.wikimedia.org/wikipedia/commons/thumb/5/5a/Paclitaxel_JMolBiol_2001_1045.jpg/108px-Paclitaxel_JMolBiol_2001_1045.jpg)

![Бензо[а]пирен, пентациклическое соединение, как природное, так и искусственное, и делокализованные π-электроны, представленные в виде дискретных связей (ароматические).](http://upload.wikimedia.org/wikipedia/commons/thumb/f/fa/Benzo-a-pyrene.svg/192px-Benzo-a-pyrene.svg.png)

