Боразин
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 1,3,5,2,4,6-триазатриборинан (только предварительно выбранный [1] ) | |||
| Другие имена Циклотриборазанборазол Неорганический бензол Боразол | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.169.303 | ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| Б 3 Ч 6 Н 3 | |||
| Молярная масса | 80.50 g/mol | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 0,81 г/см 3 | ||
| Температура плавления | -58 ° C (-72 ° F; 215 К) | ||
| Точка кипения | 53 ° C (127 ° F; 326 К) (55 ° C при 105 Па) | ||
| -49.6·10 −6 см 3 /моль | |||
| Опасности | |||
| NFPA 704 (огненный алмаз) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Боразин , также известный как боразол , представляет собой неорганическое соединение с химической формулой B 3 H 6 N 3 . В этом циклическом соединении чередуются три единицы BH и три единицы NH. Соединение изоэлектронно и изоструктурно бензолу . По этой причине боразин иногда называют «неорганическим бензолом». Как и бензол, боразин представляет собой бесцветную жидкость. [2] с ароматным запахом.
Синтез
[ редактировать ]Об этом соединении сообщили в 1926 году химики Альфред Сток и Эрих Поланд путем реакции диборана с аммиаком . [3]
Боразин можно синтезировать обработкой диборана и аммиака в соотношении 1:2 при 250–300 °С с конверсией 50%.
- 3 Б 2 Н 6 + 6 НХ 3 → 2 Б 3 Н 6 Н 3 + 12 Н 2
Альтернативный, более эффективный путь начинается с боргидрида натрия и сульфата аммония : [4]
- 6 NaBH 4 + 3 (NH 4 ) 2 SO 4 → 2 B 3 N 3 H 6 + 3 Na 2 SO 4 + 18 H 2
В двухэтапном процессе получения боразина трихлорид бора сначала превращается в трихлорборазин:
- 3 BCl 3 + 3 NH 4 Cl → Cl 3 B 3 H 3 N 3 + 9 HCl
Облигации B-Cl впоследствии конвертируются в облигации BH:
- 2 Cl 3 B 3 H 3 N 3 + 6 NaBH 4 → 2 B 3 H 6 N 3 + 3 B 2 H 6 + 6 NaCl
Структура
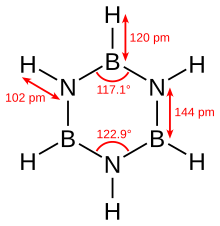
[ редактировать ]Боразин изоэлектронен бензолу и имеет аналогичную связь, поэтому его иногда называют «неорганическим бензолом». Это сравнение не совсем корректно из-за в электроотрицательности разницы бора и азота. Рентгеновские кристаллографические структурные определения показывают, что длины связей внутри боразинового кольца эквивалентны и составляют 1,429 Å - свойство, присущее бензолу. [5] Однако боразиновое кольцо не образует идеальный шестиугольник. Валентный угол составляет 117,1° у атомов бора и 122,9° у атомов азота, что придает молекуле D 3 h точечную группу симметрии .
Электроотрицательность дефицит бора (2,04 по шкале Полинга ) по сравнению с электроотрицательностью азота (3,04), а также электронов бора на атоме и неподеленной паре азота способствуют альтернативным мезомерным структурам боразина.
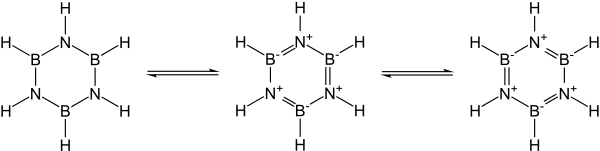
Бор ведет себя как кислота Льюиса , а азот — как основание Льюиса .
Ароматичность
[ редактировать ]Из-за его сходства с бензолом был проведен ряд вычислительных и экспериментальных анализов ароматичности боразина . Число пи-электронов в боразине подчиняется правилу 4n + 2, а длины связей BN равны, что позволяет предположить, что соединение может быть ароматическим. Однако разница в электроотрицательности между бором и азотом создает неравномерное распределение заряда, что приводит к образованию связей с более сильным ионным характером, и, таким образом, ожидается, что делокализация электронов будет хуже, чем у полностью углеродного аналога. Боразин со стандартным изменением энтальпии образования Δ f H, составляющим -531 кДж/моль, термически очень стабилен.
Орбитали естественных связей (NBO)
[ редактировать ]Анализ орбитали естественной связи (NBO) предполагает слабую ароматичность боразина. [6] В модели NBO связи BN в кольце слегка смещены от ядерных осей, а B и N имеют большие различия в заряде. Анализ естественного химического экранирования (NCS) предоставляет некоторые дополнительные доказательства ароматичности, основанные на вкладе π-связи BN в магнитное экранирование. Расчеты на основе орбиталей NBO показывают, что эта π-связь допускает слабый кольцевой ток, который в некоторой степени противодействует магнитному полю, моделируемому в центре боразинового кольца. Небольшой кольцевой ток действительно предполагает некоторую делокализацию.
Функция локализации электрона (ELF)
[ редактировать ]Топологический анализ связи в боразине с помощью функции локализации электронов (ELF) показывает, что боразин можно описать как π-ароматическое соединение. Однако связь в боразине менее делокализована, чем в бензоле, что обусловлено различием значений бифуркаций электронных бассейнов. Большие значения бифуркации указывают на лучшую делокализацию электронов, и утверждается, что, когда это значение бифуркации превышает 0,70, делокализация достаточна для обозначения ароматического соединения. [7] Для бензола это значение составляет 0,91, но π-система боразина раздваивается при значении ELF 0,682. [8] Это вызвано разницей в электроотрицательности между B и N, что приводит к более слабому взаимодействию связи, чем взаимодействие CC в бензоле, что приводит к усилению локализации электронов на звеньях BH и NH. Значение бифуркации немного ниже предела 0,70, что предполагает умеренную ароматичность.
Реактивность
[ редактировать ]Гидролиз
[ редактировать ]Боразин легко гидролизуется с образованием борной кислоты , аммиака и водорода.
Полимеризация
[ редактировать ]
При нагревании боразина при 70 °C выделяется водород с образованием полиборазилена:
- n B 3 N 3 H 6 → 1/n[B 3 N 3 H 4 ] n
С галогеноводородами и галогенами
[ редактировать ]С хлористым водородом образует аддукт .
- B 3 N 3 H 6 + 3 HCl → B 3 N 3 H 9 Cl 3
- Реакция присоединения боразина с хлористым водородом.
- B 3 N 3 H 9 Cl 3 + NaBH 4 → (BH 4 N) 3
- Восстановление борогидридом натрия
Реакция присоединения с бромом не требует катализатора . Боразины подвергаются нуклеофильной атаке по бору и электрофильной атаке по азоту.
Керамический предшественник
[ редактировать ]Нитрид бора можно получить нагреванием полиборазилена до 1000 °C. [4]
Боразины также являются исходным материалом для других потенциальных керамик, таких как карбонитриды бора . Боразин также можно использовать в качестве прекурсора для выращивания тонких пленок и одиночных слоев гексагонального нитрида бора (h-BN) на каталитических поверхностях, таких как медь, [9] платина, [10] никель [11] железо [12] и многое другое с помощью химического осаждения из паровой фазы (CVD).

Полиборазилен был предложен в качестве переработанной среды для хранения водорода для транспортных средств на водородных топливных элементах с использованием процесса «единого котла» для разложения и восстановления с целью воссоздания аммиачно-борана. [13]
Было предсказано, что среди других соединений типа BN смешанные амино-нитрозамещенные боразины превосходят взрывчатые вещества на основе углерода, такие как CL-20 . [14] [15]
Родственные соединения
[ редактировать ]( С
22Ч
2 Б
2 Н
2 ) представляет собой шестичленное ароматическое кольцо с двумя атомами углерода, двумя атомами азота и двумя атомами бора в противоположных парах. [16] [17]
1,2-Дигидро-1,2-азаборин ( C
4 БНХ
6 ) представляет собой шестичленное кольцо с четырьмя атомами углерода, одним атомом азота и одним атомом бора.
См. также
[ редактировать ]Дальнейшее чтение
[ редактировать ]- Нельсон, Ральф; и др. (1 сентября 1967 г.). «Избранные значения электрических дипольных моментов молекул в газовой фазе» (PDF) . Американское национальное бюро стандартов (10): 17.
Ссылки
[ редактировать ]- ^ «Фронт материи». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 968. дои : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Дювард Шрайвер; Питер Аткинс (2010). Неорганическая химия (Пятое изд.). Нью-Йорк: WH Freeman and Company. п. 328. ИСБН 978-1429218207 .
- ^ Запас A, Польша E (октябрь 1926 г.). знаниях 2 H 6 B 5 H 11 » « и B кислоты Раствор борной VIII . О . Отчеты (на немецком языке). 59 (9): 2210–2215. дои : 10.1002/cber.19260590906 .
- ^ Jump up to: а б Уайдман, Томас; Фазен, Пол Дж.; Линч, Энн Т.; Су, Кай; Ремсен, Эдвард Э.; Снеддон, Ларри Г. (1998). «Боразины, полиборазилены, β-винилборазины и поли (β-винилборазины)». Боразин, полиборазилен, β-винилборазин и поли(β-винилборазин) . Неорганические синтезы. Том 32. С. 232–242. дои : 10.1002/9780470132630.ch39 . ISBN 9780470132630 .
- ^ Бозе Р., Маулитц А.Х., Стеллберг П. (1994). «Твердотельный боразин: заслуживает ли он названия «неорганический бензол»?». Химише Берихте . 127 (10): 1887–1889. дои : 10.1002/cber.19941271011 .
- ^ Шен В., Ли М., Ли Ф., Ван С. (2007). «Теоретическое исследование боразина и его производных». Неорг. Хим. Акта . 360 (2): 619–624. дои : 10.1016/j.ica.2006.08.028 .
- ^ Сантос Х.К., Тизнадо В., Контрерас Р., Фуэнтеальба П. (январь 2004 г.). «Сигма-пи разделение функции локализации электрона и ароматичности». Журнал химической физики . 120 (4): 1670–3. Бибкод : 2004JChPh.120.1670S . дои : 10.1063/1.1635799 . hdl : 10533/175272 . ПМИД 15268298 .
- ^ Ислас Р., Чаморро Э., Роблес Дж., Хейне Т., Сантос Х.К., Мерино Дж. (2007). «Боразин: быть или не быть ароматным». Структура. Хим . 18 (6): 833–839. дои : 10.1007/s11224-007-9229-z . S2CID 95098134 .
- ^ Кидамби П.Р., Блюм Р., Клинг Дж., Вагнер Дж.Б., Бетц С., Уэзерап Р.С. и др. (ноябрь 2014 г.). «Наблюдения in situ во время химического осаждения из паровой фазы гексагонального нитрида бора на поликристаллическую медь» . Химия материалов . 26 (22): 6380–6392. дои : 10.1021/cm502603n . ПМК 4311958 . ПМИД 25673919 .
- ^ Ким Джи, Чан А.Р., Чон ХИ, Ли Зи, Кан DJ, Шин Х.С. (апрель 2013 г.). «Выращивание высококристаллического однослойного гексагонального нитрида бора на перерабатываемой платиновой фольге». Нано-буквы . 13 (4): 1834–9. Бибкод : 2013NanoL..13.1834K . дои : 10.1021/nl400559s . ПМИД 23527543 .
- ^ Чаттерджи С., Луо З., Асерс М., Йейтс Д.М., Джонсон А.Т., Снеддон Л.Г. (25 октября 2011 г.). «Химическое осаждение нанолистов нитрида бора из паровой фазы на металлические подложки посредством реакций декаборана/аммиака». Химия материалов . 23 (20): 4414–4416. дои : 10.1021/cm201955v . ISSN 0897-4756 .
- ^ Канева С., Уэзерап Р.С., Байер Б.С., Бреннан Б., Спенсер С.Дж., Мингард К. и др. (март 2015 г.). «Контроль зародышеобразования больших монокристаллических доменов монослойного гексагонального нитрида бора с помощью катализаторов Fe, легированного кремнием» . Нано-буквы . 15 (3): 1867–75. Бибкод : 2015NanoL..15.1867C . дои : 10.1021/nl5046632 . ПМЦ 4358078 . ПМИД 25664483 .
- ^ Дэвис Б.Л., Диксон Д.А., Гарнер Э.Б., Гордон Дж.К., Матус М.Х., Скотт Б., Стивенс Ф.Х. (2009). «Эффективная регенерация частично отработанного аммиачно-боранового топлива». Ангеванде Хеми . 48 (37): 6812–6. дои : 10.1002/anie.200900680 . ОСТИ 960522 . ПМИД 19514023 .
- ^ Кох ЕС, Клапотке ТМ (2012). «Взрывчатка на основе бора» . Пороха, взрывчатые вещества, пиротехника . 37 (3): 335–344. дои : 10.1002/prep.201100157 .
- ^ Кервин С., Фенвик О., Ди Стасио Ф., Шин Ю.С., Воутерс Дж., Аккорси Г. и др. (июнь 2013 г.). «Полиморфизм, флуоресценция и оптоэлектронные свойства производного боразина» . Химия: Европейский журнал . 19 (24): 7771–9. дои : 10.1002/chem.201204598 . ПМИД 23616404 . S2CID 9774352 .
- ^ Шривастава А.К., Мисра Н. (2015). «Представляем «карборазин» как новую гетероциклическую ароматическую разновидность». Новый химический журнал . 39 (4): 2483–2488. дои : 10.1039/c4nj02089h . S2CID 94792421 .
- ^ Бонифази Д., Фазано Ф., Лоренцо-Гарсия М.М., Маринелли Д., Убаха Х., Тассерул Дж. (октябрь 2015 г.). «Углеродные каркасы, легированные бором и азотом: органическая химия, самосборка и применение материалов боразина и его производных». Химические коммуникации . 51 (83): 15222–36. дои : 10.1039/C5CC06611E . ПМИД 26411675 .
Дальнейшее чтение
[ редактировать ]- Снеддон Л.Г., Мирабелли М.Г., Линч А.Т., Фазен П.Дж., Су К., Бек Дж.С. (1991). «Полимерные предшественники керамики на основе бора» (PDF) . Чистое приложение. Хим . 63 (3): 407–410. дои : 10.1351/pac199163030407 . S2CID 53629042 .
- Чон Дж.К., Учимару Ю., Ким Д.П. (август 2004 г.). «Синтез новой аморфной керамики из карбонитрида бора из сополимера производного бора методом гидроборирования». Неорганическая химия . 43 (16): 4796–8. дои : 10.1021/ic035254a . ПМИД 15285647 .
- Пэтцольд П. (1991). «Новые перспективы в химии бора и азота - I» (PDF) . Чистое приложение. Хим . 63 (3): 345–350. дои : 10.1351/pac199163030345 . S2CID 53659373 .
- Ислас Р. (2007). «Боразин: быть или не быть ароматным». Структурная химия . 18 (6): 833–839. дои : 10.1007/s11224-007-9229-z . S2CID 95098134 .
Внешние ссылки
[ редактировать ]![]() СМИ, связанные с боразином, на Викискладе?
СМИ, связанные с боразином, на Викискладе?