Лонгифолен
 | |
| Имена | |
|---|---|
| Название ИЮПАК (1 R ,2 S ,7 S ,9 S )-3,3,7-триметил-8-метилентрицикло- [5.4.0.0 2,9 ]ундекан | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| 5731712 2044263 4663756 | |
| ЧЭБИ |
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.006.812 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA ) |
|
| Характеристики | |
| С 15 Ч 24 | |
| Молярная масса | 204.36 g/mol |
| Плотность | 0,928 г/см 3 |
| Точка кипения | 254 ° C (489 ° F; 527 К) (706 мм рт. ст.) |
| Опасности | |
| СГС Маркировка : | |
   | |
| Опасность | |
| Х304 , Х317 , Х410 | |
| P261 , P272 , P273 , P280 , P301+P310 , P302+P352 , P321 , P331 , P333+P313 , P363 , P391 , P405 , P501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Лонгифолен — это распространенное (или тривиальное) химическое название встречающегося в природе маслянистого жидкого углеводорода, содержащегося главным образом в высококипящей фракции некоторых сосновых смол . Название происходит от названия вида сосны , из которой было выделено соединение. [1] По химическому составу лонгифолен представляет собой трициклический сесквитерпен . Эта молекула является хиральной , а энантиомер, обычно встречающийся в соснах и других высших растениях, демонстрирует положительное оптическое вращение +42,73°. Другой энантиомер (оптическое вращение -42,73°) обнаружен в небольших количествах у некоторых грибов и печеночников .
Лонгифолен также является одним из двух наиболее распространенных ароматических компонентов чая лапсанг сушонг , поскольку чай коптят на кострах из сосновых дров. [2]
и Возникновение синтезы
Терпентин, полученный из Pinus longifolia (устаревшее название Pinus roxburghii Sarg.), содержит до 20% лонгифолена. [3]
Лабораторный синтез лонгифолена привлек большое количество синтезаторов. [4] [5] [6] [7] [8] [9] [10]
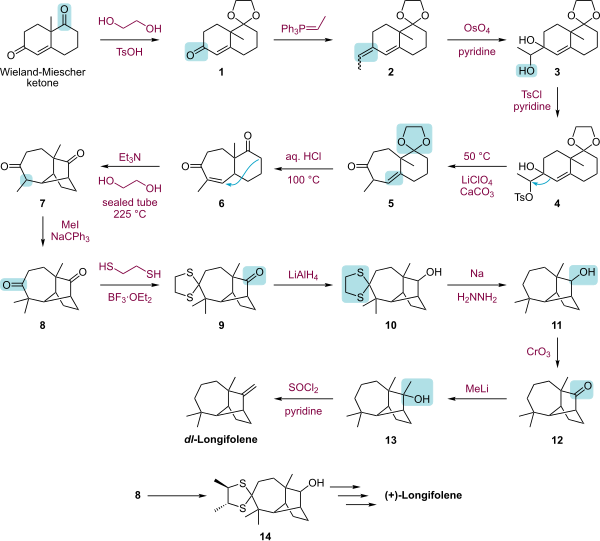 |
| Полный синтез лонгифолена от Corey.svg |
|---|
Биосинтез [ править ]
Биосинтез лонгифолена начинается с фарнезилдифосфата ( 1 ) (также называемого фарнезилпирофосфатом ) посредством катионного каскада полициклизации. Потеря пирофосфатной группы и циклизация дистальным алкеном дают промежуточное соединение 3 , которое посредством 1,3-гидридного сдвига дает промежуточное соединение 4 . После двух дополнительных циклизаций промежуточное соединение 6 дает лонгифолен путем миграции 1,2-алкила .

Реакция [ править ]
Он реагирует с бораном с образованием производного дилонгифолилборана , который представляет собой хиральный гидроборирующий агент. [11]
Ссылки [ править ]
- ^ Наффа, П.; Уриссон, Г. Бюллетень Химического общества Франции , 1954 , 1410.
- ^ Шань-Шань Яо; Вэнь-Фей Го; И Лу; Юань-Сюнь Цзян, «Вкусовые характеристики лапсанга сушонга и копченого лапсанга сушонга, специального китайского черного чая с процессом копчения сосны», Журнал сельскохозяйственной и пищевой химии , Vol. 53, №22, (2005) [ постоянная мертвая ссылка ]
- ^ Гшайдмайер, Манфред; Флейг, Хельмут (2000). «Скипидары». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a27_267 . ISBN 3527306730 .
- ^ Кори, Э.Дж.; Оно, Масаджи.; Митра, Раджат Б.; Ватакенчерри, Пол А. (февраль 1964 г.). «Тотальный синтез лонгифолена». Журнал Американского химического общества . 86 (3): 478–485. дои : 10.1021/ja01057a039 .
- ^ Макмерри, Джон Э.; Иссер, Стивен Дж. (октябрь 1972 г.). «Тотальный синтез лонгифолена». Журнал Американского химического общества . 94 (20): 7132–7137. дои : 10.1021/ja00775a044 .
- ^ Фолькманн, Роберт А.; Эндрюс, Гленн С.; Джонсон, Уильям С. (август 1975 г.). «Новый синтез лонгифолена». Журнал Американского химического общества . 97 (16): 4777–4779. дои : 10.1021/ja00849a062 .
- ^ Оппольцер, Вольфганг; Гёдель, Тьерри (апрель 1978 г.). «Новый и эффективный полный синтез (.+-.)-лонгифолена». Журнал Американского химического общества . 100 (8): 2583–2584. дои : 10.1021/ja00476a071 .
- ^ Шульц, Артур Г.; Пуч, Сальвадор (март 1985 г.). «Эквивалентность внутримолекулярного диен-карбенового циклоприсоединения и энантиоселективное восстановление-алкилирование по Берчу с использованием хирального вспомогательного подхода. Полный синтез (.+-.)- и (-)-лонгифолена». Журнал органической химии . 50 (6): 915–916. дои : 10.1021/jo00206a049 .
- ^ Бо, Лей; Фаллис, Алекс Г. (май 1990 г.). «Прямой полный синтез (+)-лонгифолена с помощью внутримолекулярной стратегии Дильса-Альдера». Журнал Американского химического общества . 112 (11): 4609–4610. дои : 10.1021/ja00167a105 .
- ^ Ho, Gregory J. Org. Chem. 2005 , 70 , 5139 -5143.
- ^ Дев, Сух (1981). «Аспекты химии лонгифолена. Пример еще одного аспекта химии натуральных продуктов». Отчеты о химических исследованиях . 14 (3): 82–88. дои : 10.1021/ar00063a004 .