Хиноксалин

| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Хиноксалин [ 1 ] | |||
| Другие имена
Бензо[b]пиразин, Бензопиразин, Бензопарадиазин, 1,4-бензодиазин, Фенопиазин, Фенпиазин, Хиназин, Хиноксалин
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.001.862 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 8 Ч 6 Н 2 | |||
| Молярная масса | 130.150 g·mol −1 | ||
| Температура плавления | 29-32 °С | ||
| Точка кипения | От 220 до 223 ° C (от 428 до 433 ° F; от 493 до 496 К) | ||
| Кислотность ( pKa ) | 0.60 [ 2 ] | ||
| Опасности | |||
| СГС Маркировка : | |||

| |||
| Предупреждение | |||
| Х315 , Х319 , Х335 | |||
| P261 , P264 , P271 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313 , P337+P313 , P362 , P403+P233 , P405 , P501 | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
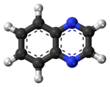
Хиноксалин соединение, содержащее кольцевой комплекс , , также называемый бензопиразином , в органической химии представляет собой гетероциклическое состоящий из бензольного кольца и пиразинового кольца. Он изомерен другим нафтиридинам, включая хиназолин , фталазин и циннолин . [ 3 ] Это бесцветное масло, которое плавится при температуре чуть выше комнатной. Хотя сам хиноксалин представляет в основном академический интерес, производные хиноксалина используются в качестве красителей, фармацевтических препаратов (например, варениклин ) и антибиотиков, таких как олаквиндокс , карбадокс , эхиномицин , левомицин и актинолейтин .
Синтез
[ редактировать ]Они могут быть образованы конденсацией орто - диаминов с 1,2- дикетонами . Исходное вещество группы, хиноксалин, образуется при глиоксаля конденсации с 1,2-диаминобензолом . [ 4 ] α-кетоновые кислоты , α-хлоркетоны, α- альдегидные спирты и α-кетоновые спирты. Замещенные производные возникают, когда вместо дикетонов используются [ 3 ] Хиноксалин и его аналоги также могут быть образованы восстановлением аминокислот, замещенных 1,5-дифтор-2,4-динитробензолом (ДФДНБ): [ 5 ]
Одно исследование [ 6 ] использовали 2-иодоксибензойную кислоту (IBX) в качестве катализатора в реакции бензила с 1,2-диаминобензолом:
Использование
[ редактировать ]свойства соединений хиноксалина. противоопухолевые Интерес представляют [ 7 ] Недавно хиноксалин и его аналоги были исследованы в качестве лигандов. [ 8 ]
Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 212. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ Браун, ХК; и др. (1955). Бауде, Э.А.; Наход, ФК (ред.). Определение органических структур физическими методами . Нью-Йорк: Академическая пресса.
- ^ Jump up to: а б Одно или несколько предыдущих предложений включают текст из публикации, которая сейчас находится в свободном доступе : Чисхолм, Хью , изд. (1911). « Хиноксалины ». Британская энциклопедия . Том. 22 (11-е изд.). Издательство Кембриджского университета. п. 760.
- ^ 2,3-пиразиндикарбоновая кислота» Рубен Г. Джонс и Кейт К. Маклафлин Org. Synth. 1950, 30, 86. дои : 10.15227/orgsyn.030.0086 . В этой статье описывается получение хиноксалина в качестве промежуточного продукта.
- ^ Сян-Хун Ву; Ган Лю; и др. (2004). «Восстановительная циклизация аналогов 2-хиноксалинола в фазе раствора: систематическое исследование параллельного синтеза». Мол. Дайверы . 8 (2): 165–174. дои : 10.1023/B:MODI.0000025639.89179.60 . ПМИД 15209169 . S2CID 28252647 .
- ^ Херави, Маджид М. (2006). «Простой синтез производных хиноксалина с использованием о-йодоксибензойной кислоты (IBX) при комнатной температуре» . Аркивок . 2006 (16): 16–22. дои : 10.3998/ark.5550190.0007.g02 . hdl : 2027/spo.5550190.0007.g02 .
- ^ Жан Рено; Мишель Барон; Патрик Майлиет; и др. (1981). «Гетероциклические хиноны. 2. Хиноксалин-5,6-(и 5-8)-дионы. Потенциальные противоопухолевые средства». Евро. Дж. Мед. Хим . 16 (6): 545–550.
- ^ Сянхун Ву; Энн Э.В. Горден (2007). «Региоселективный синтез асимметрично замещенных 2-хиноксалинол-сален-лигандов». Дж. Орг. Хим . 72 (23): 8691–8699. дои : 10.1021/jo701395w . ПМИД 17939720 .