Тиазолидин
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК 1,3-тиазолидин [1] | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.007.275 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| C3H7NC3H7NS | |
| Молярная масса | 89.16 g·mol −1 |
| Плотность | 1,131 г/см 3 [2] |
| Точка кипения | От 72 до 75 ° C (от 162 до 167 ° F; от 345 до 348 К) [2] при 25 торр |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Тиазолидин представляет собой гетероциклическое органическое соединение формулы (CH2)3(NH)S. Это 5-членное насыщенное кольцо с тиоэфирной группой и аминной группой в положениях 1 и 3. Это аналог оксазолидина серный . Тиазолидин представляет собой бесцветную жидкость. Хотя родительский тиазолидин представляет только академический интерес, некоторые производные , например, тиазолидины , имеют важное значение, например, антибиотик пенициллин .
Подготовка [ править ]
Тиазолидин получают конденсацией цистеамина и формальдегида . [3] Аналогичными конденсациями могут быть синтезированы и другие тиазолидины. Известным производным является 4-карбокситиазолидин ( тиопролин ), полученный из формальдегида и цистеина .
Производные [ править ]

Полезные тиазолидины включают препарат пиоглитазон , антибиотик пенициллин , и N-метил-2-тиазолидинтион , ускоритель вулканизации хлоропреновых каучуков. [4]
Тиазолидины, функционализированные карбонилами во 2 и 4 положениях, тиазолидиндионы , представляют собой препараты, используемые при лечении сахарного диабета 2 типа . Роданин представляет собой родственный биологически активный вид, содержащий один карбонил и один тиокарбонил.
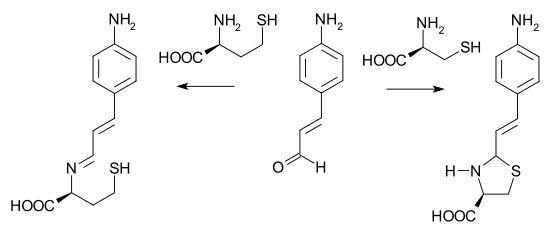
Многие тиазолидины получают из цистеина и родственных аминотиолов. [5] п- аминокоричный альдегид способен различать цистеин и гомоцистеин . В присутствии цистеина забуференный водный раствор альдегида меняется с желтого на бесцветный из-за реакции замыкания вторичного кольца имина. Гомоцистеин не способен замкнуть кольцо и цвет не меняется.
См. также [ править ]
Ссылки [ править ]
- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 142. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ↑ Перейти обратно: Перейти обратно: а б Тиазолиндин
- ^ Ратнер, Сара; Кларк, ХТ (1937). «Действие формальдегида на цистеин». Журнал Американского химического общества . 59 : 200–6. дои : 10.1021/ja01280a050 .
- ^ Рюдигер Шубарт (2000). «Дитиокарбаминовая кислота и производные». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a09_001 . ISBN 3527306730 .
- ^ Ван, Вэйхуа; Русин, Александр; Сюй, Сянъян; Ким, Кю Кван; Эскобедо, Хорхе О.; Факайоде, Сайо О.; Флетчер, Кристин А.; Лоури, Марк; Шоуолтер, Корин М.; Лоуренс, Кэндис М.; Фрончек, Фрэнк Р.; Уорнер, Исайя М.; Стронгин, Роберт М. (2005). «Обнаружение гомоцистеина и цистеина» . Журнал Американского химического общества . 127 (45): 15949–15958. дои : 10.1021/ja054962n . ПМК 3386615 . ПМИД 16277539 .