Тритиоацетон
| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Гексаметил-1,3,5-тритиан | |
| Другие имена
Тритиоацетон [ 1 ]
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 5-19-09-00119 | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.011.438 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 9 Ч 18 С 3 | |
| Молярная масса | 222.42 g·mol −1 |
| Плотность | 1,0660–1,0700 г/мл [ 2 ] |
| Температура плавления | 21,8°С [ 3 ] |
| Точка кипения | 107°С/10 мм рт.ст. [ 2 ] |
Показатель преломления ( n D )
|
от 1,5390 до 1,5430 [ 2 ] |
| Опасности | |
| СГС Маркировка : | |

| |
| Предупреждение | |
| Х315 , Х319 , Х335 | |
| P261 , P264 , P271 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313 , P337+P313 , P362 , P403+P233 , P405 , P501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
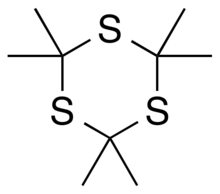
Тритиоацетон ( 1,3,5-тритиан ) представляет собой органическое химическое вещество формулы C. 2,2,4,4,6,6-гексаметил -
99Ч
18 С
3 . Его ковалентная структура: [–C(CH
3 )
2 –S–]
3 , то есть шестичленное кольцо из чередующихся атомов углерода и серы , с двумя метильными группами, присоединенными к каждому углероду. [ 4 ] [ 2 ] Его можно рассматривать как производное 1,3,5-тритиана метильной группы с заместителями для всех атомов водорода в этой исходной структуре.
Соединение Тритиоацетон представляет собой стабильный циклический тример тиоацетона (пропан-2-тиона), который сам по себе является нестабильным соединением. [ 5 ] [ 6 ] Напротив, аналогичное триоксановое соединение, 2,2,4,4,6,6-гексаметил-1,3,5-триоксан ( триацетон ), с атомами кислорода вместо атомов серы, кажется нестабильным, в то время как его соответствующий мономер ацетон (2-пропанон) стабилен.
Синтез
[ редактировать ]Тритиоацетон был впервые получен в 1889 году Бауманом и Фроммом путем реакции сероводорода с ацетоном. [ 6 ] В присутствии подкисленного ZnCl
2 при 25 °С получается продукт, состоящий из 60–70 % тритиоацетона, 30–40 % 2,2-пропандитиола и небольших количеств двух изомерных примесей 3,3,5,5,6,6- гексаметил-1,2,4-тритиан и 4-меркапто-2,2,4,6,6-пентаметил-1,3-дитиан . [ 6 ] Продукт также можно пиролизом аллилизопропилсульфида получить . [ 7 ] [ 8 ]
Реакции
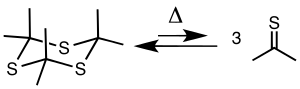
[ редактировать ]Пиролиз тритиоацетона при 500–650 °C и 5–20 мм рт. ст. дает тиоацетон, который можно собрать с помощью холодной ловушки при -78 °C.
Использование
[ редактировать ]Тритиоацетон содержится в некоторых ароматизаторах . Его номер FEMA — 3475. [ 9 ] [ 10 ] [ 11 ] [ 12 ]
Токсичность
[ редактировать ]СД (перорально) для мышей 50 составляет 2,4 г/кг. [ 9 ] [ 3 ]
См. также
[ редактировать ]- 2,4,6-триметил-1,3,5-тритиан
- Гексаметилциклотрисилоксан , аналог с кремний -кислородным кольцом вместо углеродно-серного.
- Гексаметилциклотрисилазан с кремний- азотистым кольцом. [ 13 ]
- 2,2,4,4,6,6-гексаметил-1,3,5-триселен-2,4,6-тристаннациклогексан , с олово - селеновым кольцом. [ 14 ] [ 15 ]
Ссылки
[ редактировать ]- ^ « Тритиоацетон ». Интернет-лист технических данных по химическим веществам, доступ 1 января 2020 г.
- ^ Jump up to: а б с д TCI America (2020): « Продукт H1278: 2,2,4,4,6,6-гексаметил-1,3,5-тритиан ». Страница онлайн-каталога, доступ 01.01.2020.
- ^ Jump up to: а б NCBI PubChem (2010): « 2,2,4,4,6,6-гексаметил-1,3,5-тритиан ». Интернет-лист технических данных по химическим веществам, доступ 1 января 2020 г.
- ^ Дэвид С. Бреслоу , Герман Скольник (2009): Мультисера, сера и кислород, пяти- и шестичленные гетероциклы , Часть 2; стр. 712. Том 68 химии гетероциклических соединений . ISBN 9780470188330
- ^ Р.Д. Липскомб и У.Х. Шарки (1970): «Характеристика и полимеризация тиоацетона». Журнал науки о полимерах – Часть A: Химия полимеров , том 8, выпуск 8, страницы 2187–2196. два : 10.1002/pol.1970.150080826
- ^ Jump up to: а б с Уильям Х. Шарки (1979): «Полимеризация через двойную связь углерод-сера». Полимеризация , серия «Достижения в области науки о полимерах» , том 17, страницы 73–103. дои : 10.1007/3-540-07111-3_2
- ^ Уильям Дж. Бэйли и Хильда Чу (1965): «Синтез политиоацетона». Препринты ACS Polymer , том 6, страницы=145–155
- ^ Хорст Бёме, Ханс Пфайфер и Эрих Шнайдер (1942): «Димерные тиокетоны». Отчеты Немецкого химического общества , том 75B, выпуск 7, страницы 900–909. doi : 10.1002/cber.19420750722 Примечание. В этом раннем отчете тример ошибочно принимается за мономер.
- ^ Jump up to: а б Э. Дж. Моран, О. Д. Истердей и Б. Л. Озер (1980): «Острая пероральная токсичность некоторых ароматизирующих химикатов». Лекарственная и химическая токсикология , том 3, выпуск 3, страницы 249–258. ПМИД 7449655 дои : 10.3109/01480548009002221
- ^ Всемирная организация здравоохранения (1999): « Тритиоацетон [ мертвая ссылка ] «. Онлайн-лист данных по оценке Объединенного комитета экспертов ФАО/ВОЗ по пищевым добавкам (JECFA) . По состоянию на 2 января 2020 г.
- ^ Г. Олофф и И. Фламент (1979): «Роль гетероатомных веществ в ароматических соединениях пищевых продуктов». В Fortschritte der Chemie Organischer Naturstoffe ( «Прогресс в химии органических натуральных продуктов »), том 36, страницы 231–283. дои : 10.1007/978-3-7091-3265-4_2
- ^ EUR-Lex (2012): « Запись в таблице 15.009: Тритиоацетон ». В Регламенте ЕС № 872/2012 , документ 32012R0872, Официальный журнал ЕС – Серия L , том 267, страницы 1–161.
- ^ Стюарт Д. Брюэр и Чарльз П. Хабер (1948): «Алкисилазаны и некоторые родственные соединения». Журнал Американского химического общества , том 70, выпуск 11, страницы 3888–3891. два : 10.1021/ja01191a106
- ^ Б. М. Михова (2008), «Данные ЯМР для углерода-13 – C6H18Se3Sn3» в книге Ландольта-Бёрнштейна – Конденсированные вещества группы III , том 35 Данные ядерного магнитного резонанса , подтом D5, Металлоорганические соединения . дои : 10.1007/978-3-540-74189-3_1362
- ^ Мартин Дрэгер, Аксель Блехер, Ханс-Юрген Якобсен, Бернт Кребс (1978): «Молекулярная и кристаллическая структура гексаметилциклотристаннаселенана [(CH
3 )
2 СнСи]
3 ». Журнал «Металлоорганическая химия» , том 161, выпуск 3, страницы 319–325. дои : 10.1016/S0022-328X(00)92243-5