Адаптерный белок везикулярного транспорта


Белки-адаптеры везикулярного транспорта представляют собой белки, участвующие в формировании комплексов, которые участвуют в транспортировке молекул из одного субклеточного места в другое. [ 2 ] [ 3 ] [ 4 ] Эти комплексы концентрируют нужные молекулы груза в пузырьках , которые отпочковываются или выходят из одной органеллы и перемещаются в другое место, куда доставляется груз. Хотя некоторые детали того, как эти адаптерные белки достигают своей специфичности к транспортировке, уже проработаны, еще многое предстоит узнать.
Существует несколько заболеваний человека, связанных с дефектами компонентов этих комплексов. [ 5 ] [ 6 ] включая болезни Альцгеймера и Паркинсона . [ 7 ]
Белки
[ редактировать ]






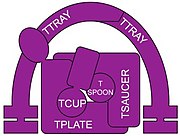
Большинство адаптерных белков являются гетеротетрамерами . В комплексах AP присутствуют два крупных белка ( ~ 100 кД ) и два более мелких белка. Один из крупных белков называется β ( бета ), где β1 входит в комплекс AP-1, β2 — в комплекс AP-2 и так далее. [ 10 ] Другой крупный белок в разных комплексах имеет разные обозначения. В AP-1 он называется γ ( гамма ), AP-2 имеет α ( альфа ), AP-3 имеет δ ( дельта ), AP-4 имеет ε ( эпсилон ) и AP-5 имеет ζ ( дзета ). [ 10 ] Два меньших белка представляют собой среднюю субъединицу, названную μ ( мю ~ 50 кДа) и малую субъединицу σ ( сигма ~ 20 кДа), названную с 1 по 5, что соответствует 5 комплексам AP. [ 10 ] Компоненты COPI (cop one) — коатомера и TSET (T-set) — мембранного транспортировочного комплекса, имеют сходные гетеротетрамеры AP-комплексов. [ 11 ]
Ретромер не является близким родственником, был рассмотрен, [ 12 ] и его белки здесь описываться не будут. GGA (локализация по Гольджи, гомология ушного домена гамма-адаптина, ARF-связывающие белки) представляют собой группу родственных белков (три у человека), которые действуют как мономерные белки-адаптеры клатрина в различных важных мембранных перевозках пузырьков . [ 13 ] но не похожи ни на один из комплексов АП и подробно рассматриваться в данной статье не будут. Стонины (не показаны на главном рисунке) также являются мономерами, в некоторых отношениях сходными с GGA. [ 4 ] и также не будут подробно обсуждаться в данной статье.
PTB — это белковые домены , которые включают NUMB , DAB1 и DAB2 . Эпсин и AP180 в домене ANTH являются другими адаптерными белками, которые были рассмотрены. [ 4 ]
Важный транспортный комплекс COPII не показан на первом рисунке. Комплекс COPII представляет собой гетерогексамер, но не тесно связан с комплексами AP/TSET. Отдельные белки комплекса COPII называются белками SEC , поскольку они кодируются генами, идентифицированными у секреторных мутантов дрожжей. Одним особенно интересным аспектом COPII является то, что он может образовывать типичные сферические везикулы и канальцы для транспортировки больших молекул, таких как предшественники коллагена , которые не могут поместиться внутри типичных сферических везикул. Структура COPII обсуждалась в открытой статье. [ 14 ] и не будет в центре внимания этой статьи. Это примеры гораздо большего набора грузовых адаптеров. [ 3 ]
Эволюционные соображения
[ редактировать ]Самый недавний общий предок (MRCA) эукариотов , должно быть, имел механизм транспортировки молекул между его эндомембранами и органеллами , и сообщалось о вероятной идентичности задействованного адапторного комплекса. [ 11 ] Считается, что MRCA имеет 3 белка, участвующих в транспортировке, и что они образуют гетеротример. Затем этот гетеротример «димеризуется» с образованием 6-членного комплекса. Отдельные компоненты далее превратились в текущие комплексы в указанном порядке, причем AP1 и AP2 расходились последними. [ 11 ]
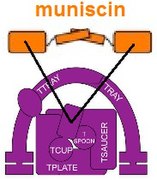
Кроме того, один компонент TSET, мунисцин, также известный как белок TCUP, по-видимому, превратился в часть белков опистоконтов (животных и грибов ). [ 11 ] Части AP-комплексов превратились в части белков GGA и стонина. [ 4 ] Есть данные, указывающие на то, что части комплекса ядерных пор и COPII могут быть эволюционно связаны. [ 15 ]
Образование транспортных везикул
[ редактировать ]

Наиболее охарактеризованным типом везикул является везикула, покрытая клатрином (CCV). Формирование пузырька COPII в эндоплазматическом ретикулуме и его транспорт к тельцу Гольджи . Участие гетеротетрамера COPI аналогично участию в ситуации AP/clathrin, но оболочка COPI не тесно связана с оболочками CCV или везикул COPII. [ 16 ] [ 17 ] AP-5 связан с двумя белками, SPG11 и SPG15 , которые имеют некоторое структурное сходство с клатрином и могут образовывать оболочку вокруг комплекса AP-5. [ 18 ] но ультраструктура этой шерсти неизвестна. Окраска АП-4 неизвестна. [ 19 ] [ а ]
Почти универсальной особенностью сборки оболочки является привлечение различных адаптерных комплексов к «донорской» мембране с помощью белка Arf1 . Единственным известным исключением является AP-2, который рекрутируется определенным липидом плазматической мембраны . [ 20 ]
Другая почти универсальная особенность сборки пальто заключается в том, что сначала набираются адаптеры, а затем они набирают пальто. Исключением является COPI, при котором 7 белков рекрутируются на мембрану в виде гептамера. [ 16 ]
Как показано на сопроводительном изображении, образование покрытой оболочки пузырька не происходит мгновенно, и значительная часть времени созревания используется для создания «абортивного» или «бесполезного» процесса. [ 21 ] взаимодействий до тех пор, пока одновременно не произойдет достаточное количество взаимодействий, позволяющее структуре продолжать развиваться. [ 22 ]
Последним этапом формирования транспортного пузырька является «отщипывание» его от донорской мембраны. Это требует энергии, но даже в хорошо изученном случае CCV не всем требуется динамин . На сопроводительной иллюстрации показан случай CCV AP-2, однако CCV AP-1 и AP-3 не используют динамин. [ 23 ]
Отбор грузовых молекул
[ редактировать ]То, какие молекулы-грузы включаются в везикулу определенного типа, зависит от конкретных взаимодействий. Некоторые из этих взаимодействий происходят напрямую с AP-комплексами, а некоторые опосредованно с «альтернативными адаптерами», как показано на этой диаграмме . [ 4 ] Например, мембранные белки могут иметь прямые взаимодействия, в то время как белки, растворимые в просвете донорской органеллы, связываются с AP-комплексами опосредованно, связываясь с мембранными белками, которые пересекают мембрану и связываются на своем просветном конце с желаемой молекулой-грузом. Молекулы, которые не должны включаться в везикулу, по-видимому, исключаются из-за «молекулярной скученности». [ 24 ]
«Сигналы» или аминокислотные «мотивы» в белках-грузах, которые взаимодействуют с белками-адаптерами, могут быть очень короткими. Например, одним хорошо известным примером является мотив дилейцина остатком лейцина , в котором за аминокислотным (аа) сразу следует другой остаток лейцина или изолейцина . [ 25 ] [ б ] Еще более простым примером является сигнал на основе тирозина , который представляет собой YxxØ ( остаток ирозина отделен 2 аминокислотными остатками от другого объемистого гидрофобного аминокислотного остатка). На прилагаемом рисунке показано, как небольшая часть белка может специфически взаимодействовать с другим белком, поэтому эти короткие сигнальные мотивы не должны вызывать удивления. [ 26 ] Вид сравнения последовательностей, используемый, частично, для определения этих мотивов. [ 10 ]
В некоторых случаях посттрансляционные модификации , такие как фосфорилирование (показано на рисунке), важны для распознавания груза.
Болезни
[ редактировать ]адаптерные болезни . Были рассмотрены [ 6 ]
AP-2/CCVs участвуют в аутосомно-рецессивной гиперхолестеринемии посредством ассоциированного белка-адаптера рецептора липопротеинов низкой плотности 1 . [ 27 ] [ 28 ]
Ретромер участвует в переработке компонентов плазматической мембраны. На важность этой переработки в синапсе намекает один из рисунков в галерее. Существует как минимум три способа, которыми дисфункция ретромера может способствовать расстройствам головного мозга, включая болезни Альцгеймера и Паркинсона. [ 7 ]
AP-5 является самым недавно описанным комплексом, и одной из причин, подтверждающих идею о том, что это подлинный адаптерный комплекс, является то, что он связан с наследственной спастической параплегией . [ 18 ] как и АП-4. [ 6 ] AP-1 связан с синдромом МЕДНИК . AP-3 связан с синдромом Германского-Пудлака . COPI связан с аутоиммунным заболеванием . [ 29 ] COPII связан с кранио-лентикуло-шовной дисплазией . Один из белков GGA может быть вовлечен в болезнь Альцгеймера. [ 30 ]
Галерея
[ редактировать ]См. также
[ редактировать ]Примечания
[ редактировать ]- ^ AP-4 гораздо менее распространен, чем другие комплексы AP, и отсутствует в некоторых модельных организмах, что затрудняет биохимический и генетический анализ.
- ^ Полный мотив «на основе дилейцина» - это (D/E) XXXL (L/I), где X представляет собой любой аа, а D/E представляет собой остатки аспарагиновой или глутаминовой кислоты .
Ссылки
[ редактировать ]- ^ Другой взгляд на 5 комплексов АП можно увидеть здесь" Маттера Р., Гуардия К.М., Сидху С.С., Бонифачино Дж.С. (2015). «Рисунок 1: Выделение тепсина как интерактора AP-4» . J Биол Хим . 290 (52): 30736–49. дои : 10.1074/jbc.M115.683409 . ПМЦ 4692204 . ПМИД 26542808 .
- ^ Бонифачино Дж.С. (2014). «Адапторные белки, участвующие в поляризованной сортировке» . Журнал клеточной биологии . 204 (1): 7–17. дои : 10.1083/jcb.201310021 . ПМЦ 3882786 . ПМИД 24395635 .
- ^ Jump up to: а б Пачковски Дж. Э., Ричардсон BC, Фромм Дж. К. (2015). «Грузовые адаптеры: структуры освещают механизмы, регулирующие биогенез везикул» . Тенденции в клеточной биологии . 25 (7): 408–16. дои : 10.1016/j.tcb.2015.02.005 . ПМЦ 4475447 . ПМИД 25795254 .
- ^ Jump up to: а б с д и Робинсон М.С. (2015). «Сорок лет везикул, покрытых клатрином» (PDF) . Трафик . 16 (12): 1210–38. дои : 10.1111/tra.12335 . ПМИД 26403691 . S2CID 13761396 .
- ^ Де Маттеис М.А., Луини А. (сентябрь 2011 г.). «Менделевские нарушения мембранного транспорта». Медицинский журнал Новой Англии . 365 (10): 927–38. дои : 10.1056/NEJMra0910494 . ПМИД 21899453 .
- ^ Jump up to: а б с Бонифачино Дж. (28 января 2014 г.). «Адапторные болезни: соединение клеточной биологии и медицины» . videocast.nih.gov . Национальные институты здравоохранения . Проверено 15 апреля 2017 г.
- ^ Jump up to: а б Малый С.А., Пецко Г.А. (март 2015 г.). «Ретромер при болезни Альцгеймера, болезни Паркинсона и других неврологических расстройствах». Обзоры природы. Нейронаука . 16 (3): 126–32. дои : 10.1038/nrn3896 . ПМИД 25669742 . S2CID 5166260 .
- ^ "здесь" .
- ^ МакМахон, Харви Т.; Галоп, Дженнифер Л. (2005). "здесь". Природа . 438 (7068): 590–596. дои : 10.1038/nature04396 . ПМИД 16319878 . S2CID 4319503 .
- ^ Jump up to: а б с д Маттера Р., Гуардия К.М., Сидху С.С., Бонифачино Дж.С. (2015). «Взаимодействие бивалентного мотива и уха опосредует ассоциацию акцессорного белка тепсина с адаптерным комплексом AP-4» . Журнал биологической химии . 290 (52): 30736–49. дои : 10.1074/jbc.M115.683409 . ПМЦ 4692204 . ПМИД 26542808 .
- ^ Jump up to: а б с д Херст Дж., Шлахт А., Норкотт Дж.П., Трейнор Д., Блумфилд Дж., Антробус Р., Кей Р.Р., Дакс Дж.Б., Робинсон М.С. (2014). «Характеристика TSET, древнего и широко распространенного комплекса мембранного транспорта» . электронная жизнь . 3 : e02866. doi : 10.7554/eLife.02866 . ПМК 4031984 . ПМИД 24867644 .
- ^ Берд С., Каллен П.Дж. (2014). «Ретромер: мастер сортировки эндосом» . Перспективы Колд-Спринг-Харбор в биологии . 6 (2): а016774. doi : 10.1101/cshperspect.a016774 . ПМЦ 3941235 . ПМИД 24492709 .
- ^ Тан Дж., Эвин Дж. (2012). «Транспорт фермента 1, расщепляющего АРР-участок, и патогенез болезни Альцгеймера» . Журнал нейрохимии . 120 (6): 869–80. дои : 10.1111/j.1471-4159.2011.07623.x . ПМИД 22171895 . S2CID 44408418 .
- ^ Занетти Г., Принц С., Даум С., Мейстер А., Шекман Р., Басия К., Бриггс Дж.А. (2013). «Строение транспортно-везикулярной оболочки COPII, собранной на мембранах» . электронная жизнь . 2 : е00951. doi : 10.7554/eLife.00951 . ПМЦ 3778437 . ПМИД 24062940 .
- ^ Промпонас В.Дж., Кацани К.Р., Бленкоу Б.Дж., Узунис Калифорния (2016). «Доказательства последовательности общего происхождения коатомеров эндомембран эукариот» . Научные отчеты . 6 : 22311. Бибкод : 2016NatSR...622311P . дои : 10.1038/srep22311 . ПМЦ 4773986 . ПМИД 26931514 .
- ^ Jump up to: а б Файни М., Бек Р., Виланд Ф.Т., Бриггс Дж.А. (июнь 2013 г.). «Оболочки везикул: строение, функции и общие принципы сборки». Тенденции в клеточной биологии . 23 (6): 279–88. дои : 10.1016/j.tcb.2013.01.005 . ПМИД 23414967 .
- ^ Джексон LP (август 2014 г.). «Структура и механизм биогенеза везикул COPI». Современное мнение в области клеточной биологии . 29 : 67–73. дои : 10.1016/j.ceb.2014.04.009 . ПМИД 24840894 .
- ^ Jump up to: а б Херст Дж., Борнер Г.Х., Эдгар Дж., Хейн М.Ю., Манн М., Бухгольц Ф., Антробус Р., Робинсон М.С. (2013). «Взаимодействие между AP-5 и наследственными белками спастической параплегии SPG11 и SPG15» . Молекулярная биология клетки . 24 (16): 2558–69. doi : 10.1091/mbc.E13-03-0170 . ПМЦ 3744948 . ПМИД 23825025 .
- ^ Фрейзер М.Н., Дэвис А.К., Волер М., Кендалл А.К., Борнер Г.Х., Чазин В.Дж., Робинсон М.С., Джексон Л.П. (2016). «Молекулярная основа взаимодействия между AP4 β4 и его акцессорным белком тепсином» . Трафик . 17 (4): 400–15. дои : 10.1111/tra.12375 . ПМЦ 4805503 . ПМИД 26756312 .
- ^ Ю Х, Брейтман М, Голдберг Дж (2012). «Структурный механизм Arf1-зависимого привлечения коатомера к мембранам» . Клетка . 148 (3): 530–42. дои : 10.1016/j.cell.2012.01.015 . ПМЦ 3285272 . ПМИД 22304919 .
- ^ Кирххаузен, Том. «Создание пузырей» . youtube.com . Гарвард.edu. Архивировано из оригинала 21 декабря 2021 г. Проверено 23 апреля 2017 г.
- ^ Кокуччи Э., Аге Ф., Булан С., Кирххаузен Т. (август 2012 г.). «Первые пять секунд жизни ямы, покрытой клатрином» . Клетка . 150 (3): 495–507. дои : 10.1016/j.cell.2012.05.047 . ПМК 3413093 . ПМИД 22863004 .
- ^ Курал С., Тачева-Григорова С.К., Булан С., Кокуччи Е., Бауст Т., Дуарте Д., Кирххаузен Т. (2012). «Динамика внутриклеточных клатрин/AP1- и клатрин/AP3-содержащих носителей» . Отчеты по ячейкам . 2 (5): 1111–9. дои : 10.1016/j.celrep.2012.09.025 . ПМЦ 3513667 . ПМИД 23103167 .
- ^ Херст Дж., Эдгар Дж.Р., Борнер Г.Х., Ли С., Салендер Д.А., Антробус Р., Робинсон М.С. (2015). «Вклад epsinR и гадкина во внутриклеточный трафик, опосредованный клатрином» . Молекулярная биология клетки . 26 (17): 3085–103. doi : 10.1091/mbc.E15-04-0245 . ПМЦ 4551321 . ПМИД 26179914 .
- ^ Маттера Р., Бём М., Чаудхури Р., Прабху Ю., Бонифачино Дж.С. (2011). «Сохранение и диверсификация распознавания сигнала дилейцина вариантами комплекса адаптерного белка (AP)» . Журнал биологической химии . 286 (3): 2022–30. дои : 10.1074/jbc.M110.197178 . ПМЦ 3023499 . ПМИД 21097499 .
- ^ Трауб Л.М., Бонифачино Дж.С. (2013). «Распознавание грузов при клатрин-опосредованном эндоцитозе» . Перспективы Колд-Спринг-Харбор в биологии . 5 (11): а016790. doi : 10.1101/cshperspect.a016790 . ПМЦ 3809577 . ПМИД 24186068 .
- ^ Интернет-менделевское наследование у человека (OMIM): 605747
- ^ «Ген Энтрез: белок-адаптер 1 рецептора липопротеина низкой плотности LDLRAP1» .
- ^ Интернет-менделевское наследование у человека (OMIM): 616414
- ^ Интернет-менделевское наследование у человека (OMIM): 606006