Молекулярная эволюция
| Часть серии о |
| Эволюционная биология |
|---|
 |
Молекулярная эволюция описывает, как унаследованная ДНК и/или РНК изменяются с течением эволюционного времени, а также последствия этого для белков и других компонентов клеток и организмов . Молекулярная эволюция лежит в основе филогенетических подходов к описанию древа жизни . Молекулярная эволюция пересекается с популяционной генетикой , особенно в более коротких временных масштабах. Темы молекулярной эволюции включают происхождение новых генов, генетическую природу сложных признаков , генетическую основу адаптации и видообразования , эволюцию развития , а также закономерности и процессы, лежащие в основе геномных изменений в ходе эволюции.
История [ править ]
История молекулярной эволюции начинается в начале 20-го века со сравнительной биохимии и использования методов «отпечатков пальцев», таких как иммунные анализы, гель-электрофорез и бумажная хроматография в 1950-х годах для исследования гомологичных белков . [1] [2] Появление секвенирования белков позволило молекулярным биологам создавать филогении на основе сравнения последовательностей и использовать различия между гомологичными последовательностями в качестве молекулярных часов для оценки времени, прошедшего с момента появления самого недавнего общего предка . [3] [1] Удивительно большое количество молекулярных различий внутри видов и между видами вдохновило на создание нейтральной теории молекулярной эволюции в конце 1960-х годов. [4] [5] [6] Нейтральная теория также обеспечила теоретическую основу для молекулярных часов , хотя это не требуется для достоверности часов. После 1970-х годов секвенирование нуклеиновых кислот позволило молекулярной эволюции выйти за рамки белков и перейти к высококонсервативным последовательностям рибосомальных РНК , что стало основой переосмысления ранней истории жизни . [1] Общество молекулярной биологии и эволюции было основано в 1982 году.
Молекулярная филогенетика
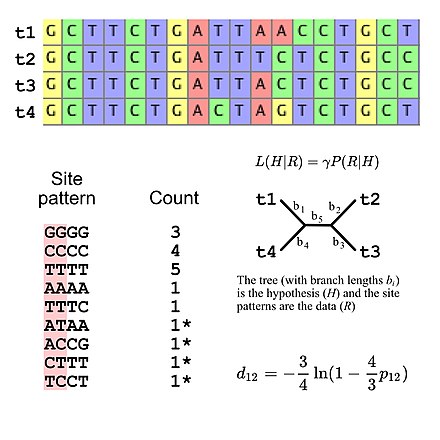
Молекулярная филогенетика использует последовательности ДНК , РНК или белков для решения вопросов систематики , т. е. их правильной научной классификации с точки зрения эволюционной истории . Результат молекулярно- филогенетического анализа выражается в виде филогенетического дерева . Филогенетический вывод проводится с использованием данных секвенирования ДНК . Это выравнивается для определения того, какие сайты являются гомологичными . Модель замещения описывает, какие закономерности будут распространены или редки. Затем сложный вычислительный вывод используется для создания одного или нескольких правдоподобных деревьев.
Некоторые филогенетические методы учитывают различия между участками и ветвями деревьев . Различные гены, например, гемоглобин или цитохром с , обычно развиваются с разной скоростью . [7] Эти скорости относительно постоянны во времени (например, гемоглобин не развивается с той же скоростью, что и цитохром с, но гемоглобины человека, мышей и т. д. имеют сопоставимые скорости эволюции), хотя быстрая эволюция вдоль одной ветви может указывать на усиление направленного отбора. на этой ветке. [8] Очищающий отбор приводит к тому, что функционально важные области развиваются медленнее, а аминокислотные замены с участием сходных аминокислот происходят чаще, чем разнородные. [7]

семейства генов Эволюция

Дупликация генов может производить несколько гомологичных белков (паралогов) в пределах одного и того же вида. Филогенетический анализ белков показал, как белки развиваются и меняют свою структуру и функции с течением времени. [9] [10]
Например, рибонуклеотидредуктаза (РНР) развила множество структурных и функциональных вариантов. RNR класса I используют субъединицу ферритина и различаются металлом, который они используют в качестве кофакторов. В класса II RNR тиильный радикал генерируется с использованием кофактора аденозилкобаламина , и эти ферменты не требуют дополнительных субъединиц (в отличие от класса I, который это делает). В RNR класса III тиильный радикал генерируется с использованием S-аденозилметионина, связанного с кластером [ 4Fe-4S ]. То есть внутри одного семейства белков могут развиваться многочисленные структурные и функциональные механизмы. [11]
В ходе исследования, подтверждающего концепцию, Бхаттачарья и его коллеги превратили миоглобин , неферментативный белок, запасающий кислород, в высокоэффективную элиминазу Кемпа , используя всего три мутации . Это показывает, что для радикального изменения функции белка достаточно лишь нескольких мутаций. [12] Направленная эволюция — это попытка создать белки, используя методы, вдохновленные молекулярной эволюцией.
Молекулярная эволюция на одном сайте [ править ]
Изменение в одном локусе начинается с новой мутации , которая может закрепиться в результате некоторой комбинации естественного отбора , генетического дрейфа и генной конверсии .
Мутация [ править ]

Мутации — это постоянные, передаваемые изменения генетического материала ( ДНК или РНК ) клетки или вируса . Мутации возникают в результате ошибок репликации ДНК во время деления клеток , а также в результате воздействия радиации , химических веществ, других стрессовых факторов окружающей среды, вирусов или мобильных элементов . Когда точечные мутации только одной пары оснований ДНК попадают в область, кодирующую белок , они характеризуются тем, являются ли они синонимичными (не меняют аминокислотную последовательность) или несинонимичными. Другие типы мутаций изменяют более крупные сегменты ДНК и могут вызывать дупликации, вставки, делеции, инверсии и транслокации. [13]
Распределение скоростей различных видов мутаций называется «спектром мутаций» (см. приложение Б [14] ). Мутации разных типов происходят с очень разной скоростью. Частота точечных мутаций для большинства организмов очень низкая, примерно 10. −9 до 10 −8 на сайт на поколение, [15] хотя некоторые вирусы имеют более высокую частоту мутаций, порядка 10 −6 на сайт на поколение. [16] Переходы (А ↔ G или С ↔ Т) встречаются чаще, чем трансверсии ( пурин (аденин или гуанин)) ↔ пиримидин (цитозин или тимин, или в РНК урацил)). [17] Возможно, наиболее распространенным типом мутации у человека является изменение длины короткого тандемного повтора (например, CAG-повторов, лежащих в основе различных мутаций, связанных с заболеванием). Такие мутации STR могут возникать с частотой порядка 10 −3 на поколение. [18]
Разная частота мутаций разных типов может играть важную роль в эволюции через смещение при внесении изменчивости (смещение прибытия), способствуя параллелизму, тенденциям и различиям в судоходности адаптивных ландшафтов. [19] [20] Предвзятость мутаций вносит систематический или предсказуемый вклад в параллельную эволюцию . [14] С 1960-х годов содержание геномных GC отражает мутационные тенденции. считалось, что [21] [22] Мутационные искажения также способствуют смещению использования кодонов . [23] Хотя такие гипотезы часто связаны с нейтральностью, недавние теоретические и эмпирические результаты установили, что мутационные тенденции могут влиять как на нейтральную, так и на адаптивную эволюцию через смещение при введении вариаций (смещение прибытия).
Выбор [ править ]
Отбор может происходить, когда аллель придает большую приспособленность среднестатистическому индивидууму , т. е. большую способность к выживанию или размножению, чем несет ее. Селекционистский подход подчеркивает , например, что отклонения в использовании кодонов обусловлены, по крайней мере частично, способностью даже слабого отбора формировать молекулярную эволюцию. [24]
Отбор может также действовать на уровне генов в ущерб приспособленности организма, что приводит к внутригеномному конфликту . могут иметь селективное преимущество, Это связано с тем, что эгоистичные генетические элементы несмотря на стоимость хозяина. Примеры таких эгоистичных элементов включают мобильные элементы , мейотические драйверы и эгоистичные митохондрии .
Отбор можно обнаружить с помощью соотношения Ka/Ks , критерия Макдональда-Крейтмана . Быстрая адаптивная эволюция часто наблюдается у генов, вовлеченных во внутригеномный конфликт , половую антагонистическую коэволюцию и иммунную систему .
Генетический дрейф [ править ]
Генетический дрейф — это изменение частот аллелей от одного поколения к другому из-за стохастических эффектов случайной выборки в конечных популяциях. Эти эффекты могут накапливаться до тех пор, пока мутация не зафиксируется в популяции . Для нейтральных мутаций скорость фиксации на поколение равна скорости мутации на репликацию. Таким образом, относительно постоянная скорость мутаций обеспечивает постоянную скорость изменений в каждом поколении (молекулярные часы).
Также можно исправить незначительно вредные мутации с коэффициентом отбора менее порогового значения 1/ эффективный размер популяции . Многие геномные особенности приписывают накоплению почти нейтральных вредных мутаций в результате небольших эффективных размеров популяции. [25] При меньшем эффективном размере популяции большее разнообразие мутаций будет вести себя так, как если бы они были нейтральными из-за неэффективности отбора.
Конверсия генов [ править ]
Конверсия генов происходит во время рекомбинации, когда повреждения нуклеотидов восстанавливаются с использованием гомологичной области генома в качестве матрицы. Это может быть предвзятый процесс, т.е. один аллель может иметь более высокую вероятность стать донором, чем другой, в случае конверсии гена. В частности, конверсия генов, основанная на GC, имеет тенденцию увеличивать содержание GC в геномах, особенно в регионах с более высокими скоростями рекомбинации. [26] Есть также свидетельства смещения GC в процессе исправления несоответствий. [27] Считается, что это может быть адаптацией к высокой скорости дезаминирования метилцитозина, которая может приводить к переходам C→T.
Динамика предвзятой конверсии генов напоминает динамику естественного отбора: частота предпочтительного аллеля имеет тенденцию к экспоненциальному увеличению частоты, когда он встречается редко.
Архитектура генома [ править ]
Размер генома [ править ]
На размер генома влияет количество повторяющейся ДНК, а также количество генов в организме. Некоторые организмы, такие как большинство бактерий, Drosophila и Arabidopsis, имеют особенно компактные геномы с небольшим количеством повторяющегося содержимого или некодирующей ДНК. Другие организмы, такие как млекопитающие или кукуруза, имеют большое количество повторяющейся ДНК, длинные интроны и значительные расстояния между генами. Парадокс C-значения относится к отсутствию корреляции между «сложностью» организма и размером генома. Объяснения так называемого парадокса двоякие. Во-первых, повторяющиеся генетические элементы могут составлять большие части генома многих организмов, тем самым увеличивая содержание ДНК в гаплоидном геноме. Повторяющиеся генетические элементы часто происходят от мобильных элементов .
Во-вторых, количество генов не обязательно указывает на количество стадий развития или типов тканей в организме. Организм с небольшим количеством стадий развития или типов тканей может иметь большое количество генов, которые влияют на фенотипы, не связанные с развитием, увеличивая содержание генов по сравнению с семействами генов развития.
Нейтральные объяснения размера генома предполагают, что когда размеры популяции невелики, многие мутации становятся почти нейтральными. Следовательно, в небольших популяциях повторяющийся контент и другая «мусорная» ДНК могут накапливаться, не ставя организм в невыгодное конкурентное положение. Существует мало доказательств того, что размер генома у многоклеточных эукариот находится под сильным широким отбором. Размер генома, независимо от содержания генов, плохо коррелирует с большинством физиологических признаков, и многие эукариоты, включая млекопитающих, содержат очень большое количество повторяющейся ДНК.
Однако птицы , вероятно, подверглись сильному отбору по уменьшению размера генома в ответ на изменение энергетических потребностей для полета. Птицы, в отличие от людей, производят ядросодержащие эритроциты, а более крупные ядра приводят к снижению уровня транспорта кислорода. Метаболизм птиц намного выше, чем у млекопитающих, в основном благодаря полету, а потребность в кислороде высока. Следовательно, большинство птиц имеют небольшие, компактные геномы с небольшим количеством повторяющихся элементов. Косвенные данные позволяют предположить, что нептичьи тероподы-динозавры были предками современных птиц. [28] также имели уменьшенные размеры генома, что соответствовало эндотермии и высоким энергетическим потребностям для скорости бега. Многие бактерии также подверглись отбору из-за небольшого размера генома, поскольку время репликации и потребление энергии тесно коррелируют с приспособленностью.
Число и организация хромосом [ править ]
Муравей Myrmecia pilosula имеет только одну пару хромосом. [29] тогда как папоротник змеевидный Ophioglossum reticulatum имеет до 1260 хромосом. [30] Число хромосом в геноме организма не обязательно коррелирует с количеством ДНК в его геноме. по всему геному Объем рекомбинации напрямую контролируется количеством хромосом, с одним кроссинговером на хромосому или на плечо хромосомы, в зависимости от вида. [31]
Изменения числа хромосом могут играть ключевую роль в видообразовании , поскольку различное число хромосом может служить барьером для размножения у гибридов. Человеческая хромосома 2 была создана в результате слияния двух хромосом шимпанзе и до сих пор содержит центральные теломеры , а также рудиментарную вторую центромеру . Полиплоидия , особенно аллополиплоидия, которая часто встречается у растений, также может приводить к репродуктивной несовместимости с родительскими видами. Голубые бабочки Agrodiatus имеют разнообразное число хромосом в диапазоне от n = 10 до n = 134, а также имеют один из самых высоких показателей видообразования, выявленных на сегодняшний день. [32]
В геномах реснитчатых каждый ген находится в отдельных хромосомах.
Органеллы [ править ]
Помимо ядерного генома , органеллы эндосимбионтов содержат собственный генетический материал. ДНК митохондрий и хлоропластов варьируется в зависимости от таксона, но мембраносвязанные белки , особенно компоненты цепи переноса электронов , чаще всего кодируются в органелле. Хлоропласты и митохондрии у большинства видов наследуются по материнской линии, поскольку органеллы должны пройти через яйцеклетку . Известно , что некоторые виды мидий , за редким исключением, наследуют митохондрии от отца к сыну.
Происхождение новых генов [ править ]
Новые гены возникают в результате нескольких различных генетических механизмов, включая дупликацию гена , рождение гена de novo , ретротранспозицию , образование химерных генов , рекрутирование некодирующей последовательности в существующий ген и усечение гена.
Дупликация генов изначально приводит к избыточности. Однако дублированные последовательности генов могут мутировать, развивая новые функции или специализируясь , так что новый ген выполняет подмножество исходных наследственных функций. Ретротранспозиция дублирует гены путем копирования мРНК в ДНК и вставки ее в геном. Ретрогены обычно встраиваются в новые места генома, не имея интронов . а иногда и разрабатывать новые модели и функции выражения.
Химерные гены образуются, когда дупликация, делеция или неполная ретротранспозиция объединяют части двух разных кодирующих последовательностей для получения новой последовательности гена. Химеры часто вызывают регуляторные изменения и могут перемещать белковые домены для выполнения новых адаптивных функций.
de novo Рождение генов может привести к появлению генов, кодирующих белок, и некодирующих генов из ранее нефункциональной ДНК. [33] Например, Левин и его коллеги сообщили о происхождении пяти новых генов в геноме D. melanogaster . [34] [35] Подобное происхождение генов de novo было также показано и у других организмов, таких как дрожжи, [36] рис [37] и люди. [38] Гены de novo могут развиваться из ложных транскриптов, которые уже экспрессируются на низких уровнях. [39]
нейтральная Конструктивная эволюция
Конструктивная нейтральная эволюция (CNE) объясняет, что сложные системы могут возникать и распространяться в популяции посредством нейтральных переходов с принципами избыточной мощности, предварительного подавления и храповика. [40] [41] [42] и он применялся в самых разных областях: от происхождения сплайсосом до сложной взаимозависимости микробных сообществ . [43] [44] [45]
Журналы и общества [ править ]
Общество молекулярной биологии и эволюции издает журналы «Молекулярная биология и эволюция» и «Геномная биология и эволюция» и проводит ежегодное международное собрание. Другие журналы, посвященные молекулярной эволюции, включают Journal of Molecular Evolution и Molecular Phylogenetics and Evolution . Исследования молекулярной эволюции также публикуются в журналах по генетике , молекулярной биологии , геномике , систематике и эволюционной биологии .
См. также [ править ]
- Эволюция
- E. coli Эксперимент по долгосрочной эволюции
- Эволюционная физиология
- Геномная организация
- Эволюция генома
- Гетеротахия
- История молекулярной эволюции
- Горизонтальный перенос генов
- Эволюция человека
- Молекулярные часы
- Молекулярная палеонтология
- Почти нейтральная теория молекулярной эволюции
- Нейтральная теория молекулярной эволюции
- Нуклеотидное разнообразие
- Филогенетические сравнительные методы
- Филогенетика
- Популяционная генетика
- Выбор
Ссылки [ править ]
- ^ Jump up to: Перейти обратно: а б с Дитрих М.Р. (1998). «Парадокс и убеждение: обсуждение места молекулярной эволюции в эволюционной биологии». Журнал истории биологии . 31 (1): 85–111. дои : 10.1023/А:1004257523100 . ПМИД 11619919 . S2CID 29935487 .
- ^ Хаген Дж.Б. (1999). «Натуралисты, молекулярные биологи и проблемы молекулярной эволюции». Журнал истории биологии . 32 (2): 321–341. дои : 10.1023/А:1004660202226 . ПМИД 11624208 . S2CID 26994015 .
- ^ Цукеркандль, Эмиль; Полинг, Лайнус (март 1965 г.). «Молекулы как документы эволюционной истории». Журнал теоретической биологии . 8 (2): 357–366. Бибкод : 1965JThBi...8..357Z . дои : 10.1016/0022-5193(65)90083-4 . ПМИД 5876245 .
- ^ Кимура М. (февраль 1968 г.). «Скорость эволюции на молекулярном уровне». Природа . 217 (5129): 624–626. Бибкод : 1968Natur.217..624K . дои : 10.1038/217624a0 . ПМИД 5637732 . S2CID 4161261 .
- ^ Кинг Дж.Л., Джукс Т.Х. (май 1969 г.). «Недарвиновская эволюция». Наука . 164 (3881): 788–798. Бибкод : 1969Sci...164..788L . дои : 10.1126/science.164.3881.788 . ПМИД 5767777 .
- ^ Кимура, М. (1983). Нейтральная теория молекулярной эволюции . Издательство Кембриджского университета , Кембридж. ISBN 0-521-23109-4 .
- ^ Jump up to: Перейти обратно: а б Фэй Дж. К., Ву CI (2003). «Расхождение последовательностей, функциональные ограничения и отбор в эволюции белков» . Ежегодный обзор геномики и генетики человека . 4 : 213–235. дои : 10.1146/annurev.genom.4.020303.162528 . ПМИД 14527302 . S2CID 6360375 .
- ^ Альварес-Карретеро, Сандра; Капли, Пасхалия; Ян, Цзыхэн (4 апреля 2023 г.). «Руководство для начинающих по использованию PAML для обнаружения положительного отбора» . Молекулярная биология и эволюция . 40 (4). дои : 10.1093/molbev/msad041 . ПМЦ 10127084 . ПМИД 37096789 .
- ^ Ханукоглу I (февраль 2017 г.). «Натриевые каналы типа ASIC и ENaC: конформационные состояния и структуры ионно-селективных фильтров» . Журнал ФЭБС . 284 (4): 525–545. дои : 10.1111/февраль 13840 . ПМИД 27580245 . S2CID 24402104 .
- ^ Ханукоглу I, Ханукоглу А (апрель 2016 г.). «Семейство эпителиальных натриевых каналов (ENaC): филогения, структура-функция, распределение в тканях и связанные с ними наследственные заболевания» . Джин . 579 (2): 95–132. дои : 10.1016/j.gene.2015.12.061 . ПМЦ 4756657 . ПМИД 26772908 .
- ^ Бурним А.А., Спенс М.А., Сюй Д., Джексон С.Дж., Андо Н. (сентябрь 2022 г.). Бен-Тал Н., Вайгель Д., Бен-Тал Н., Стуббе Дж., Хофер А. (ред.). «Комплексный филогенетический анализ семейства рибонуклеотидредуктаз обнаруживает предковую кладу» . электронная жизнь . 11 : e79790. doi : 10.7554/eLife.79790 . ПМК 9531940 . ПМИД 36047668 .
- ^ Бхаттачарья С., Маргеритис Э.Г., Такахаши К., Кулеша А., Д'Суза А., Ким И. и др. (октябрь 2022 г.). «Направленная эволюция под контролем ЯМР» . Природа . 610 (7931): 389–393. Бибкод : 2022Natur.610..389B . дои : 10.1038/s41586-022-05278-9 . ПМЦ 10116341 . ПМИД 36198791 . S2CID 245067145 .
- ^ Ян, Дж. (23 марта 2016 г.). Что такое генетические мутации? Получено с https://www.singerinstruments.com/resource/what-are-genetic-mutation/ .
- ^ Jump up to: Перейти обратно: а б А. Штольцфус (2021). Мутация, случайность и эволюция . Оксфорд, Оксфорд.
- ^ Ван, Игуань; Оббард, Даррен Дж. (19 июля 2023 г.). «Экспериментальные оценки частоты мутаций зародышевой линии у эукариот: филогенетический метаанализ» . Письма об эволюции . 7 (4): 216–226. дои : 10.1093/evlett/qrad027 . hdl : 20.500.11820/8ffd5b76-77ae-4764-ae31-de2fb8aa35cf . ПМЦ 10355183 . ПМИД 37475753 .
- ^ Пек, Кайла М.; Лоринг, Адам С. (15 июля 2018 г.). «Сложности скорости вирусных мутаций» . Журнал вирусологии . 92 (14): e01031-17. дои : 10.1128/JVI.01031-17 . ПМК 6026756 . ПМИД 29720522 .
- ^ «Переходы против трансверсий» .
- ^ Дж. Л. Вебер и К. Вонг (1993). «Мутация коротких тандемных повторов человека». Хум Мол Жене . 2 (8): 1123–8. дои : 10.1093/hmg/2.8.1123 . ПМИД 8401493 .
- ^ А. В. Кано и Дж. Л. Пейн (2020). «Предвзятость мутаций взаимодействует с предвзятостью состава, влияя на адаптивную эволюцию» . PLOS Вычислительная биология . 16 (9): e1008296. Бибкод : 2020PLSCB..16E8296C . дои : 10.1371/journal.pcbi.1008296 . ПМЦ 7571706 . ПМИД 32986712 .
- ^ М. Ней (2013). Эволюция, управляемая мутациями . Издательство Оксфордского университета.
- ^ Э. Фриз (1962). «Об эволюции основного состава ДНК». Дж. Теория. Биол . 3 (1): 82–101. Бибкод : 1962JThBi...3...82F . дои : 10.1016/S0022-5193(62)80005-8 .
В этой связи не имеет значения, был ли отбор незначительным или самоотменяющимся.
- ^ Н. Суэока (1962). «О генетических основах изменчивости и гетерогенности базового состава ДНК» . Учеб. Натл. акад. наук. США . 48 (4): 582–592. Бибкод : 1962ПНАС...48..582С . дои : 10.1073/pnas.48.4.582 . ПМК 220819 . ПМИД 13918161 .
- ^ А. Штольцфус и Л.Я. Ямпольский (2009). «Восхождение на гору вероятно: мутация как причина неслучайности в эволюции» . Дж. Херед . 100 (5): 637–47. дои : 10.1093/jhered/esp048 . ПМИД 19625453 .
- ^ Хершберг Р., Петров Д.А. (декабрь 2008 г.). «Отбор по смещению кодонов». Ежегодный обзор генетики . 42 (1): 287–299. дои : 10.1146/annurev.genet.42.110807.091442 . ПМИД 18983258 . S2CID 7085012 .
- ^ Линч М. (2007). Истоки архитектуры генома . Синауэр. ISBN 978-0-87893-484-3 .
- ^ Дюре Л., Галтье Н. (2009). «Предвзятая конверсия генов и эволюция геномных ландшафтов млекопитающих». Ежегодный обзор геномики и генетики человека . 10 : 285–311. doi : 10.1146/annurev-genom-082908-150001 . ПМИД 19630562 .
- ^ Галтье Н., Пигано Г., Муширу Д., Дюре Л. (октябрь 2001 г.). «Эволюция содержания GC в геномах млекопитающих: гипотеза предвзятой конверсии генов» . Генетика . 159 (2): 907–911. дои : 10.1093/генетика/159.2.907 . ПМК 1461818 . ПМИД 11693127 .
- ^ Орган CL, Шедлок А.М., Мид А., Пейджел М., Эдвардс С.В. (март 2007 г.). «Происхождение размера и структуры птичьего генома у нептичьих динозавров». Природа . 446 (7132): 180–184. Бибкод : 2007Natur.446..180O . дои : 10.1038/nature05621 . ПМИД 17344851 . S2CID 3031794 .
- ^ Кросланд М.В., Крозье Р.Х. (март 1986 г.). «Myrmecia pilosula, муравей только с одной парой хромосом». Наука . 231 (4743): 1278. Бибкод : 1986Sci...231.1278C . дои : 10.1126/science.231.4743.1278 . ПМИД 17839565 . S2CID 25465053 .
- ^ Герардус Дж. Груббен (2004). Овощи . ПРОТА. стр. 404 . ISBN 978-90-5782-147-9 . Проверено 10 марта 2013 г.
- ^ Пардо-Мануэль де Вильена, Фернандо; Сапиенца, Кармен (апрель 2001 г.). «Рекомбинация пропорциональна числу плеч хромосом у млекопитающих». Геном млекопитающих . 12 (4): 318–322. дои : 10.1007/s003350020005 . ПМИД 11309665 .
- ^ Кандул Н.П., Лухтанов В.А., Пирс Н.Е. (март 2007 г.). «Кариотипическое разнообразие и видообразование бабочек Agrodiaetus» . Эволюция; Международный журнал органической эволюции . 61 (3): 546–559. дои : 10.1111/j.1558-5646.2007.00046.x . ПМИД 17348919 .
- ^ МакЛисахт А., Герцони Д. (сентябрь 2015 г.). «Новые гены из некодирующей последовательности: роль генов, кодирующих белки de novo, в эволюционных инновациях эукариот» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 370 (1678): 20140332. doi : 10.1098/rstb.2014.0332 . ПМЦ 4571571 . ПМИД 26323763 .
- ^ Левин М.Т., Джонс CD, Керн А.Д., Линдфорс Х.А., Бегун DJ (июнь 2006 г.). «Новые гены, полученные из некодирующей ДНК Drosophila melanogaster, часто сцеплены с Х-хромосомой и демонстрируют предвзятую экспрессию семенников» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (26): 9935–9939. Бибкод : 2006PNAS..103.9935L . дои : 10.1073/pnas.0509809103 . ПМК 1502557 . ПМИД 16777968 .
- ^ Чжоу Ц, Чжан Г, Чжан Ю, Сюй С, Чжао Р, Чжан Цз и др. (сентябрь 2008 г.). «О происхождении новых генов у дрозофилы» . Геномные исследования . 18 (9): 1446–1455. дои : 10.1101/гр.076588.108 . ПМК 2527705 . ПМИД 18550802 .
- ^ Цай Дж., Чжао Р., Цзян Х., Ван В. (май 2008 г.). «Происхождение de novo нового гена, кодирующего белок, у Saccharomyces cerevisiae» . Генетика . 179 (1): 487–496. doi : 10.1534/genetics.107.084491 . ПМК 2390625 . ПМИД 18493065 .
- ^ Сяо В, Лю Х, Ли Ю, Ли Х, Сюй С, Лонг М, Ван С (2009). Эль-Шеми ХА (ред.). «Ген риса, возникший de novo, негативно регулирует защитную реакцию, вызванную патогенами» . ПЛОС ОДИН . 4 (2): e4603. Бибкод : 2009PLoSO...4.4603X . дои : 10.1371/journal.pone.0004603 . ПМЦ 2643483 . ПМИД 19240804 .
- ^ Ноулз Д.Г., Маклизат А. (октябрь 2009 г.). «Недавнее происхождение генов, кодирующих человеческие белки», de novo . Геномные исследования . 19 (10): 1752–1759. дои : 10.1101/гр.095026.109 . ПМЦ 2765279 . ПМИД 19726446 .
- ^ Уилсон Б.А., Мэйсел Дж (2011). «Предположительно некодирующие транскрипты обнаруживают обширную связь с рибосомами» . Геномная биология и эволюция . 3 : 1245–1252. дои : 10.1093/gbe/evr099 . ПМК 3209793 . ПМИД 21948395 .
- ^ Штольцфус А (август 1999 г.). «О возможности конструктивной нейтральной эволюции». Журнал молекулярной эволюции . 49 (2): 169–181. Бибкод : 1999JMolE..49..169S . дои : 10.1007/PL00006540 . ПМИД 10441669 . S2CID 1743092 .
- ^ Штольцфус А (октябрь 2012 г.). «Конструктивная нейтральная эволюция: исследование любопытного противоречия эволюционной теории» . Биология Директ . 7 (1): 35. дои : 10.1186/1745-6150-7-35 . ПМЦ 3534586 . ПМИД 23062217 .
- ^ Муньос-Гомес С.А., Билоликар Г., Видеман Дж.Г., Гейлер-Самеротт К. (апрель 2021 г.). «Конструктивная нейтральная эволюция 20 лет спустя» . Журнал молекулярной эволюции . 89 (3): 172–182. Бибкод : 2021JMolE..89..172M . дои : 10.1007/s00239-021-09996-y . ПМЦ 7982386 . ПМИД 33604782 .
- ^ Лукеш Дж., Арчибальд Дж.М., Килинг П.Дж., Дулиттл В.Ф., Грей М.В. (июль 2011 г.). «Как нейтральный эволюционный храповик может усложнить клетку». ИУБМБ Жизнь . 63 (7): 528–537. дои : 10.1002/iub.489 . ПМИД 21698757 . S2CID 7306575 .
- ^ Воссеберг Дж., Снел Б. (декабрь 2017 г.). «Одомашнивание самосплайсинговых интронов во время эукариогенеза: появление сложного сплайсосомного аппарата» . Биология Директ . 12 (1): 30. дои : 10.1186/s13062-017-0201-6 . ПМК 5709842 . ПМИД 29191215 .
- ^ Брюне Т.Д., Дулиттл В.Ф. (19 марта 2018 г.). «Общность конструктивной нейтральной эволюции» . Биология и философия . 33 (1): 2. doi : 10.1007/s10539-018-9614-6 . ISSN 1572-8404 . S2CID 90290787 .
Дальнейшее чтение [ править ]
- Ли WH (2006). Молекулярная эволюция . Синауэр. ISBN 0-87893-480-4 .
- Линч М. (2007). Истоки архитектуры генома . Синауэр. ISBN 978-0-87893-484-3 .
- Мейер А., ван де Пер Ю., ред. (2003). Эволюция генома: дупликация генов и геномов и возникновение новых функций генов . Дордрехт: Академический паб Kluwer. ISBN 978-1-4020-1021-7 .
- Григорий Т.Р. (2005). Эволюция генома . Берлингтон, Массачусетс: Elsevier Academic. ISBN 978-0-12-301463-4 .
- Левинсон Дж. (2020). Переосмысление эволюции: революция, которая скрывается на виду . Лондон: World Scientific. ISBN 978-1-78634-726-8 .
- Граур Д. , Ли В.Х. (2000). Основы молекулярной эволюции . Синауэр. ISBN 0-87893-266-6 .
- Граур Д (2016). Молекулярная и геномная эволюция . Сандерленд (Массачусетс): Sinauer Associates, Inc. ISBN 978-1605354699 .
Категория: молекулярнаяэволюция (кимура 1968)