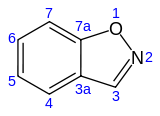
бензизоксазол
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК 1,2-бензоксазол | |||
| Другие имена Бензо[ d ]изоксазол; Индоксазин | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 2154 | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.005.440 | ||
| Номер ЕС |
| ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 7 Н 5 Н О | |||
| Молярная масса | 119.123 g·mol −1 | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 1,18 г/см 3 | ||
| Точка кипения | От 35 до 38 ° C (от 95 до 100 ° F; от 308 до 311 К) (при 2,67 гПа) 101-102 °С (при 2 кПа) | ||
| Опасности | |||
| СГС Маркировка : | |||
 | |||
| Предупреждение | |||
| Х315 , Х319 , Х335 | |||
| P261 , P264 , P271 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313, P337+P313 , , P362 P403 P403 +P233, P405, P501, P501, P501, P501 , P362, +P233 , P405 , P501 , P362, P403+P233, P3 | |||
| точка возгорания | 58 ° С (136 ° F; 331 К) | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
1,2-Бензизоксазол представляет собой ароматическое органическое соединение с молекулярной формулой C 7 H 5 NO, содержащее бензолом кольцевую структуру, конденсированную с изоксазольную . [1] [2] Само соединение не имеет общего применения; однако функционализированные бензизоксазолы и бензизоксазоилы имеют множество применений, включая фармацевтические препараты, такие как некоторые антипсихотики (включая рисперидон , палиперидон , окаперидон и илоперидон ) и противосудорожное средство зонисамид .
Его ароматичность делает его относительно стабильным; [3] однако он лишь слабо основной.
Синтез
[ редактировать ]Бензизоксазол можно получить из недорогого салицилового альдегида посредством реакции при комнатной температуре, катализируемой основанием, с гидроксиламин- O -сульфоновой кислотой . [4]
Реакции
[ редактировать ]Устранение Кемпа
[ редактировать ]Впервые сообщил Дэниел С. Кемп , [5] [6] [7] относительно слабая связь NO может быть расщеплена сильным основанием с образованием 2-гидроксибензонитрила.
См. также
[ редактировать ]- Структурные изомеры
Ссылки
[ редактировать ]- ^ Катрицкий, Арканзас; Пожарский, А.Ф. (2000). Справочник по гетероциклической химии (2-е изд.). Академическая пресса. ISBN 0080429882 .
- ^ Клейден, Дж.; Гривз, Н.; Уоррен, С.; Уотерс, П. (2001). Органическая химия . Оксфорд, Оксфордшир: Издательство Оксфордского университета. ISBN 0-19-850346-6 .
- ^ Домен, Кармен; Дженнескенс, Леонардус В.; Фаулер, Патрик В. (2005). «Ароматичность антранила и его изомеров, 1,2-бенизоксазола и бензоксазола». Буквы тетраэдра . 46 (23): 4077–4080. дои : 10.1016/j.tetlet.2005.04.014 . hdl : 1874/14837 . ISSN 0040-4039 .
- ^ Кемп, Д.С.; Вудворд, РБ (1965). «Катион N-этилбензизоксазолия — I». Тетраэдр . 21 (11): 3019–3035. дои : 10.1016/S0040-4020(01)96921-2 . ISSN 0040-4020 .
- ^ Кейси, Марта Л.; Кемп, Д.С.; Пол, Кеннет Г.; Кокс, Дэниел Д. (июнь 1973 г.). «Физическая органическая химия бензизоксазолов. I. Механизм катализируемого основаниями разложения бензизоксазолов». Журнал органической химии . 38 (13): 2294–2301. дои : 10.1021/jo00953a006 .
- ^ Кемп, Д.С.; Кокс, Дэниел Д.; Пол, Кеннет Г. (декабрь 1975 г.). «Физическая органическая химия бензизоксазолов. IV. Происхождение и каталитическая природа ускорения скорости растворителя при декарбоксилировании 3-карбоксибензизоксазолов». Журнал Американского химического общества . 97 (25): 7312–7318. дои : 10.1021/ja00858a018 .
- ^ Кемп, Дэниел С. (апрель 1970 г.). «Декарбоксилирование бензизоксазол-3-карбоновых кислот. Катализ экстракцией, имеющий возможное отношение к проблеме ферментативного механизма». Журнал Американского химического общества . 92 (8): 2553–2554. дои : 10.1021/ja00711a061 .



