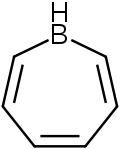
Борепин
| |
| Имена | |
|---|---|
| Название ИЮПАК
1 H -борепин
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
ПабХим CID
|
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 6 Ч 7 Б | |
| Молярная масса | 89.93 g/mol |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
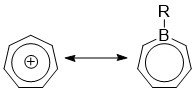
Борепины представляют собой класс борсодержащих гетероциклов, используемых в химии основной группы . Они состоят из семичленного ненасыщенного кольца с трехкоординированным бором в нем. Простые борепины являются аналогами циклогептатриена , который представляет собой семичленное кольцо, содержащее три двойные углерод-углеродные связи, каждая из которых вносит 2π-электрона, всего 6π-электронов . В отличие от других семичленных систем, таких как силепины и фосфепины , бор имеет вакантную p-орбиталь, которая может взаимодействовать с π- и π*-орбиталями циклогептатриена. [ 1 ] [ 2 ] [ 3 ] Это приводит к изоэлектронному состоянию, подобному состоянию катиона тропилия , ароматизируя борепин и одновременно позволяя ему действовать как кислота Льюиса . [ 3 ] Ароматичность борепина относительно слаба по сравнению с традиционными ароматическими соединениями , привело к синтезу многих конденсированных π-сопряженных систем борепина. такими как бензол или даже циклогептатриен, что на протяжении многих лет [ 2 ] [ 3 ] [ 4 ] [ 5 ] [ 6 ] [ 7 ] Простые и сложные борепины в последнее время широко изучаются из-за их высокой флуоресценции и потенциального применения в таких технологиях, как органические светоизлучающие диоды ( OLED ) и фотоэлектрические элементы . [ 3 ] [ 5 ] [ 7 ] [ 8 ] [ 9 ]
Синтез
[ редактировать ]Первый зарегистрированный синтетический метод
[ редактировать ]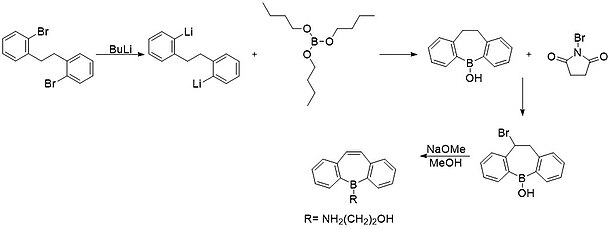
О первом синтезе стабильного борепина сообщили в 1960 году ван Тамелен , Бригер и Унтч. Синтез начался с литиирования о,о'-дибромбибензила. Затем его подвергли реакции с трибутилборатом с образованием конденсированного кольца бориновой кислоты. Этот продукт подвергали взаимодействию с н-бромсукцинимидом (NBS) с получением бромзамещенного продукта. Наконец, они провели дегидрогалогенирование , чтобы получить кольцевую систему борепин, показанную выше. [ 10 ] Подобный метод, включающий обмен олова на бор, обычно используется в современном синтезе плавленых борепиновых систем. [ 11 ]
Синтетические разработки
[ редактировать ]
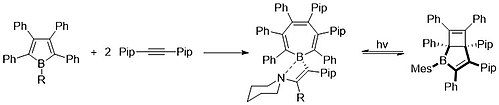
Эйш и Галле выделили первую неслитую борепин в 1975 году. Гептафенилборабициклогептадиен слева претерпел супрафациальную сигматропную перегруппировку , что привело к образованию промежуточного соединения в середине. Это промежуточное соединение впоследствии подверглось дисротаторному раскрытию кольца с образованием гептафенилборепина справа. [ 6 ] [ 12 ] Изолированный борепин кинетически стабилизируется объемистыми фенильными группами, связанными со всеми семью положениями кольца, защищая его от реакций с влагой воздуха. Однако, как и большинство бурепинов, это соединение вступало в реакцию с кислородом, меняя цвет флуоресцентно-зеленого на фиолетовый. [ 6 ] [ 13 ]

Совсем недавно Эш и Дрон разработали метод минимально замещенного бурепина. Они исходили из 1,2-дибромциклопентена и применили метод Ван дер Керка для получения борного гетероцикла. Затем они инициировали замыкание кольца с образованием 7-членного комплекса олова. Наконец, они завершили реакцию обмена олова на бор, получив бициклический борепин справа. [ 2 ] [ 14 ]
Предыдущие методы синтеза давали сильно замещенные и объемистые соединения борепина, такие как гептафенил борепин. Эти маршруты, хотя и порождали очень стабильные комплексы, затрудняли анализ свойств кольца борепин. Минимальное замещение позволило таким ученым, как Эш, подтвердить наличие ароматичности и кольцевых токов в системе борепин. [ 2 ] [ 6 ] [ 13 ] [ 14 ]
По мере появления более современных методов реакция обмена олова и бора стала более широко использоваться, поскольку олово может выступать в качестве заполнителя в семичленном кольце, довольно легко реагируя с галогенидами бора. [ 3 ]
изомеризация
[ редактировать ]В заключение отметим, что в 2018 году группа из Брауншвейга синтезировала валентный изомер борепина, показанный ниже. бициклический борсодержащий гетероцикл можно преобразовать в его изомер борепина с помощью перициклических фотохимических Этот реакций. [ 15 ]
Реактивность
[ редактировать ]Хотя прямая функционализация атома бора возможна благодаря его свободной p-орбитали, большинство простых борепин просто слишком реагируют с воздухом и влагой, чтобы их можно было изолировать. Таким образом, борепины были стабилизированы двумя общими методами: объемистыми кинетически стабилизирующими лигандами, связанными с борным центром, и дополнительными ароматическими π-системами, которые могут передавать электронную плотность пустой p-орбитали бора.
Кислотно-основные аддукты Льюиса
[ редактировать ]Борепины представляют интерес благодаря своей льюисовской кислотности. Расчеты по теории функционала плотности (DFT) показали, что ВЗМО борепина находится в основном с углеродными фрагментами семичленного кольца, а НСМО сосредоточена вокруг атома бора. [ 3 ] [ 5 ] Пример распределения HOMO/LUMO можно увидеть на рисунке ниже.

Химики, такие как Эш, смогли использовать эти знания в 1990-х годах для функционализации борепинов как соединений, что привело к образованию многих кислотно-основных аддуктов Льюиса. Наиболее распространенным предшественником борепина, используемым химиками, является комплекс борепин-галогенид, поскольку галогениды являются хорошей уходящей группой . [ 3 ] [ 13 ] Комплекс борепин-гидрид не удалось выделить из-за его нестабильности, тогда как спироцикл , легированный бором , на правой стороне соответствует октету бора, образуя цвиттер-ион между бором и азотом.
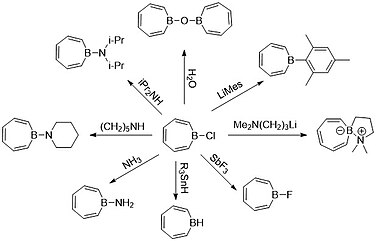
Катионы, анионы и радикалы борепина
[ редактировать ]Используя концепцию цвиттер-ионов, Gilliard et al. недавно смог синтезировать и охарактеризовать катионное состояние борепина, используя N-гетероциклические карбены (NHC) и циклические (алкил) (амино) карбены (CAACS). Из-за дативной передачи NHC и CAAC бор имеет только две ковалентные связи, что придает ему формальный положительный заряд. [ 8 ]
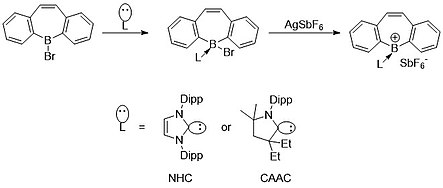
Совсем недавно, в 2022 году, Gilliard et al. смогли применить аналогичные принципы к своим катионным борепинам, чтобы сформировать и охарактеризовать первый экземпляр изолированных борепиновых радикалов . Эти радикалы также были способны восстанавливаться до первого экземпляра борепинового аниона , в котором между бор-углеродным центром имеется множественная связь. [ 16 ] Генерация радикала происходит из-за сильной π-принимающей способности карбенового углерода. Электронная плотность, общая с центром бора, слегка связывается с атомом углерода, что приводит к образованию одноэлектронных радикалов.

Манипулирование фреймворком
[ редактировать ]Спектроскопические данные, расчеты методом DFT и термохимические данные показали, что борепин слабо ароматичен по сравнению с катионом тропилия. Это снижение ароматичности приводит к повышенной реакционной способности и нестабильности в центре бора, поскольку на p-орбиталь бора передается меньшая электронная плотность. [ 1 ] [ 2 ] [ 17 ] [ 18 ]
В результате химики искали способы усилить ароматический характер борепинов. Проверенный метод, с помощью которого химики стабилизируют борепины, — это слияние фенил-борепинового кольца ( аннуляция ). Добавление двух конденсированных фенильных колец увеличивает систему борепин 6π до конденсированной системы 14π.
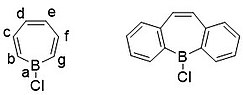
Сложностью, возникающей при слиянии фенильных колец, является их расположение. При синтезе дибензо[b,f]борепинов (b — углерод рядом с атомом бора) они идеально выравниваются для сопряжения бороциклогептатриенового кольца. Однако если фенилы расположены по схеме [c,e] (см. ниже), то полученное соединение менее стабильно, чем дибензо[b,f]борепины, примерно на 34 ккал/моль, что является довольно большой разницей в энергии. [ 17 ]

Эти результаты, объясненные Шульманом и Дишем, неоднократно применялись для модификации каркасов буровых штифтов. Некоторые распространенные примеры включают увеличение количества колец - получение полициклических ароматических углеводородов (ПАУ), легированных бором, добавление дополнительных групп R к каркасу, таких как алкины и длинноцепочечные алканы, и даже введение богатых электронами гетероатомов, таких как азот или сера. для дальнейшей стабилизации буревин. [ 4 ] [ 9 ] [ 11 ] [ 19 ] [ 20 ] Некоторые примеры этих соединений можно увидеть на изображении ниже:

Быстрое развитие стабилизации и функционализации борепинов с 2000-х годов стимулировало исследования сложных и универсальных молекул. Как и многие другие соединения основной группы, борепины используются в полевых условиях с середины-конца 1900-х годов, но бездействуют до тех пор, пока их не смогут использовать более современные методы.
Фотофизические свойства
[ редактировать ]Флуоресценция/фосфоресценция
[ редактировать ]Первые сообщения о флуоресценции борепина были опубликованы в 1975 году Эйшем и Галле и описывали, как гептафенилборепин при исследовании флуоресцировал зеленым светом. [ 6 ] Незначительные фотофизические явления регистрировались в течение многих лет, пока группа Пирса не опубликовала первый пример сине-флуоресцентного вида борепин в 2009 году. [ 5 ] Они обнаружили, что, расширяя π-систему (т.е. добавляя больше конденсированных фенильных колец), они могут резко изменить длину волны своих соединений примерно с 250 нанометров (нм) до более чем 450 нм. Обоснование этого сдвига заключается в том, что присутствие бора в ароматической системе уменьшает энергетическую щель между ВЗМО и НСМО, что приводит к изменению поглощения и большей интенсивности флуоресценции. [ 5 ] Об аналогичных результатах сообщили Карузо, Товар и Зиглер в 2010 году, когда они подвергали борепин электрохимическим окислительно-восстановительным реакциям , а также Мессерсмит, Зиглер и Товар в 2016 году при тестировании эффектов переменной ароматичности борепинов. [ 21 ] [ 22 ]
Первоначальное волнение, стоящее за этими результатами, заключалось в возможности их использования в электронных материалах, таких как органические светоизлучающие диоды ( OLED ). Если бы «переключателем» флуоресценции можно было управлять, а также иметь стабильные борепиновые комплексы, то было бы относительно легко и дешево получить яркий флуоресцентный свет, потенциально любого цвета. [ 20 ]
Другой потенциал окислительно-восстановительной химии — использование борсодержащих полициклических ароматических углеводородов в качестве полупроводников . Из-за низкой LUMO борепинов он может действовать как акцептор электронов, участвуя в транспорте электронов. Группа Вагнера, а также Тоскано и его коллеги вычислительно и экспериментально продемонстрировали потенциальное применение этих комплексов. [ 4 ] [ 23 ]
С другой стороны, ученые стремились использовать борепины в качестве потенциальных датчиков анионов. В прошлом трехкоординированные бораны использовались для обнаружения анионов, таких как фторид , цианид и даже аммиак . [ 21 ] [ 24 ] [ 25 ] Такие ученые, как Адачи и Ошита, продемонстрировали, что при координации фторида ( F − ) флуоресценция увеличивается во много раз. [ 24 ]
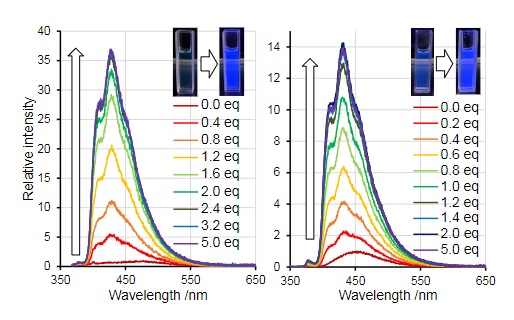
В отличие от этого примера, при добавлении цианида к одному из их борепиновых аналогов тетратиеноантрацента Адачи и Ошита наблюдали потерю флуоресценции. наблюдалась заметная фосфоресценция . Однако при охлаждении в растворе [ 25 ]
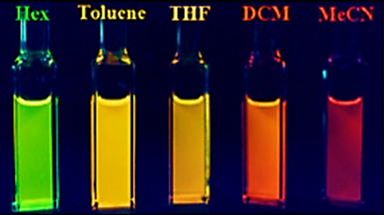
Флуоресценция не ограничивается только внешней координацией. При введении азота в борепиновое кольцо Li et al. смогли наблюдать сольватохромные эффекты. При добавлении борепина к гексанам , толуолу , тетрагидрофурану (ТГФ), дихлорметану (DCM) и ацетонитрилу (MeCN) наблюдались довольно резкие изменения цвета. [ 9 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б Шульман, Джером М.; Диш, Раймонд Л. (март 1989 г.). «Термохимия борабензола и борепина». Металлоорганические соединения . 8 (3): 733–737. дои : 10.1021/om00105a024 .
- ^ Jump up to: а б с д и Эш, Эй Джей; Дрон, Ф.Дж.; Кауш, СМ; Крокер, Дж.; Аль-Тавил, С.М. (1 января 1990 г.). «Борепины и гетеролы 15-элементной группы» . Чистая и прикладная химия . 62 (3): 513–517. дои : 10.1351/pac199062030513 . S2CID 96223530 .
- ^ Jump up to: а б с д и ж г Ван, Лили; Ма, Хуан; Си, Эрбинг; Дуань, Чжэн (февраль 2021 г.). «Последние достижения в области люминесцентных кольчатых борепинов, силепинов и фосфепинов». Синтез . 53 (4): 623–635. дои : 10.1055/s-0040-1705946 . S2CID 228982156 .
- ^ Jump up to: а б с Шикеданц, Кай; Радтке, Джулиан; Болт, Майкл; Лернер, Ганс-Вольфрам; Вагнер, Матиас (22 февраля 2017 г.). «Простой путь к четырехкратно кольчатым борепинам» . Журнал Американского химического общества . 139 (7): 2842–2851. дои : 10.1021/jacs.7b00268 . ПМИД 28125773 .
- ^ Jump up to: а б с д и ж Мерсье, Лорен Г.; Пирс, Уоррен Э.; Парвез, Масуд (29 июля 2009 г.). «Бензо- и нафтоборепины: борные аналоги высших аценов, излучающие синее излучение» . Angewandte Chemie, международное издание . 48 (33): 6108–6111. дои : 10.1002/anie.200902803 . ПМИД 19598197 .
- ^ Jump up to: а б с д и Эйш, Джон Дж.; Галле, Джеймс Э. (июль 1975 г.). «Перегруппировки металлоорганических соединений. XIII. Бораароматические системы. IV. Синтез гептафенилборепина термической перегруппировкой гептафенил-7-борабицикло[2.2.1]гептадиена». Журнал Американского химического общества . 97 (15): 4436–4437. дои : 10.1021/ja00848a070 .
- ^ Jump up to: а б Адачи, Ёхей; Осита, Джоджи (26 марта 2018 г.). «Синтез и свойства бензо[d]дитиено[b, f]борепинов». Металлоорганические соединения . 37 (6): 869–881. doi : 10.1021/acs.organomet.7b00844 .
- ^ Jump up to: а б Ян, Вэньлун; Кранц, Келси Э.; Фриман, Лукас А.; Дикки, Дайан А.; Молино, Эндрю; Каур, Айшварьядип; Уилсон, Дэвид Джей Ди; Жильяр, Роберт Дж. (25 сентября 2019 г.). «Стабильные гетероциклы борепиния и борафторения: обратимый термохромный «переключатель», основанный на взаимодействиях бора и кислорода». Химия – Европейский журнал . 25 (54): 12512–12516. дои : 10.1002/chem.201903348 . ПМИД 31334883 . S2CID 198170504 .
- ^ Jump up to: а б с д Ли, Чэнлун; Ши, Яфэй; Ли, Пэнфэй; Чжан, Ню; Ван, Нан; Инь, Сяодун; Чен, Панкуань (17 сентября 2021 г.). «Доступ к высоколюминесцентным диазаборепинам, легированным N, с пента-, гекса- и семиугольными субструктурами». Органические письма . 23 (18): 7123–7128. doi : 10.1021/acs.orglett.1c02528 . ПМИД 34449226 . S2CID 237339643 .
- ^ ван Тамелен, Э.Э.; Бригер, Г.; Унч, КГ (14 марта 1960 г.). «Синтез борепинки». Буквы тетраэдра . 1 (29): 14–15. дои : 10.1016/S0040-4039(01)82703-9 .
- ^ Jump up to: а б Карузо, Энтони; Товар, Джон Д. (17 июня 2011 г.). «Сопряженные «B-энтацены»: полициклические ароматические соединения, содержащие два борепиновых кольца». Органические письма . 13 (12): 3106–3109. дои : 10.1021/ol2010159 . ПМИД 21604774 .
- ^ Эйш, Джон Дж.; Галле, Джеймс Э.; Шафии, Бабак; Рейнгольд, Арнольд Л. (август 1990 г.). «Бора-ароматические системы. 12. Термическая генерация и трансформация борепиновой кольцевой системы: парадигма перициклических процессов». Металлоорганические соединения . 9 (8): 2342–2349. дои : 10.1021/om00158a035 .
- ^ Jump up to: а б с Эш, Артур Дж.; Кляйн, Вольфрам; Руссо, Роджер (август 1993 г.). «Оценка ароматичности борепина: синтез и свойства 1-замещенных борепинов». Металлоорганические соединения . 12 (8): 3225–3231. дои : 10.1021/om00032a051 .
- ^ Jump up to: а б Эш, Артур Дж.; Дрон, Фредерик Дж. (март 1987 г.). «1-Метил-4,5-циклопентеноборепин: нейтральный борный аналог тропилия». Журнал Американского химического общества . 109 (6): 1879–1880. дои : 10.1021/ja00240a058 .
- ^ Чаша, Хауке; Плитка, Стефани; Уолер, Джон; Челик, Мехмет Али; Стой, Андреас; Крумменахер, Иво; Крамер, Томас; Радацкий, Кшиштоф; Брауншвейг, Хольгер (12 октября 2018 г.). «Борабицикло[3.2.0]гептадиен: конденсированный бициклический изомер борепина». Химия - Европейский журнал . 24 (57): 15387–15391. дои : 10.1002/chem.201803509 . ПМИД 30095190 . S2CID 51953498 .
- ^ Холлистер, Кимберли К.; Ян, Вэньлун; Мондол, Ранаджит; Венц, Келси Э.; Молино, Эндрю; Каур, Айшварьядип; Дикки, Дайан А.; Фрекинг, Гернот; Пан, Судип; Уилсон, Дэвид Джей Ди; Жильяр, Роберт Дж. (7 июня 2022 г.). «Выделение стабильных борепиновых радикалов и анионов» . Angewandte Chemie, международное издание . 61 (23): e202202516. дои : 10.1002/anie.202202516 . ПМЦ 9324096 . ПМИД 35289046 .
- ^ Jump up to: а б Шульман, Джером М.; Диш, Раймонд Л. (1 июля 2000 г.). «Борепин и его аналоги: плоские и неплоские соединения». Металлоорганические соединения . 19 (15): 2932–2936. дои : 10.1021/om0002733 .
- ^ Субраманиан, Говиндан; Шлейер, Поль фон Раге; Цзяо, Хайцзюнь (1 мая 1997 г.). «Ароматичность аннелированных бурепин». Металлоорганические соединения . 16 (11): 2362–2369. дои : 10.1021/om970008q .
- ^ Левин, Дэвид Р.; Зиглер, Максим А.; Товар, Джон Д. (14 мая 2014 г.). «Сплавленные с тиофеном борепины как непосредственно функционализируемые борсодержащие π-электронные системы». Журнал Американского химического общества . 136 (19): 7132–7139. дои : 10.1021/ja502644e . ПМИД 24738628 .
- ^ Jump up to: а б Карузо, Энтони; Товар, Джон Д. (25 февраля 2011 г.). «Функционализированные дибензоборепины как компоненты малых молекул и полимерных π-сопряженных электронных материалов». Журнал органической химии . 76 (7): 2227–2239. дои : 10.1021/jo2001726 . ПМИД 21351778 .
- ^ Jump up to: а б Карузо, Энтони; Зиглер, Максим А.; Товар, Джон Д. (7 мая 2010 г.). «Синтез функционализируемых борсодержащих π-электронных материалов, включающих формально ароматические конденсированные борепиновые кольца». Angewandte Chemie, международное издание . 49 (25): 4213–4217. дои : 10.1002/anie.201000411 . ПМИД 20455227 .
- ^ Мессерсмит, Рид Э.; Зиглер, Максим А.; Товар, Джон Д. (1 июля 2016 г.). «Конкуренция ароматичности в дифференциально конденсированных борепинсодержащих полициклических ароматических соединениях». Журнал органической химии . 81 (13): 5595–5605. дои : 10.1021/acs.joc.6b00927 . ПМИД 27224845 .
- ^ Де Симона, Бруна Клара; Маццоне, Глория; Марино, Тициана; Руссо, Нино; Тоскано, Марироса (31 августа 2018 г.). «Об электрохромных свойствах борепинов: вычислительное предсказание» . АСУ Омега . 3 (8): 9556–9563. дои : 10.1021/acsomega.8b01288 . ПМК 6645310 . ПМИД 31459087 .
- ^ Jump up to: а б с Адачи, Ёхей; Ямада, Кохей; Осита, Джоджи (5 июня 2022 г.). «Синтез и оптические свойства антрилзамещенных тетрациклических борепинов». Химические письма . 51 (6): 654–657. дои : 10.1246/кл.220139 . S2CID 248313365 .
- ^ Jump up to: а б Адачи, Ёхей; Арай, Фука; Ямада, Кохей; Курихара, Махо; Осита, Джоджи (23 мая 2022 г.). «Оптические свойства борсодержащих аналогов тетратиеноантрацена». Металлоорганические соединения . 41 (10): 1225–1231. doi : 10.1021/acs.organomet.2c00106 . S2CID 248735151 .