Тропон
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Циклогепта-2,4,6-триен-1-он | |||
| Другие имена
Циклогепта-2,4,6-триенон
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.007.933 | ||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 7 Н 6 О | |||
| Молярная масса | 106.12 g/mol | ||
| Плотность | 1,094 г/мл | ||
| Точка кипения | 113 ° C (235 ° F; 386 К) (15 мм рт. ст.) | ||
| Опасности | |||
| точка возгорания | > 113 ° C (235 ° F; 386 К) | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Тропон или 2,4,6-циклогептатриен-1-он представляет собой органическое соединение , имеющее определенное значение в органической химии как небензеноидное ароматическое вещество . [ 2 ] Соединение состоит из кольца из семи атомов углерода с тремя сопряженными алкеновыми группами и кетоновой группой. Родственное соединение трополон (2-гидрокси-2,4,6-циклогептатриен-1-он) имеет дополнительную спиртовую (или енольную, включающую двойную связь) группу рядом с кетоном. Тропоны редко встречаются в натуральных продуктах, за исключением 2-гидроксильных производных, которые называются трополонами .
Тропон известен с 1951 года и его еще называют оксидом циклогептатриенилия . Название трополон было придумано М.Дж.С. Дьюаром в 1945 году в связи с предполагаемыми ароматическими свойствами. [ 3 ]
Характеристики
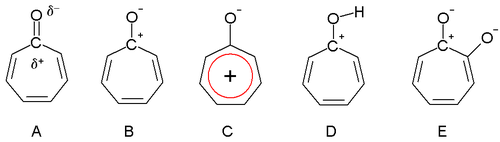
[ редактировать ]Дьюар в 1945 году предположил, что тропоны могут обладать ароматическими свойствами. Карбонильная . группа более поляризована за счет триенового кольца, что дает частичный положительный заряд атому углерода (А) и частичный отрицательный заряд кислороду В крайнем случае атом углерода имеет полный положительный заряд (B), образуя кольцо иона тропилия , которое представляет собой ароматическую 6-электронную систему (C).
Тропоны также являются основными (D) в результате ароматической стабилизации. Это свойство можно наблюдать по легкости образования солей с кислотами. Дипольный момент тропона составляет 4,17 Д по сравнению со значением всего лишь 3,04 Д для циклогептанона . Это различие согласуется со стабилизацией структуры диполярного резонанса.
Синтез
[ редактировать ]Существует множество методов органического синтеза тропонов и их производных. Два выбранных метода синтеза тропона - это диоксидом селена окисление циклогептатриена . [ 4 ] и косвенно из тропинона путем элиминирования Гофмана и бромирования . [ 2 ]
Реакции
[ редактировать ]Тропон подвергается сжатию кольца до бензойной кислоты с гидроксидом калия при повышенной температуре. Многие производные также сжимаются до соответствующих аренов . [ 2 ] Тропон реагирует при электрофильном замещении , например, с бромом , но реакция протекает через продукт 1,2-присоединения и не является электрофильным ароматическим замещением . [ 2 ]
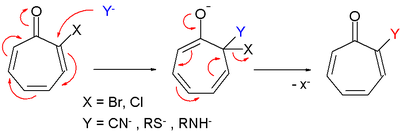
Производные тропона также реагируют на нуклеофильное замещение, очень похожее на нуклеофильное ароматическое замещение . [ 2 ]
Также обнаружено, что тропон реагирует в форме [8+3] -кольца с коричным альдегидом . [ 5 ]
Diene персонаж
[ редактировать ]Тропон ведет себя как диен в реакциях Дильса-Альдера , например, с малеиновым ангидридом . [ 2 ] Точно так же он образует аддукты с трикарбонилом железа, подобные (бутадиен)трикарбонилу железа . [ 6 ]
Производные
[ редактировать ]| Имя | Химическая структура | Природные источники |
|---|---|---|
| Трополон |  |
Pseudomonas lindbergii , Pseudomonas plantarii [ 7 ] |
| хинокитиол |  |
кипарисовых Деревья [ 8 ] |
| Стипитатовая кислота |  |
Таларомицес стипитатус [ 9 ] |
| Троподитиетиновая кислота |  |
Phaeobacter piscinae , Phaeobacterhibitus , Phaeobacter Gallaeciensis [ 10 ] [ 11 ] |
| Колхицин |  |
Безвременник осенний , Славный гордый [ 12 ] |
Другие производные тропона включают пуберулоновую и пуберуловую кислоты, розеобактициды, пернамбукон, крототропон, оробанон. [ 13 ] [ 14 ] [ 15 ] [ 16 ] [ 17 ]
Ссылки
[ редактировать ]- ^ Тропон в Sigma-Aldrich
- ^ Перейти обратно: а б с д и ж Паусон, Питер Л. (1955). «Тропоны и трополоны». хим. Откр. 55 (1): 9–136. дои : 10.1021/cr50001a002 .
- ^ MJS Дьюар (1945). «Структура стипитатовой кислоты». Природа . 155 (3924): 50–51. Бибкод : 1945Natur.155...50D . дои : 10.1038/155050b0 . S2CID 4086209 .
- ^ Данке, Карл Р.; Пакетт, Лео А. (1993). «Обратное электронно-запросное циклоприсоединение дитиоацеталя Дильса-Альдера. Восстановление сопряженного енона, стимулируемое гидридом меди. 9-дитиоланобицикло[3.2.2]нон-6-ен-2-он» . Орг. Синтез. 71 : 181 дои : 10.15227/orgsyn.071.0181 .
- ^ N-гетероциклическое карбен-катализируемое [8 + 3] аннелирование тропона и эналов через гомоенолят Виджай Наир, Маноджкумар Пунот, Шрикумар Веллалат, Эрингатоди Суреш и Раджасекаран Тирумалай J. Org. хим. ; 2006 год ; 71(23) стр. 8964-8965; (Примечание) два : 10.1021/jo0615706
- ^ Додж, Р.П. (1964). «Кристаллическая и молекулярная структура трикарбонила тропонового железа». Журнал Американского химического общества . 86 (24): 5429–5431. дои : 10.1021/ja01078a013 .
- ^ Лю, На; Сонг, Вангзе; Шинебек, Каси М.; Чжан, Мин; Тан, Вэйпин (декабрь 2014 г.). «Синтез природных тропонов и трополонов» . Тетраэдр . 70 (49): 9281–9305. дои : 10.1016/j.tet.2014.07.065 . ПМЦ 4228802 . ПМИД 25400298 .
- ^ Саньевски, Мариан; Хорбович, Марцин; Канлаянарат, Сиричай (10 сентября 2014 г.). «Обзор биологической активности тропоноидов и их использования в сельском хозяйстве» . Журнал садоводческих исследований . 22 (1): 5–19. дои : 10.2478/johr-2014-0001 .
- ^ Дэвисон, Дж.; аль Фахад, А.; Кай, М.; Песня, З.; Йехия, С.Ю.; Лазарь, CM; Бейли, AM; Симпсон, Ти Джей; Кокс, Р.Дж. (15 мая 2012 г.). «Генетические, молекулярные и биохимические основы биосинтеза трополона грибов» . Труды Национальной академии наук . 109 (20): 7642–7647. дои : 10.1073/pnas.1201469109 . ПМЦ 3356636 . ПМИД 22508998 .
- ^ Рабе, Патрик; Клапщинский, Тим А; Брок, Нельсон Л; Цитрон, Кристиан А; Д'Альвиз, Пол; Бабушка, Одинокий; Дикшат, Йерун С. (6 августа 2014 г.). «Синтез и биологическая активность аналогов морского антибиотика троподитиетиновой кислоты» . Журнал органической химии Байльштейна . 10 : 1796–1801. дои : 10.3762/bjoc.10.188 . ПМЦ 4142847 . ПМИД 25161739 .
- ^ Байерсманн, Пол Г.; Томаш, Юрген; Сын, Кванмин; Стокер, Роман; Гёкер, Маркус; Вагнер-Дёблер, Ирен; Саймон, Мейнхард; Бринкхофф, Торстен (декабрь 2017 г.). «Двойная функция троподитиетиновой кислоты как антибиотика и сигнальной молекулы в глобальной регуляции генов пробиотической бактерии Phaeobacter inhibens» . Научные отчеты . 7 (1): 730. Бибкод : 2017НатСР...7..730Б . дои : 10.1038/s41598-017-00784-7 . ПМЦ 5429656 . ПМИД 28389641 .
- ^ Кейт, Майкл П.; Гиллиланд, Уильям Р.; Уль, Кэтлин (2009). «Подагра». Фармакология и терапия : 1039–1046. дои : 10.1016/B978-1-4160-3291-5.50079-2 . ISBN 978-1-4160-3291-5 .
- ^ Тиль, Верена; Бринкхофф, Торстен; Дикшат, Йерун С.; Викель, Сюзанна; Груненберг, Йорг; Вагнер-Дёблер, Ирен; Саймон, Мейнхард; Шульц, Стефан (10 декабря 2009 г.). «Идентификация и биосинтез производных тропона и летучих веществ серы, продуцируемых бактериями морской клады Roseobacter». Органическая и биомолекулярная химия . 8 (1): 234–246. дои : 10.1039/B909133E . ПМИД 20024154 .
- ^ Дуань, Ин; Петцольд, Мелани; Салим-Батча, Распудин; Тойфель, Робин (сентябрь 2020 г.). «Натуральные продукты и производные бактериальных тропонов: обзор их биосинтеза, биоактивности, экологической роли и биотехнологического потенциала» . ХимБиоХим . 21 (17): 2384–2407. дои : 10.1002/cbic.201900786 . ПМЦ 7497051 . ПМИД 32239689 .
- ^ Рандау, КП; Сролл, С.; Лерш, Х.; Брейчер, Ф. (1 мая 2009 г.). «Пернамбукон, новое производное тропона из Croton argyroglossum». Die Pharmazie . 64 (5): 350–351. дои : 10.1691/ph.2009.7592 . ПМИД 19530449 .
- ^ Брахер, Франц; Рандау Карина П.; Лерче, Хольгер (1 апреля 2008 г.). «Крототропон, новый тропон, полученный из Croton zehntneri». Фитотерапия . 79 (3): 236–237. дои : 10.1016/j.fitote.2007.12.001 . ПМИД 18321658 .
- ^ Фрюшье, Ален; Расколь, Жан-Пьер; Андари, Клод; Приватт, Гай (1 января 1981 г.). «Производное тропона из orobanche rapum-genistae». Фитохимия . 20 (4): 777–779. Бибкод : 1981PChem..20..777F . дои : 10.1016/0031-9422(81)85173-4 .