Диффузная срединная глиома
Эта статья нуждается в более надежных медицинских ссылках для проверки или слишком сильно полагается на первоисточники . ( май 2017 г. ) |  |
| Диффузная срединная глиома | |
|---|---|
 | |
| Магнитно-резонансная томография диффузной внутренней глиомы моста. | |
| Обычное начало | 5–10 лет [ 1 ] |
| Уход | Радиация Химиотерапия (Операция по биопсии или удалению опухоли небезопасна из-за ее местоположения) [ 1 ] |
| Прогноз | Средняя общая выживаемость обычно колеблется от 8 до 11 месяцев. [ 2 ] |
| Частота | ~ 10–20% опухолей головного мозга у детей [ 1 ] |
Диффузная срединная глиома, измененная H3 K27 ( DMG ), представляет собой смертельную опухоль , которая возникает в срединных структурах головного мозга, чаще всего в стволе мозга , таламусе и спинном мозге . При расположении в мосту она также известна как диффузная внутренняя глиома моста ( ДИПГ ). [ 3 ]
Считается, что DMG вызван генетическими мутациями, которые вызывают эпигенетические изменения в клетках развивающейся нервной системы, что приводит к неспособности клеток правильно дифференцироваться. [ 4 ] [ 5 ] В настоящее время стандартом лечения является фракционированная дистанционная лучевая терапия, поскольку расположение опухоли исключает хирургическое вмешательство, а химиотерапия оказалась неэффективной. [ 6 ] [ 7 ] Однако расчетная выживаемость после постановки диагноза остается всего 9–15 месяцев. ДМГ в первую очередь поражают детей: средний возраст постановки диагноза составляет около 6-7 лет. [ 8 ]
Современные знания показали, что в патологии глиомы участвуют несколько генов. Патология устойчива к лечению, что позволяет предположить, что основной причиной является отключение механизмов клеточного апоптоза. [ 9 ]
Диагностика
[ редактировать ]

Как и большинство опухолей ствола мозга, диагностика диффузной внутренней глиомы моста обычно включает неинвазивную визуализацию головного мозга, такую как МРТ, в дополнение к неврологическому физическому осмотру. Биопсия и другие процедуры проводятся очень редко. Подобно ДИПГ, диффузные срединные глиомы (ДМГ) часто попадают в те же категории как по диагностике, так и по лечению, что и ДИПГ, и часто классифицируются вместе. [ 10 ] В последнее время биопсию проводят, чтобы можно было выбрать лучший вариант клинических испытаний. [ 11 ]
В исследованиях, полученных на основе реестра DIPG/DMG и в связи с коллаборацией DIPG/DMG, статистика показывает, что примерно у 150–300 пациентов в США диагностируется DIPG в год, средний возраст пациентов с DIPG составляет примерно 6–7 лет. старше, а соотношение мужчин и женщин среди пациентов с ДИПГ составляет 1:1. [ 8 ]
Уход
[ редактировать ]Стандартное лечение ДИПГ составляет 6 недель лучевой терапии , которая часто значительно улучшает симптомы. Однако симптомы обычно рецидивируют через 6–9 месяцев и быстро прогрессируют. [ 12 ]
Нейрохирургия
[ редактировать ]При ДИПГ хирургическое вмешательство по удалению опухоли обычно невозможно или нецелесообразно. По своей природе эти опухоли диффузно проникают по всему стволу мозга, разрастаясь между нормальными нервными клетками. Агрессивная операция может привести к серьезному повреждению нервных структур, жизненно важных для движений рук и ног, движения глаз, глотания, дыхания и даже сознания.
Нейрохирургически выполненная биопсия ствола головного мозга для иммунотипирования диффузной внутренней глиомы моста в последнее время сыграла ограниченную роль в экспериментальных клинических исследованиях и испытаниях лечения. Однако это не является текущим стандартом медицинской помощи, поскольку представляет значительный риск, учитывая местоположение биопсии, и поэтому надлежащим образом выполняется только в контексте участия в продолжающемся клиническом исследовании лечения.
Биопсия моста никоим образом не является терапевтической или лечебной операцией, и риски (потенциально катастрофические и фатальные) перевешиваются только тогда, когда диагноз неопределенен (чрезвычайно необычен) или когда пациент участвует в одобренном клиническом исследовании.
Лучевая терапия
[ редактировать ]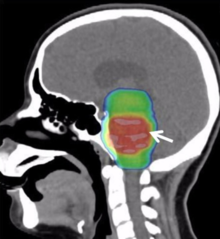
Традиционная лучевая терапия, ограниченная пораженной областью опухоли, является основой лечения ДИПГ. Стандартной является общая доза облучения от 5400 до 6000 сГр , вводимая ежедневными фракциями от 150 до 200 сГр в течение 6 недель. Гиперфракционированная (дважды в день) лучевая терапия использовалась ранее для получения более высоких доз радиации, но не приводила к улучшению выживаемости. Радиохирургия (например, гамма-нож или кибернож) играет определенную роль в лечении ДИПГ и может рассматриваться в отдельных случаях.
Химиотерапия и другие медикаментозные методы лечения
[ редактировать ]Роль химиотерапии при ДИПГ остается неясной. Исследования показали незначительное улучшение выживаемости, хотя в рамках Детской онкологической группы (COG), Консорциума педиатрических опухолей головного мозга (PBTC) и других предпринимаются усилия (см. ниже) по дальнейшему изучению использования химиотерапии и других препаратов. Лекарства, усиливающие эффект лучевой терапии ( радиосенсибилизаторы ), не показали дополнительной пользы, но новые многообещающие препараты находятся в стадии изучения. Иммунотерапия бета -интерфероном и ингибиторами иммунных контрольных точек также не имела большого эффекта в исследованиях. Было показано, что неоэпитоп-специфичные пептидные вакцины, нацеленные на клональную драйверную мутацию H3 K27M, вызывают ответы цитотоксических Т-клеток и Т-хелперов у пациентов с диффузной глиомой средней линии. [ 13 ] [ 14 ] Интенсивная или высокодозная химиотерапия с аутологичной трансплантацией костного мозга или спасением стволовых клеток периферической крови не продемонстрировала никакой эффективности при глиомах ствола головного мозга. Будущие клинические испытания могут включать лекарства, предназначенные для вмешательства в клеточные пути (ингибиторы передачи сигнала), или другие подходы, которые изменяют опухоль или ее окружение. [ 15 ] [ 16 ] [ 17 ]
Прогноз
[ редактировать ]
ДИПГ является неизлечимым заболеванием , поскольку 5-летняя выживаемость при нем составляет <1%. Медиана общей выживаемости детей с диагнозом ДИПГ составляет примерно 9 месяцев. Выживаемость через 1 и 2 года составляет примерно 30% и менее 10% соответственно. Эти статистические данные делают DIPG одним из самых разрушительных видов рака у детей . [ 18 ] Хотя у 75–85% пациентов наблюдается некоторое улучшение симптомов после лучевой терапии , ДИПГ почти всегда начинают снова расти (это называется рецидивом, рецидивом или прогрессированием). Клинические исследования показали, что среднее время между лучевой терапией и прогрессированием составляет 5–8,8 месяцев. [ 19 ] Пациенты, у которых опухоли снова начинают расти, могут иметь право на экспериментальное лечение посредством клинических испытаний, чтобы попытаться замедлить или остановить рост опухоли. Однако клинические испытания пока не показали какой-либо существенной пользы от экспериментальной терапии DIPG. [ 19 ]
Прогрессирующие ДИПГ обычно быстро растут и поражают важные части мозга. Среднее время от прогрессирования опухоли до смерти обычно очень короткое – от 1 до 4,5 месяцев. В это время врачи сосредотачиваются на паллиативной помощи : контроле симптомов и обеспечении максимального комфорта пациента. [ 19 ]
Исследовать
[ редактировать ]
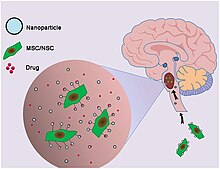
Как и в случае с большинством опухолей головного мозга, основной трудностью в лечении ДИПГ является преодоление гематоэнцефалического барьера . [ 20 ] [ 21 ]
В мозге – в отличие от других частей тела, где вещества могут свободно проходить из крови в ткани – между клетками, выстилающими кровеносные сосуды, очень мало места. Таким образом, движение веществ в мозг существенно ограничивается. Этот барьер образован клетками, выстилающими сосуды, а также отростками близлежащих астроцитов . Эти два типа клеток связаны белками, образуя так называемые «плотные соединения». Вся структура называется гематоэнцефалический барьер (ГЭБ). Он предотвращает попадание химических веществ, токсинов, бактерий и других веществ в мозг и, таким образом, выполняет постоянную защитную функцию. Однако при таких заболеваниях, как опухоли головного мозга, ГЭБ также может препятствовать достижению цели диагностическими и терапевтическими средствами.
Исследователи и врачи опробовали несколько методов преодоления гематоэнцефалического барьера:
- Интратекальное/интравентрикулярное введение : химиопрепараты вводятся непосредственно в спинномозговую жидкость либо через люмбальную пункцию , либо через хирургически имплантированный катетер .
- Внутримозговые имплантаты : нейрохирург создает полость внутри опухоли, чтобы можно было разместить химиотерапевтические пластины размером с десятицентовую монету, такие как пластины глиадели. Несколько таких пластинок можно установить во время операции, и они высвобождать химиотерапевтический агент кармустин со временем будут медленно . Это обеспечивает гораздо более высокую концентрацию химиопрепаратов в мозге, чем при внутривенном введении, и вызывает меньше системных побочных эффектов . Однако это вариант только для пациентов с хирургически операбельными опухолями; его нельзя использовать для лечения ДИПГ. [ 22 ]
- Осмотическое нарушение гематоэнцефалического барьера (BBBD): клетки гематоэнцефалического барьера уменьшаются под действием концентрированного раствора сахара ( маннита ). Это открывает барьер и позволяет в 10–100 раз большему количеству химиопрепаратов проникнуть в мозг. Катетер вводится в крупную артерию (обычно ту, что в паху, называемую бедренной артерией ) и подводится к сонной или позвоночной артерии . Вводится гипертонический маннитол, а затем химиотерапевтический агент. Пациенты проводят несколько дней в больнице для каждого введения. Это было предпринято с опухолями DIPG. [ 23 ]
- Доставка с усиленной конвекцией: химиотерапия доставляется к опухоли с помощью хирургически имплантированного катетера под градиентом давления для достижения большего распределения, чем при одной лишь диффузии. Ограниченные эксперименты были проведены с опухолями головного мозга, в том числе с DIPG. [ 24 ]
- Носители лекарств. Такие носители, как молекулы «троянского коня», липосомы и наночастицы , теоретически могут позволить терапевтическому лекарству проникнуть в мозг. Такая тактика в основном находится на стадии исследования и еще не имеет клинического значения для лечения опухолей головного мозга. [ 21 ]
Патология
[ редактировать ]Окончательным генетическим маркером диффузной глиомы средней линии является потеря H3K27me3 . Диффузные срединные глиомы имеют три известных подтипа: [ 25 ]
- H3K27M: Называется диффузной глиомой средней линии, мутант H3K27 .
- Сверхэкспрессия EZHIP : называется H3K27 EZHIP-DMG дикого типа . [ 26 ]
- Мутант EGFR : называется диффузной глиомой средней линии, EGFR-измененным .
Выдающиеся пациенты
[ редактировать ]- Карен Армстронг (1959–1962), дочь американского астронавта Нила Армстронга и его первой жены Джанет Элизабет Широн. [ 27 ]
- Елена Дессерих (2000–2007), дочь Брук и Кита Дессерих. После ее кончины ее родители основали фонд The Cure Starts Now Foundation. [ 28 ] первая международная благотворительная организация DIPG/DMG, которая сегодня профинансировала более 12 миллионов долларов на исследования в 114 больницах. Ее история также была описана в «Записках, оставленных позади» и стала бестселлером New York Times 12 ноября 2009 года. [ 29 ]
- Габриэлла Миллер (2003–2013), американская защитница борьбы с детским раком, которая собрала тысячи долларов для благотворительных организаций по борьбе с детским раком и основала Smashing Walnuts Foundation. [ 30 ] [ 31 ] Закон о первых исследованиях детей Габриэллы Миллер , подписанный в законе США в 2014 году, был назван в ее честь.
- Лорен Хилл (1995–2015), американская баскетболистка-первокурсница Университета Маунт-Сент-Джозеф , Цинциннати. Чтобы исполнить ее желание сыграть в баскетбол за команду колледжа в одной игре, женский баскетбольный матч Хирам против Маунт-Сент-Джозефа 2014 года был запланирован на 13 дней раньше первоначально запланированной даты и содержал сообщение о раке мозга. В результате ее усилий через Фонд The Cure Starts Now Foundation было собрано более 2,2 миллиона долларов на исследования DIPG. [ 32 ]
В популярной культуре
[ редактировать ]«Записки, оставленные позади» , научно-популярная книга, опубликованная в 2009 году, рассказывает о девушке по имени Елена Дессерих. Дессерих оставила своей семье сотни записок, прежде чем умерла от ДИПГ в возрасте 6 лет. [ 33 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с «Диффузная внутренняя глиома моста (ДИПГ)» . Детская исследовательская больница Св. Иуды . Проверено 12 марта 2023 г.
- ^ «Прогноз диффузной срединной глиомы (ДИПГ)» . thebraintumourcharity.org . Проверено 12 марта 2023 г.
- ^ Опухоли центральной нервной системы (5-е изд.). Международное агентство по исследованию рака. 2022. стр. 69–73. ISBN 9789283245087 .
- ^ Ванан М.И., Эйзенштат Д.Д. (2015). «ДИПГ у детей – чему мы можем научиться из прошлого?» . Границы онкологии . 5 : 237. doi : 10.3389/fonc.2015.00237 . ПМК 4617108 . ПМИД 26557503 .
- ^ Бейкер С.Дж., Эллисон Д.В., Гутманн Д.Х. (июнь 2016 г.). «Детские глиомы как нарушения нервного развития» . Глия . 64 (6): 879–895. дои : 10.1002/glia.22945 . ПМЦ 4833573 . ПМИД 26638183 .
- ^ Уильямс Дж.Р., Янг К.С., Витанза Н.А., МакГрат М., Фероз А.Х., Броуд С.Р. и др. (январь 2020 г.). «Прогресс в лечении диффузной внутренней глиомы моста: поддержка стереотаксической биопсии в качестве стандарта медицинской помощи» . Нейрохирургический фокус . 48 (1): Е4. дои : 10.3171/2019.9.FOCUS19745 . ПМИД 31896081 . S2CID 209671910 .
- ^ Бейли С.П., Фигероа М., Мохиуддин С., Заки В., Чандра Дж. (октябрь 2018 г.). «Передовые терапевтические знания, полученные на основе молекулярной биологии детской глиомы высокой степени злокачественности и диффузной внутренней глиомы моста (DIPG)» . Биоинженерия . 5 (4): 88. doi : 10.3390/bioengineering5040088 . ПМК 6315414 . ПМИД 30340362 .
- ^ Jump up to: а б «Статистика ДИПГ» . DIPG.org . Проверено 5 июня 2024 г.
- ^ «Апоптоз: обзор запрограммированной гибели клеток» . www.ncbi.nlm.nih.gov .
- ^ «Диффузные срединные глиомы» . Национальный институт рака . nd Архивировано из оригинала 8 октября 2019 года . Проверено 24 ноября 2019 г. .
- ^ Гупта Н., Гумнерова Л.К., Мэнли П., Чи С.Н., Нойберг Д., Пулигандла М. и др. (октябрь 2018 г.). «Проспективная оценка возможности и безопасности хирургической биопсии у пациентов с впервые диагностированной диффузной внутренней глиомой моста» . Нейроонкология . 20 (11): 1547–1555. дои : 10.1093/neuonc/noy070 . ПМК 6176802 . ПМИД 29741745 .
- ^ «Диффузная внутренняя глиома моста (ДИПГ)» . Детская исследовательская больница Святого Иуды .
- ^ Мюллер С., Тейт Дж.М., Вильянуэва-Мейер Дж.Э., Боннер Э.Р., Нехо Т., Лулла Р.Р. и др. (декабрь 2020 г.). «Массовая цитометрия обнаруживает H3.3K27M-специфические реакции на вакцину при диффузной срединной глиоме» . Журнал клинических исследований . 130 (12): 6325–6337. дои : 10.1172/JCI140378 . ПМЦ 7685729 . ПМИД 32817593 .
- ^ Грассл Н., Пошке И., Линднер К., Бунсе Л., Милденбергер И., Бошерт Т. и др. (октябрь 2023 г.). «Вакцина, нацеленная на H3K27M, для взрослых с диффузной срединной глиомой» . Природная медицина . 29 (10): 2586–2592. дои : 10.1038/s41591-023-02555-6 . ПМЦ 10579055 . ПМИД 37735561 .
- ^ Фишер П.Г., Монже М. (10 мая 2010 г.). «Глиомы ствола мозга в детстве» . Джермантаун, Мэриленд: Фонд опухолей головного мозга у детей.
- ^ Фишер П.Г., Брейтер С.Н., Карсон Б.С., Варам М.Д., Уильямс Дж.А., Вайнгарт Дж.Д. и др. (октябрь 2000 г.). «Клинико-патологическая переоценка классификации опухолей ствола головного мозга. Идентификация пилоцистной астроцитомы и фибриллярной астроцитомы как отдельных образований» . Рак . 89 (7): 1569–1576. doi : 10.1002/1097-0142(20001001)89:7<1569::aid-cncr22>3.0.co;2-0 . ПМИД 11013373 . S2CID 25562391 .
- ^ Дональдсон С.С., Лэнингем Ф., Фишер П.Г. (март 2006 г.). «Прогресс в понимании глиомы ствола мозга». Журнал клинической онкологии . 24 (8): 1266–1272. дои : 10.1200/JCO.2005.04.6599 . ПМИД 16525181 .
- ^ Коронес Д.Н. (май 2007 г.). «Лечение впервые выявленных диффузных глиом ствола головного мозга у детей: в поисках Святого Грааля». Экспертный обзор противораковой терапии . 7 (5): 663–674. дои : 10.1586/14737140.7.5.663 . ПМИД 17492930 . S2CID 39928507 .
- ^ Jump up to: а б с «Рецидив/рецидив – реестр DIPG» . Архивировано из оригинала 9 апреля 2015 года . Проверено 20 декабря 2018 г.
- ^ «Проникновение в мозг: подходы к усилению доставки лекарств в мозг» . Просто еще один день . Архивировано из оригинала 1 июля 2012 года.
- ^ Jump up to: а б Патель М.М., Гоял Б.Р., Бхадада С.В., Бхатт Дж.С., Амин А.Ф. (2009). «Проникновение в мозг: подходы к улучшению доставки лекарств в мозг». Препараты ЦНС . 23 (1): 35–58. дои : 10.2165/0023210-200923010-00003 . ПМИД 19062774 . S2CID 26113811 .
- ^ «МОА Видео» . Архивировано из оригинала 5 мая 2010 г. Проверено 13 апреля 2015 г.
- ^ Холл В.А., Дулиттл Н.Д., Даман М., Брунс П.К., Малдун Л., Фортин Д. и др. (май 2006 г.). «Осмотическая химиотерапия, разрушающая гематоэнцефалический барьер, при диффузных глиомах моста». Журнал нейроонкологии . 77 (3): 279–284. дои : 10.1007/s11060-005-9038-4 . ПМИД 16314949 . S2CID 10779089 .
- ^ Лонсер Р.Р., Уоррен К.Е., Бутман Дж.А., Кесадо З., Робисон Р.А., Уолбридж С. и др. (июль 2007 г.). «Прямая конвективная перфузия внутренних поражений ствола мозга под контролем изображения в реальном времени. Техническое примечание». Журнал нейрохирургии . 107 (1): 190–197. дои : 10.3171/JNS-07/07/0190 . ПМИД 17639894 .
- ^ Таузьед-Эспариат А., Зигфрид А., Уро-Косте Е., Никез И., Кастель Д., Севели А. и др. (август 2022 г.). «Диссеминированные диффузные глиомы средней линии, измененные H3K27, имитирующие диффузные лептоменингеальные глионейрональные опухоли: диагностическая проблема!» . Acta Neuropathologica Communications . 10 (1): 119. дои : 10.1186/s40478-022-01419-3 . ПМЦ 9392342 . ПМИД 35986414 .
- ^ Финдли И.Дж., Де Юлиис Г.Н., Дюшатель Р.Дж., Джексон Э.Р., Витанца Н.А., Кейн Дж.Е. и др. (январь 2022 г.). «Фармако-протеогеномное профилирование диффузной срединной глиомы у детей для обоснования будущих стратегий лечения» . Онкоген . 41 (4): 461–475. дои : 10.1038/s41388-021-02102-y . hdl : 10852/90951 . ПМЦ 8782719 . ПМИД 34759345 .
- ^ Хансен-младший (2005). Первый человек: жизнь Нила А. Армстронга . Нью-Йорк: Саймон и Шустер. стр. 161–164. ISBN 978-0-7432-5631-5 . OCLC 937302502 .
- ^ "Дом" . thecurestartsnow.org .
- ^ "Дом" . Notesleftbehind.com .
- ^ Гибсон С. (14 ноября 2013 г.). «Федеральный закон о педиатрических медицинских исследованиях имени Габриэллы Миллер» . Вашингтон Пост . Проверено 3 февраля 2021 г.
- ^ «Наша история» . Фонд Smashing Walnuts . Проверено 3 февраля 2021 г.
- ^ «Cure Starts Now достигла цели в 2,2 миллиона долларов в честь Лорен Хилл» . Местное 12 января 2016 г. Проверено 03 мая 2021 г.
- ^ "Записки, оставленные шестилетней жертвой рака для семьи, превратились в книгу - Телеграф" . 09.11.2009. Архивировано из оригинала 09.11.2009 . Проверено 4 марта 2023 г.