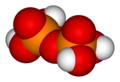
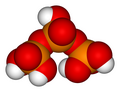
Оксокислота фосфора
В химии , фосфорная оксокислота (или фосфорная кислота ) — общее название любой кислоты которой молекула состоит из атомов фосфора , кислорода и водорода . [ 1 ] Существует потенциально бесконечное число таких соединений. Некоторые из них нестабильны и не выделены, но производные анионы и органические группы присутствуют в стабильных солях и сложных эфирах . Важнейшими из них — в биологии, геологии, промышленности и химических исследованиях — являются фосфорные кислоты , эфиры и соли которых — фосфаты .
В общем, любой атом водорода, связанный с атомом кислорода, является кислым, а это означает, что группа –OH может потерять протон H. +
оставляя отрицательно заряженный – О −
группу и таким образом превращая кислоту в оксоанион фосфора . Каждый дополнительный потерянный протон имеет связанную с ним кислотную константу диссоциации K a 1 , K a 2 K a 3 , ..., часто выражаемую его колорарифмом (pK a 1 , pK a 2 , pK a 3 , ...). Атомы водорода, связанные непосредственно с фосфором, обычно не являются кислыми.
Классификация
[ редактировать ]Оксокислоты фосфора можно классифицировать по степени окисления атома(ов) фосфора, которая может варьироваться от +1 до +5. Атомы кислорода обычно находятся в степени окисления -2, но могут находиться в состоянии -1, если молекула включает пероксидные группы .
Степень окисления +1
[ редактировать ]
- Гипофосфористая кислота (или фосфиновая кислота), H
3 НОЧИ
2 (или H
2 PO(OH) ), монопротонная кислота (это означает, что только один из атомов водорода является кислым). Его соли и эфиры называются гипофосфитами или фосфинатами.
Степень окисления +3
[ редактировать ]
- Фосфористая кислота (или фосфоновая кислота), H
3 НОЧИ
3 (или HPO(OH)
2 ), дипротонная кислота (только с двумя кислыми атомами водорода). Его соли и эфиры называются фосфитами или фосфонатами.
Степень окисления +4
[ редактировать ]
- Гипофосфорная кислота , H
4 П
22О
6 (или (НО)
2 П – П(ОН)
2 ). Все четыре атома водорода являются кислотными. Его соли и эфиры являются гипофосфатами .
Степень окисления +5
[ редактировать ]Наиболее важными членами этой группы являются фосфорные кислоты , где каждый атом фосфора связан с четырьмя атомами кислорода, один из которых посредством двойной связи , расположенной в виде углов тетраэдра . Два или более из этих ПО
4 тетраэдра могут быть соединены общими одинарными атомами кислорода, образуя линейные или разветвленные цепи, циклы или более сложные структуры. Необщие атомы кислорода с одинарной связью дополняются кислыми атомами водорода. Их общая формула: H n - x +2 P n O 3 n - x +1 , где n — количество атомов фосфора, а x — количество фундаментальных циклов в структуре молекулы.
Эти кислоты, а также их эфиры и соли (« фосфаты ») включают некоторые из наиболее известных и наиболее важных соединений фосфора.
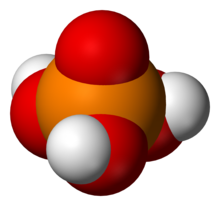
3 НОЧИ
4 .
Самый простой член этого класса:
- Собственно фосфорная кислота (также называемая ортофосфорной кислотой или монофосфорной кислотой), H
3 НОЧИ
4 (или ОП(ОН)
3 ), трипротонная кислота. Он образует ортофосфатные соли и сложные эфиры, обычно называемые фосфатами .
Наименьшие соединения этого класса с двумя или более атомами фосфора называются «олигофосфорными кислотами», а более крупные, с линейными остовами –P–O–, являются «полифосфорными кислотами»; без четкого разделения между ними. Некоторые из наиболее важных членов:
- Пирофосфорная кислота , H
4 П
22О
7 (или (НО)
2 P –O– P(OH)
2 ) с четырьмя кислотными атомами водорода. Образует пирофосфаты . - Трифосфорная кислота (или триполифосфорная кислота), H
5 П
33О
10 (или (НО)
2 P –O– P(OH) –O– P(OH)
2 ) с пятью кислыми атомами водорода. Образует трифосфаты или триполифосфаты. - Тетрафосфорная кислота , H
18:00
4 Ох
13 (или (НО)
2 P (–O– P(OH) ) 2 –O– P(OH)
2 ) с шестью кислыми атомами водорода. Образует тетрафосфаты .
Позвоночник может быть разветвленным, например:
- Трифосфонофосфорная кислота , H
18:00
4 Ох
13 или P(O)(– OP(O)(OH)
2 ) 3 , разветвленный изомер тетраполифосфорной кислоты.
ПО
4 тетраэдра могут быть соединены с образованием замкнутых цепочек –P–O–, например:
- Триметафосфорная кислота (или циклотрифосфорная кислота), H
33П
33О
9 (или (HPO
3 )
3 , (–P(O)(OH)–O–) 3 ), циклическая молекула с тремя кислотными атомами водорода. Образует триметафосфатные соли и сложные эфиры.
Метафосфорная кислота — это общий термин для фосфорных кислот с одним циклом (–P(O)(OH)–O–) n которых , элементарная формула – HPO.
3 .
-
Тетраполифосфорная кислота
Ч 6 П 4 О 13 -
Триметафосфорная кислота
ЧАС
33П
33О
9
Еще одним соединением, которое можно включить в этот класс, является
- Пероксомонофосфорная кислота , H 3 PO 5 (или OP(OH) 2 (OOH)), которую можно рассматривать как монофосфорную кислоту с перекисной группой, замещающей атом кислорода в одной из гидроксильных групп.
Смешанные степени окисления
[ редактировать ]Некоторые оксокислоты фосфора имеют два или более атома P в разных степенях окисления. Одним из примеров является
- Изогипофосфорная кислота , H
4 П
22О
6 (или H(OH)(O)P-O-P(O)(OH) 2 ), тетрапротонная кислота и изомер гипофосфорной кислоты, содержащий P в степени окисления +3 и +5.

П 4 О 10

См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
Дальнейшее чтение
[ редактировать ]- Шредер Х.К., Курц Л., Мюллер В.Е., Лоренц Б. (март 2000 г.). «Полифосфат в кости» (PDF) . Биохимия (Москва) . 65 (3): 296–303. Архивировано из оригинала (PDF) 25 августа 2011 г.
Внешние ссылки
[ редактировать ]- Определение полифосфатов с использованием ионной хроматографии с детектированием по подавленной проводимости, Примечание по применению 71 от Dionex
- США 3044851 , Янг, Дональд К., «Производство фосфатов аммония и продуктов из него», опубликован 17 июля 1962 г., передан Collier Carbon & Chemical Co.
- Фосфор + кислоты Национальной медицинской библиотеки США в медицинских предметных рубриках (MeSH)