Дифосфор
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Дифосфор | |||
| Систематическое название ИЮПАК Дифосфин [1] | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ЧЭБИ | |||
| ХимическийПаук | |||
| 1400241 | |||
ПабХим CID | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| П 2 | |||
| Молярная масса | 61.947 523 996 g·mol −1 | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Дифосфор представляет собой неорганическое химическое вещество с химической формулой P.
2 . В отличие от азота, своего более легкого соседа пниктогена , который образует стабильную молекулу N 2 азот-азот с тройной связью , фосфор предпочитает тетраэдрическую форму P 4 , поскольку пи-связи PP имеют высокую энергию. Таким образом, дифосфор очень реакционноспособен: энергия диссоциации связи (117 ккал / моль или 490 кДж /моль) вдвое меньше, чем у динитрогена . Расстояние связи было измерено и составило 1,8934 Å. [2]
Синтез
[ редактировать ]Дифосфор был получен путем нагревания белого фосфора при температуре 1100 Кельвинов (827 °C ). Тем не менее, были получены некоторые успехи в получении двухатомной молекулы в гомогенном растворе при нормальных условиях с использованием некоторых переходных металлов комплексов (на основе, например, вольфрама и ниобия ). [3] методы диссоциации связей в Р 4 молекулах посредством фотовозбуждения . Предложены также [4]
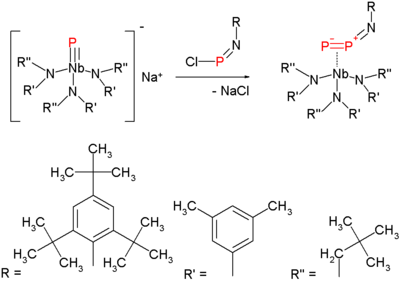
Молекула привлекла внимание в 2006 году, когда появился новый метод ее синтеза при более мягких температурах. [3] Этот метод представляет собой разновидность вытеснения азота из азидов с образованием нитрена . Синтез предшественника дифосфора состоит из реакции терминального ниобия фосфида с хлориминофосфаном:
Нагревание этого соединения при 50 ° C в 1,3-циклогексадиене, служащем растворителем и улавливающим реагентом, приводит к удалению дифосфора, который является реакционноспособным, поскольку конечными продуктами являются двойной аддукт Дильса-Альдера и имидосоединение ниобия:
Такое же имидосоединение образуется и при термолизе в толуоле , но в этом случае судьба дифосфора неизвестна.
P 2 Предполагается, что образуется в качестве промежуточного продукта при фотолизе P 4 , [5] а в присутствии 2,3-диметил-1,3-бутадиена вновь образуется дифосфан, образующийся в результате присоединения Дильса-Альдера. [6] На сегодняшний день прямых доказательств образования P 2 посредством фотолиза P 4 не существует.
Сообщалось об образовании дифосфора из аддукта дифосфор-бисантрацена. [7] Синтез стабилизированного HP 2 + Сообщалось о катионе. [8]
Ссылки
[ редактировать ]- ^ «Дифосфор (ЧЕБИ:33472)» . Химические соединения биологического интереса (ХЭБИ) . Великобритания: Европейский институт биоинформатики.
- ^ Хубер, КП; Герцберг, Г. (1979). Молекулярные спектры и молекулярная структура IV. Константы двухатомных молекул . Нью-Йорк: Ван Ностранд. ISBN 978-0442233945 .
- ^ Jump up to: а б Пиро, Николас А.; Фигероа, Джошуа С.; МакКеллар, Джессика Т.; Камнинс, Кристофер К. (1 сентября 2006 г.). «Реакционная способность молекул дифосфора с тройной связью». Наука . 313 (5791): 1276–1279. Бибкод : 2006Sci...313.1276P . дои : 10.1126/science.1129630 . ПМИД 16946068 . S2CID 27740669 .
- ^ Ли-Пин Вангб; Дэниел Тофана; Цзяхао Чена; Трой Ван Вурхиса и Кристофер К. Камминс (сентябрь 2013 г.). «Путь к дифосфору в результате диссоциации фотовозбужденного тетрафосфора» . РСК Прогресс . 3 (45). Королевское химическое общество: 23166. Бибкод : 2013RSCAd...323166W . дои : 10.1039/C3RA43940B . hdl : 1721.1/90977 . Архивировано из оригинала 21 июля 2017 г. Проверено 21 июля 2017 г.
- ^ Ратенау, Г. (июнь 1937 г.). «Оптические и фотохимические испытания с фосфором». Физика (на немецком языке). 4 (6): 503–514. Бибкод : 1937Phy.....4..503R . дои : 10.1016/S0031-8914(37)80084-1 .
- ^ Тофан, Дэниел; Камминс, Кристофер К. (26 августа 2010 г.). «Фотохимическое включение дифосфорных звеньев в органические молекулы». Angewandte Chemie, международное издание . 49 (41): 7516–7518. дои : 10.1002/anie.201004385 . ПМИД 20799313 .
- ^ Ретро-путь Дильса-Альдера к химии дифосфора: синтез молекулярных предшественников, кинетика переноса P2 в 1,3-диены и обнаружение P2 с помощью молекулярно-лучевой масс-спектрометрии Александра Велиан, Мэтью Нава, Мануэль Темпрадо, Ян Чжоу, Роберт В. Филд и Кристофер К. Камминс Журнал Американского химического общества 2014 136 (39), 13586-13589 дои : 10.1021/ja507922x
- ^ Протонирование карбен-стабилизированного дифосфора: комплексообразование HP2+ Ючжун Ван, Хантер П. Хикокс, Яомин Се, Пингронг Вэй, Дунтао Цуй, Мелоди Р. Уолтер, Генри Ф. Шефер III и Грегори Х. Робинсон Chem. Коммун., 2016, два : 10.1039/C6CC01759B
Внешние ссылки
[ редактировать ]- Рон Дагани, «Мягкий путь к P2», Новости химии и инженерии , 4 сентября 2006 г. Ссылка
- Кармен Драль «Вспышка инноваций в химии фосфора», Новости химии и техники , 13 сентября 2010 г. Ссылка