Синтез кетона Вайнреба
| Синтез кетона Вайнреба | |
|---|---|
| Назван в честь | Стивен М. Вайнреб |
| Тип реакции | Реакция сцепления |
| Идентификаторы | |
| Портал органической химии | Weinreb-кетон-синтез |
Синтез кетонов Вайнреба или синтез кетонов Вайнреба-Нама представляет собой химическую реакцию, используемую в органической химии для образования связей углерод-углерод . Он был открыт в 1981 году Стивеном М. Вайнребом и Стивеном Намом как метод синтеза кетонов . [ 1 ] Первоначальная реакция включала два последующих нуклеофильных ацильных замещения : преобразование хлорангидрида с N , O - диметилгидроксиламином с образованием амида Вейнреба-Нама и последующую обработку этого вида металлоорганическим реагентом, таким как реактив Гриньяра или литийорганический реагент . Нам и Вайнреб также сообщили о синтезе альдегидов путем восстановления амида Восстановление избытком алюмогидрида лития (см. амида ).

Основное преимущество этого метода перед добавлением металлоорганических реагентов к более типичным ацильным соединениям заключается в том, что он позволяет избежать распространенной проблемы избыточного добавления. В этих последних реакциях два эквивалента входящей группы присоединяются с образованием спирта, а не кетона или альдегида. Это происходит даже в том случае, если эквиваленты нуклеофила строго контролируются.

С тех пор амид Вайнреба-Нама стал регулярно использоваться химиками-органиками в качестве надежного метода синтеза кетонов. Эти функциональные группы присутствуют во многих природных продуктах и могут надежно вступать в реакцию с образованием новых углерод-углеродных связей или превращаться в другие функциональные группы. Этот метод был использован в ряде синтезов, в том числе макросфелидов A и B, [ 2 ] амфидинолид J, [ 3 ] и спирофунгины А и В. [ 4 ]
Механизм
[ редактировать ]Вайнреб и Нам первоначально предложили следующий механизм реакции , чтобы объяснить селективность, проявляющуюся в реакциях амида Вейнреба-Нама. Их предположение заключалось в том, что тетраэдрический промежуточный продукт ( A ниже), образующийся в результате нуклеофильного присоединения металлоорганического реагента , стабилизируется за счет хелатирования метоксигруппы , как показано. [ 1 ] Этот промежуточный продукт стабилен только при низких температурах, требуя низкотемпературной закалки .

Это хелатирование противоречит механизму образования продукта избыточного присоединения, при котором коллапс тетраэдрического промежуточного соединения позволяет осуществить второе присоединение. Механистическая гипотеза Вайнреба была немедленно принята академическим сообществом, но только в 2006 году она была подтверждена спектроскопическим и кинетическим анализом. [ 5 ]
Подготовка
[ редактировать ]В дополнение к оригинальной процедуре, показанной выше (которая может иметь проблемы совместимости с чувствительными субстратами), амиды Вейнреба можно синтезировать из множества ацильных соединений. В подавляющем большинстве этих процедур используется коммерчески доступная соль гидрохлорида N,O-диметилгидроксиламина [MeO(Me)NH•HCl], с которой обычно легче обращаться, чем со свободным амином. [ 6 ]
Обработка сложного эфира или лактона AlMe 3 или AlMe 2 Cl дает соответствующий амид Вейнреба с хорошими выходами. Альтернативно, для активации амина перед добавлением сложного эфира можно использовать ненуклеофильные реагенты Гриньяра, такие как изопропилмагнийхлорид. [ 7 ]

различные реагенты для связывания пептидов Для получения амидов Вейнреба-Нама из карбоновых кислот также можно использовать о различных сочетаниях на основе карбодиимида , гидроксибензотриазола и трифенилфосфина . . Специально для этой цели сообщалось [ 6 ] [ 7 ]

Наконец, реакция аминокарбонилирования, о которой сообщил Стивен Бухвальд, позволяет превращать арилгалогениды непосредственно в ариламиды Вайнреба-Нама. [ 8 ]

Объем
[ редактировать ]Известно, что стандартные условия синтеза кетонов Вейнреба-Нама допускают наличие широкого спектра функциональных групп в других частях молекулы, включая замещение альфа-галогена, N-защищенные аминокислоты , α-β-ненасыщенность, силиловые эфиры , различные лактамы и лактоны. сульфонаты , сульфинаты и сложные эфиры фосфоновой кислоты. [ 6 ] [ 7 ] В сочетании с амидом можно использовать самые разнообразные нуклеофилы. литиаты и реактивы Гриньяра Чаще всего используются примерах с участием алифатических , винильных , ариловых и алкинилуглеродных нуклеофилов . ; Сообщалось о Однако в случае высокоосновных или стерически затрудненных нуклеофилов отщепление метоксидного фрагмента с высвобождением формальдегида может происходить как значительная побочная реакция. [ 9 ]

Тем не менее, амид Вайнреба-Нама играет важную роль во многих синтезах, выступая в качестве важного партнера для связывания различных фрагментов. Ниже показаны ключевые этапы с участием амидов Вайнреба в синтезе нескольких натуральных продуктов, включая членов семейства иммунодепрессантов макросфелидов и антибиотиков семейства спирофунгинов. [ 2 ] [ 3 ] [ 4 ]

Вариации
[ редактировать ]Реакция амидов Вайнреба-Нама с реагентами Виттига была проведена во избежание иногда жестких условий, необходимых для добавления гидридных реагентов или металлоорганических соединений. В результате образуется N-метил-N-метоксиенамин , который при гидролитической обработке превращается в соответствующий кетон или альдегид. [ 10 ]

Кроме того, был разработан однореакторный магний-галогеновый обмен с последующим арилированием, демонстрирующий стабильность амида Вайнреба-Нама и обеспечивающий простой в эксплуатации метод синтеза арилкетонов. [ 11 ]
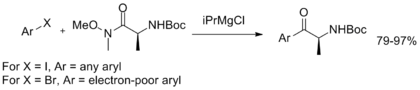
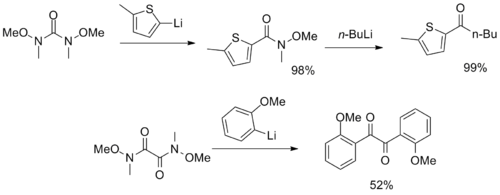
Были синтезированы более необычные реагенты с несколькими амидными функциональными группами Вейнреба-Нама, служащие CO 2 и α-дикетона синтонами . [ 12 ] [ 13 ]
Наконец, Стивен Г. Дэвис из Оксфорда разработал хиральное вспомогательное вещество , которое сочетает в себе функциональность амида Вайнреба с функциональностью вспомогательного вещества псевдоэфедрина Майерса , обеспечивая диастереоселективное енолятное алкилирование с последующим легким расщеплением до соответствующего энантиообогащенного альдегида или кетона. [ 14 ]

См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б Нам, С.; Вайнреб, С.М. (1981), «N-метокси-н-метиламиды как эффективные ацилирующие агенты», Tetrahedron Letters , 22 (39): 3815–3818, doi : 10.1016/s0040-4039(01)91316-4
- ^ Jump up to: а б Паек, С.-М.; Со, С.-Ю.; Ким, С.-Х.; Юнг, Дж.-В.; Ли, Ю.-С.; Юнг, Ж.-К.; Эх, Ю.-Г. (2005), «Краткий синтез (+)-макросфелидов A и B», Organic Letters , 7 (15): 3159–3162, doi : 10.1021/ol0508429 , PMID 16018610
- ^ Jump up to: а б Барбазанж, М.; Мейер, К.; Косси, Дж. (2008), «Тотальный синтез амфидинолида J», Organic Letters , 10 (20): 4489–4492, doi : 10.1021/ol801708x , PMID 18811171
- ^ Jump up to: а б Симидзу, Т.; Сато, Т.; Муракоши, К.; Содеока, М. (2005), «Асимметричный полный синтез (-)-спирофунгина А и (+)-спирофунгина B», Organic Letters , 7 (25): 5573–5576, doi : 10.1021/ol052039k , PMID 16320994
- ^ Цюй, Б.; Коллум, Д.Б. (2006), «Механизм ацилирования фенилацетилида лития амидом Вайнреба», Журнал органической химии , 71 (18): 7117–7119, doi : 10.1021/jo061223w , PMID 16930080
- ^ Jump up to: а б с Сингх, Дж.; Сатьямурти, Н.; Эйдхен, И.С. (2000), «Растущая синтетическая полезность амида Вайнреба», Journal für praktische Chemie , 342 : 340, doi : 10.1002/(sici)1521-3897(200004)342:4<340::aid-prac340> 3.0.co;2-1
- ^ Jump up to: а б с Менцель, М.; Хоффманн, HMR (1997), «N-метокси-N-метиламиды (амиды Вайнреба) в современном органическом синтезе», Journal for Practice Chemistry/Chemiker-Zeitung , 339 : 517–524, doi : 10.1002/prac.19973390194
- ^ Мартинелли-младший; Фрекманн, DMM; Бухвальд, С.Л. (2006), «Удобный метод получения амидов Вайнреба посредством Pd-катализируемого аминокарбонилирования арилбромидов при атмосферном давлении», Organic Letters , 8 (21): 4843–4846, doi : 10.1021/ol061902t , PMID 17020317
- ^ Грэм, СЛ; Шольц, Т.Х. (1990), «Новый способ реакционной способности N-метокси-N-метиламидов с сильноосновными реагентами», Tetrahedron Letters , 31 (44): 6269–6272, doi : 10.1016/s0040-4039(00)97039 -4
- ^ Хислер, К.; Триполи, Р.; Мерфи, Дж. А. (2006), «Реакции амидов Вайнреба: образование альдегидов по реакциям Виттига», Tetrahedron Letters , 47 (35): 6293–6295, doi : 10.1016/j.tetlet.2006.06.118
- ^ Конрад, К.; Сяо, Ю.; Миллер, Р. (2005), «Практический однореакторный процесс синтеза α-аминоарилкетона», Tetrahedron Letters , 46 (49): 8587–8589, doi : 10.1016/j.tetlet.2005.09.183
- ^ Уиппл, WL; Райх, HJ (1991), «Использование N,N'-диметокси-N,N'-диметилмочевины в качестве эквивалента карбонильного дикатиона в реакциях металлоорганического присоединения. Синтез несимметричных кетонов», Журнал органической химии , 56 (8): 2911–2912, номер документа : 10.1021/jo00008a057.
- ^ Сиби, член парламента; Шарма, Р.; Полсон, К.Л. (1992), «N,N'-Диметокси-N,N-Диметилэтандиамид: полезный α-оксо-N-метокси-N-метиламид и синтон 1,2-дикетона», Tetrahedron Letters , 33 : 1941, дои : 10.1016/0040-4039(92)88108-h
- ^ Дэвис, СГ; Гудвин, CJ; Хепворт, Д.; Робертс, премьер-министр; Томсон, Дж. Э. (2010), «О происхождении диастереоселективности при алкилировании енолятов, полученных из N-1-(1'-нафтил)этил-О-трет-бутилгидроксаматов: эквиваленты хирального амида Вайнреба», Журнал органической химии , 75 (4): 1214–1227, doi : 10.1021/jo902499s , PMID 20095549