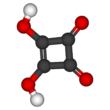
квадратная кислота
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
3,4-Дигидроксициклобут-3-ен-1,2-дион | |||
| Другие имена
Квадратная кислота
Циклобутендиовая кислота | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.018.875 | ||
| Номер ЕС |
| ||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 4 Н 2 О 4 | |||
| Молярная масса | 114.056 g·mol −1 | ||
| Появление | белый кристаллический порошок | ||
| Температура плавления | > 300 ° C (572 ° F; 573 К) | ||
| Кислотность ( pKa ) | р К а1 = 1,5 р К а2 = 3,4 | ||
| Опасности [ 2 ] | |||
| СГС Маркировка : | |||

| |||
| Опасность | |||
| H314 | |||
| P260 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340+P310 , P305+P351+P338 | |||
| точка возгорания | 190 ° С (374 ° F; 463 К) [ 3 ] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Квадратная кислота , также называемая квадратичной кислотой , поскольку ее четыре атома углерода примерно образуют квадрат, представляет собой дипротонную органическую кислоту с химической формулой С 4 О 2 (ОН) 2 . [ 4 ]
Сопряженным основанием квадратной кислоты является водородквадрат-анион. УВ 4 О - 4 ; а сопряженное основание водородквадрат-аниона представляет собой двухвалентный квадратат-анион. С 4 О 2- 4 . Это один из оксоуглеродных анионов , которые состоят только из углерода и кислорода.
Сквариновая кислота является реагентом для химического синтеза , используемым, например, для изготовления светочувствительных сквараиновых красителей и ингибиторов протеинтирозинфосфатаз .
Химические свойства
[ редактировать ]Сквариновая кислота представляет собой белый кристаллический порошок. [ 5 ] Начало термического разложения зависит от различных термодинамических условий, таких как скорость нагрева.
Структура квадратной кислоты не является идеальным квадратом, поскольку длины связей углерод-углерод не совсем равны. Высокая кислотность с p K a1 = 1,5 для первого протона и p a2 = 3,4 для второго обусловлена резонансной стабилизацией аниона K . [ 6 ] Поскольку отрицательные заряды одинаково распределены между каждым атомом кислорода, дианион квадратной кислоты полностью симметричен (в отличие от самой квадратной кислоты) с одинаковой длиной всех связей C-C и одинаковой длиной всех связей C-O.
Производные
[ редактировать ]Во многих реакциях квадратной кислоты участвуют группы ОН. Молекула ведет себя аналогично сильной дикарбоновой кислоте. Это более сильная кислота, чем типичные карбоновые кислоты. [ 7 ]
- C 4 O 2 (OH) 2 → [C 4 O 3 (OH)] − + Ч + , p K a1 = 1,5
- [С 4 О 3 (ОН)] − → [С 4 О 4 ] 2− + Ч + , п К а2 = 3,5
ОН-группы лабильны в квадратной кислоте. образует дихлорид С тионилхлоридом :
- C 4 O 2 (OH) 2 + 2 SOCl 2 → C 4 O 2 Cl 2 + 2 HCl + 2 SO 2
Хлориды являются хорошими уходящими группами, напоминающими хлорангидриды . Их замещают разнообразные нуклеофилы. Таким способом можно получить дитиоскварат. [ 8 ]
Бис(метиловый эфир) получают алкилированием триметилортоформиатом . [ 9 ]
Дибутилкварат используется для лечения бородавок. [ 10 ] и при очаговой алопеции . [ 11 ]
Диэтилскверат использовался в качестве промежуточного продукта в синтезе перзинфотеля . [ нужна ссылка ]
Скварамиды получают замещением алкокси- или хлоридных групп из C 4 O 2 X 2 (X = OR, Cl). [ 8 ] [ 12 ]
Одна или обе кислородные группы (=O) в квадратном анионе могут быть заменены дицианометиленом . =С(CN) 2 . Полученные анионы, такие как 1,2-бис(дицианометилен)кварат и 1,3-бис(дицианометилен)кварат , сохраняют ароматический характер квадрата и были названы псевдооксоуглеродными анионами .
Фотолиз квадратной кислоты в твердой матрице аргона при 10 К (-263 ° C) дает ацетилендиол . [ 13 ]
Координационные комплексы
[ редактировать ]Квадратный дианион ведет себя аналогично оксалату , образуя моно- и полиядерные комплексы с ионами твердых металлов. Гидрат квадрата кобальта(II) Co(C 4 O 4 )·2H 2 O (желтый, кубический) можно получить автоклавированием гидроксида кобальта(II) и квадратной кислоты в воде при 200 °C. Вода связана с атомом кобальта , а кристаллическая структура состоит из кубической структуры полых ячеек, стенки которых представляют собой либо шесть квадратных анионов (оставляя пустоту шириной 7 Å), либо несколько молекул воды (оставляя пустоту 5 Å). [ 14 ]
Дигидроксид квадрата кобальта(II) Co 3 (OH) 2 (C 4 O 4 ) 2 ·3H 2 O (коричневый) получают вместе с предыдущим соединением. Он имеет столбчатую структуру, включающую каналы, заполненные молекулами воды; их можно удалить и заменить, не разрушая кристаллическую структуру. Цепи ферромагнитны ; в гидратной форме они связаны антиферромагнитно, в безводной форме ферромагнитно. [ 14 ]
Синтезированы и охарактеризованы мономерные и димерные разнолигандные комплексы квадрата меди(II). [ 15 ] Сообщается об инфракрасных, электронных и Q-диапазонных спектрах ЭПР, а также магнитной восприимчивости.
Тем же методом получают дигидроксид скварата железа (II). Fe 2 (OH) 2 (C 4 O 4 ) (светло-коричневый). [ 14 ]
Синтез
[ редактировать ]Первоначальный синтез начался с этанолиза перфторциклобутена с получением 1,2-диэтокси-3,3,4,4-тетрафтор-1-циклобутен. Гидролиз дает квадратную кислоту. [ 16 ] [ 4 ]
Хотя это непрактично, квадратные и родственные анионы, такие как дельтат, C 3 O 2− 3 и ацетилендиолят C 2 O 2− 2 получают восстановительным сочетанием оксида углерода с использованием уранорганических комплексов . [ 17 ] [ 18 ]
См. также
[ редактировать ]- Ацетилендиол , H 2 (CO) 2 или НО-C≡C-OH
- Дельтовая кислота , Н 2 (СО) 3
- кроконовая кислота , Н 2 (СО) 5
- Родизоновая кислота , Н 2 (СО) 6
- циклопропенон , C3H2C3H2O
- Циклобутен , С 4 Ч 6
- Скварамид , C 4 O 2 (NH 2 ) 2 , азотистый аналог квадратной кислоты, в котором ОН-группы квадратной кислоты заменены на НХ 2 группы
- Монилиформин , NaC 4 HO 3 , натриевая соль . полуквадратной кислоты
Ссылки
[ редактировать ]- ^ 3,4-Дигидрокси-3-циклобутен-1,2-дион . Сигма-Олдрич
- ^ «ПАСПОРТ БЕЗОПАСНОСТИ» . 21 марта 2021 г.
- ^ 3,4-Дигидрокси-3-циклобутен-1,2-дион, 98+% . Альфа Аесар
- ^ Jump up to: а б Роберт Уэст (1980). «История оксоуглеродов». У Роберта Уэста (ред.). Оксоуглероды . Академическая пресса. стр. 1–14. дои : 10.1016/B978-0-12-744580-9.50005-1 . ISBN 9780127445809 .
- ^ Ли, К.-С.; Квеон, Джей-Джей; Ой, И.-Х.; Ли, CE (2012). «Полиморфный фазовый переход и термическая стабильность в квадратной кислоте ( H
2 С
4 Ох
4 )". J. Phys. Chem. Solids . 73 (7): 890–895. doi : 10.1016/j.jpcs.2012.02.013 . - ^ Уэст, Роберт ; Пауэлл, Дэвид Л. (1963). «Новые ароматические анионы. III. Расчеты молекулярных орбиталей кислородсодержащих анионов». Дж. Ам. хим. Соц. 85 (17): 2577–2579. дои : 10.1021/ja00900a010 .
- ^ «Таблицы кислотности гетероатомных органических кислот и углекислот» .
- ^ Jump up to: а б Артур Х. Шмидт (1980). «Реакции квадратной кислоты и производных квадратной кислоты». Синтез . 1980 (12): 961. doi : 10.1055/s-1980-29291 . S2CID 101871124 .
- ^ Лю, Хуэй; Томука, Крейг С.; Сюй, Саймон Л.; Йеркса, Бенджамин Р.; Салливан, Роберт В.; Сюн, Ифэн; Мур, Гарольд В. (1999). «Диметилкварат и его превращение в 3-этенил-4-метоксициклобутен-1,2-дион и 2-бутил-6-этенил-5-метокси-1,4-бензохинон». Органические синтезы . 76 : 189. дои : 10.15227/orgsyn.076.0189 .
- ^ Сильверберг, Нанетт Б.; Лим, Джозеф К.; Паллер, Эми С.; Манчини, Энтони Дж. (2000). «Иммунотерапия квадратной кислотой бородавок у детей». Журнал Американской академии дерматологии . 42 (5): 803–808. дои : 10.1067/mjd.2000.103631 . ПМИД 10775858 .
- ^ Ёсимасу, Такаши; Фурукава, Фукуми (2016). «Модифицированная иммунотерапия очаговой алопеции». Обзоры аутоиммунитета . 15 (7): 664–667. дои : 10.1016/j.autrev.2016.02.021 . ПМИД 26932732 .
- ^ Ян Сторер, Р.; Асиро, Кэролайн; Джонс, Лин Х. (2011). «Скварамиды: физические свойства, синтез и применение». хим. Соц. Преподобный . 40 (5): 2330–2346. дои : 10.1039/c0cs00200c . ПМИД 21399835 .
- ^ Майер, Гюнтер; Рор, Кристина (1995). «Этиндиол: фотохимическая генерация и матрично-спектроскопическая идентификация». Либигс Аннален . 1996 (3): 307–309. дои : 10.1002/jlac.199619960303 .
- ^ Jump up to: а б с Хитоши, Кумагай; Хидео, Собукава; Мохамедалли, Курму (2008). «Гидротермальный синтез, структура и магнитные свойства координационных каркасов двухвалентных переходных металлов». Журнал материаловедения . 43 (7): 2123–2130. Бибкод : 2008JMatS..43.2123K . дои : 10.1007/s10853-007-2033-8 . S2CID 95205908 .
- ^ Рейнпрехт, JT; Миллер, Дж. Г.; Фогель, ГК; и др. (1979). «Синтез и характеристика квадратных комплексов меди (II)». Неорг. хим., 19, 927-931.
- ^ Парк, Джей Ди; Коэн С. и Лачер-младший (1962). «Реакции гидролиза галогенированных эфиров циклобутена: синтез дикетоциклобутендиола». Дж. Ам. хим. Соц. 84 (15): 2919–2922. дои : 10.1021/ja00874a015 .
- ^ Фрей, Алистер С.; Клок, Ф. Джеффри Н.; Хичкок, Питер Б. (2008). «Механистические исследования восстановительной циклоолигомеризации CO смешанными сэндвич-комплексами U(III); молекулярная структура [(U(η-C 8 H 6 {Si′Pr 3 -1,4} 2 )(η-Cp * )] 2 (m-n 1 :или 1 -C 2 O 2 )». Журнал Американского химического общества . 130 (42): 13816–13817. doi : 10.1021/ja8059792 . PMID 18817397 .
- ^ Саммерскейлс, Оуэн Т.; Фрей, Алистер СП; Клок, Ф. Джеффри Н.; Хичкок, Питер Б. (2009). «Восстановительное диспропорционирование диоксида углерода до карбонатных и квадратных продуктов с использованием смешанного сэндвич-комплекса U (III)». Химические коммуникации (2): 198–200. дои : 10.1039/b815576c . ПМИД 19099067 .