стауроспорин
 | |
 | |
| Клинические данные | |
|---|---|
| код АТС |
|
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЭБ | |
| ХЭМБЛ | |
| PDB-лиганд | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.109.946 |
| Химические и физические данные | |
| Формула | С 28 Н 26 Н 4 О 3 |
| Молярная масса | 466.541 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Стауроспорин (антибиотик AM-2282 или STS) представляет собой натуральный продукт, первоначально выделенный в 1977 году из бактерии Streptomyces staurosporeus . [ 1 ] Это был первый из более чем 50 алкалоидов , у которых была обнаружена такая бис-индольная химическая структура. Химическая структура стауроспорина была выяснена методом рентгеновской кристаллографии в 1994 году. [ 2 ]
Было обнаружено, что стауроспорин обладает биологической активностью от противогрибковой до антигипертензивной. [ 3 ] Интерес к этой деятельности привел к масштабным исследованиям в области химии и биологии и открытию возможностей лечения рака.
Биологическая деятельность
[ редактировать ]Основная биологическая активность стауроспорина заключается в за счет ингибировании протеинкиназ предотвращения связывания АТФ с киназой. Это достигается за счет более сильного сродства стауроспорина к АТФ-связывающему участку киназы. Стауроспорин является прототипом АТФ-конкурентного ингибитора киназы, поскольку он связывается со многими киназами с высоким сродством, хотя и с небольшой селективностью. [ 4 ] Структурный анализ киназных карманов показал, что атомы основной цепи, которые консервативны в своих положениях относительно стауроспорина, способствуют беспорядочным связям стауроспорина. [ 5 ] Отсутствие специфичности препятствовало его клиническому использованию, но сделало его ценным исследовательским инструментом. В исследованиях стауроспорин используется для индукции апоптоза . Механизм того, как это опосредует это, не совсем понятен. Было обнаружено, что одним из способов индукции апоптоза стауроспорином является активация каспазы-3 . [ 6 ] В более низких концентрациях, в зависимости от типа клеток, стауроспорин индуцирует специфические эффекты клеточного цикла, останавливая клетки либо в фазе G1 , либо в фазе G2 клеточного цикла. [ 7 ]
Химическая семья
[ редактировать ]Стауроспорин представляет собой индолокарбазол . Он принадлежит к наиболее часто выделяемой группе индолкарбазолов: индоло(2,3-а)карбазолы. Из них стауроспорин относится к наиболее распространенной подгруппе, называемой индоло(2,3-а)пиррол(3,4-с)карбазолами. Они делятся на два класса – галогенированные (хлорированные) и негалогенированные. Галогенированные индоло(2,3-а)пиррол(3,4-с)карбазолы имеют полностью окисленный углерод C-7 и только один индольный азот, содержащий β-гликозидную связь, тогда как негалогенированные индоло(2,3-а) Пиррол(3,4-с)карбазолы имеют как гликозилированный индольный азот, так и полностью восстановленный углерод C-7. Стауроспорин относится к негалогенированному классу. [ 8 ]
Стауроспорин является предшественником нового ингибитора протеинкиназы мидостаурина (PKC412). [ 9 ] [ 10 ] Помимо мидостаурина, стауроспорин также используется в качестве исходного материала при коммерческом синтезе K252c (также называемого стауроспориновым агликоном). В естественном пути биосинтеза K252c является предшественником стауроспорина.

Биосинтез
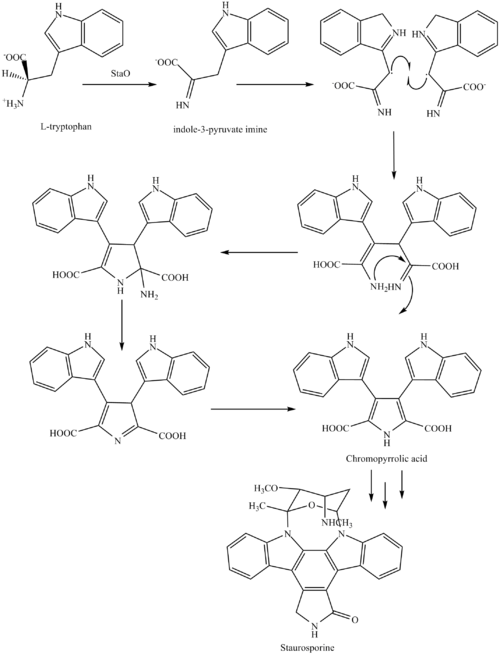
[ редактировать ]Биосинтез стауроспорина начинается с аминокислоты L-триптофана в ее цвиттер-ионной форме. Триптофан превращается в имин под действием фермента StaO, который представляет собой оксидазу L-аминокислот (который может зависеть от FAD). StaD воздействует на имин с образованием нехарактерного промежуточного продукта, который, как предполагается, является продуктом димеризации между двумя молекулами имина. Хромопирроловая кислота — это молекула, образующаяся из этого промежуточного продукта после потери VioE (используемого в биосинтезе виолацеина — природного продукта, образующегося из точки ветвления этого пути, который также расходится с образованием ребеккамицина ). Считается, что арил-арильное соединение катализируется происходит фермент цитохрома P 450 с образованием ароматической кольцевой системы. [ 8 ]
За этим следует нуклеофильная атака между атомами азота индола, приводящая к циклизации, а затем декарбоксилированию, которому способствует StaC исключительно с образованием агликона стауроспорина или K252c. Глюкоза преобразуется в NTP-L-ристоамин с помощью StaA/B/E/J/I/K, который затем добавляется к агликону стауроспорина по 1 индолу N с помощью StaG. Фермент StaN переориентирует сахар, присоединяя его ко 2-му индольному азоту в неблагоприятную конформацию с образованием промежуточного O-деметил-N-деметилстауроспорина. Наконец, O-метилирование 4'амина StaMA и N-метилирование 3'-гидрокси StaMB приводит к образованию стауроспорина. [ 8 ]
Исследования в доклиническом использовании
[ редактировать ]Показано, что стауроспорин , инкапсулированный в липосомальные наночастицы , подавляет опухоли in vivo на мышиной модели без токсических побочных эффектов, которые запрещают его использование в качестве противоракового препарата с высокой апоптотической активностью. Исследователи из Онкологического центра Мурса Калифорнийского университета в Сан-Диего разрабатывают платформенную технологию, обеспечивающую высокую эффективность загрузки лекарств путем управления рН среды клеток. При инъекции в модель глиобластомы мышей стауроспорин накапливается преимущественно в опухоли, что подтверждается флуоресцентным подтверждением, и мыши не страдают от потери веса по сравнению с контрольными мышами, которым вводили свободное соединение, что является показателем пониженной токсичности. [ 11 ] [ 12 ]
Список соединений, тесно связанных со стауроспорином
[ редактировать ]Ссылки
[ редактировать ]- ^ Омура С., Иваи Ю., Хирано А., Накагава А., Авая Дж., Цучья Х. и др. (апрель 1977 г.). «Новый алкалоид АМ-2282 происхождения Streptomyces. Таксономия, ферментация, выделение и предварительная характеристика» . Журнал антибиотиков . 30 (4): 275–282. дои : 10.7164/антибиотики.30.275 . ПМИД 863788 .
- ^ Фунато Н., Такаянаги Х., Конда Ю., Тода Ю., Харигая Ю., Омура С. (1994). «Абсолютная конфигурация стауроспорина по данным рентгеноструктурного анализа». Тетраэдр Летт . 35 (8): 1251–1254. дои : 10.1016/0040-4039(94)88036-0 .
- ^ Рюэгг, Юта, генеральный директор Берджесс (июнь 1989 г.). «Стауроспорин, К-252 и UCN-01: мощные, но неспецифические ингибиторы протеинкиназ». Тенденции в фармакологических науках . 10 (6): 218–20. дои : 10.1016/0165-6147(89)90263-0 . ПМИД 2672462 .
- ^ Караман М.В., Херргард С., Трейбер Д.К., Галлант П., Аттеридж К.Э., Кэмпбелл Б.Т. и др. (январь 2008 г.). «Количественный анализ селективности ингибиторов киназ». Природная биотехнология . 26 (1): 127–132. дои : 10.1038/nbt1358 . ПМИД 18183025 . S2CID 205273598 .
- ^ Танрамлюк Д., Шрайер А., Питт В.Р., Бланделл Т.Л. (июль 2009 г.). «О происхождении селективности и распущенности ингибиторов ферментов: тематическое исследование связывания протеинкиназы со стауроспорином» . Химическая биология и дизайн лекарств . 74 (1): 16–24. дои : 10.1111/j.1747-0285.2009.00832.x . ПМЦ 2737611 . ПМИД 19519740 .
- ^ Че Х.Дж., Кан Дж.С., Бён Дж.О., Хан К.С., Ким Д.У., О СМ и др. (октябрь 2000 г.). «Молекулярный механизм стауроспорин-индуцированного апоптоза в остеобластах». Фармакологические исследования . 42 (4): 373–381. дои : 10.1006/phrs.2000.0700 . ПМИД 10987998 .
- ^ Бруно С., Ардельт Б., Скиерски Дж.С., Траганос Ф., Даржинкевич З. (январь 1992 г.). «Различные эффекты стауроспорина, ингибитора протеинкиназ, на клеточный цикл и структуру хроматина нормальных и лейкемических лимфоцитов». Исследования рака . 52 (2): 470–473. ПМИД 1728418 .
- ^ Jump up to: а б с Райан КС (2008). «Структурные исследования ферментов биосинтеза ребеккамицина, стауроспорина и виолацеина» (PDF) . доктор философии Диссертация . Массачусетский технологический институт. Архивировано из оригинала (PDF) 14 марта 2012 г.
- ^ Мидостаурин. Архивировано 1 сентября 2014 г. на странице продукта Wayback Machine , Fermentek.
- ^ Ван Ю, Инь О.К., Граф П., Кисицки Дж.К., Шран Х. (июнь 2008 г.). «Дозо- и временная фармакокинетика мидостаурина у больных сахарным диабетом». Журнал клинической фармакологии . 48 (6): 763–775. дои : 10.1177/0091270008318006 . ПМИД 18508951 . S2CID 26657407 .
- ^ Пресс-релиз (21 октября 2013 г.). «Исследование выявило безопасную систему доставки сложных, но очень эффективных противораковых соединений» . Система здравоохранения Калифорнийского университета в Сан-Диего . Проверено 27 октября 2013 г.
- ^ Муктаварам Р., Цзян П., Саклеча Р., Симберг Д., Бхарати И.С., Номура Н. и др. (2013). «Высокоэффективная липосомальная инкапсуляция ингибитора тирозинкиназы приводит к улучшению токсичности in vivo и профиля реакции опухоли» . Международный журнал наномедицины . 8 (1): 3991–4006. дои : 10.2147/IJN.S51949 . ПМЦ 3808212 . ПМИД 24174874 .