Молекулярное сито
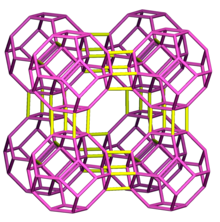

Молекулярное сито – это материал с порами одинакового размера. Эти поры по диаметру аналогичны размерам малых молекул, и поэтому большие молекулы не могут проникать или адсорбироваться , в то время как более мелкие молекулы могут. Когда смесь молекул мигрирует через неподвижный слой пористого полутвердого вещества, называемый ситом (или матрицей), компоненты с наибольшей молекулярной массой (которые не могут пройти в молекулярные поры) покидают слой первыми, за которыми следуют последовательно более мелкие молекулы. Некоторые молекулярные сита используются в эксклюзионной хроматографии — методе разделения, который сортирует молекулы по их размеру. Другое важное применение — в качестве осушителя . Большинство молекулярных сит представляют собой алюмосиликатные цеолиты с молярным соотношением Si/Al менее 2, но есть также примеры активированного угля и силикагеля . [1]
Диаметр пор молекулярного сита измеряется в ангстремах (Å) или нанометрах (нм). Согласно обозначениям ИЮПАК , микропористые материалы имеют диаметр пор менее 2 нм (20 Å), а макропористые материалы имеют диаметр пор более 50 нм (500 Å); Таким образом, категория мезопор находится посередине с диаметром пор от 2 до 50 нм (20–500 Å). [2]
Материалы [ править ]
Молекулярные сита могут представлять собой микропористый , мезопористый или макропористый материал .
Микропористый материал (<2 нм) [ править ]
- Цеолиты ( алюмосиликатные минералы , не путать с силикатами алюминия )
- Цеолит LTA: 3–4 Å [3]
- Цеолит FAU: 7-10 Å
- Пористое стекло : 10 Å (1 нм) и выше.
- Активный уголь : 0–20 Å (0–2 нм) и выше.
- Глины
- Монтмориллонитовые смеси
- Галлуазит (энделлит): обнаружены две распространенные формы: при гидратации глина имеет расстояние между слоями 1 нм, а при обезвоживании (метагаллуазит) расстояние между слоями составляет 0,7 нм. В природе галлуазит встречается в виде небольших цилиндров диаметром в среднем 30 нм и длиной от 0,5 до 10 микрометров. [4]
- Монтмориллонитовые смеси
материал (2–50 Мезопористый ) нм
- Диоксид кремния (используется для изготовления силикагеля ): 24 Å (2,4 нм). [5]
Макропористый материал (>50 нм) [ править ]
- Макропористый кремнезем, 200–1000 Å (20–100 нм) [6]
Приложения [ править ]
Молекулярные сита часто используются в нефтяной промышленности, особенно для осушки газовых потоков. Например, в промышленности сжиженного природного газа (СПГ) содержание воды в газе необходимо снизить до уровня менее 1 ppmv , чтобы предотвратить закупорку, вызванную льдом или клатратом метана .
В лаборатории для сушки растворителя используются молекулярные сита. «Сита» доказали свое превосходство над традиционными методами сушки, в которых часто используются агрессивные осушители . [7]
Под термином «цеолиты» молекулярные сита используются для широкого спектра каталитических применений. Они катализируют изомеризацию , алкилирование и эпоксидирование и используются в крупномасштабных промышленных процессах, включая гидрокрекинг и каталитический крекинг с флюидом . [8]
Они также используются для фильтрации воздуха, подаваемого в дыхательные аппараты, например, используемые аквалангистами и пожарными . В таких случаях воздух подается воздушным компрессором и проходит через картриджный фильтр, который, в зависимости от применения, заполнен молекулярными ситами и/или активированным углем , и в конечном итоге используется для заправки резервуаров с воздухом для дыхания. [9] Такая фильтрация позволяет удалить частицы и продукты выхлопа компрессора из подаваемого воздуха для дыхания.
Морфология молекулярных сит [ править ]

Молекулярные сита доступны в различных формах и размерах. Молекулярные сита можно использовать непосредственно в механизированной форме во многих приложениях, например, в изоляционном стекле или покрытиях . Однако, чтобы сделать обращение с материалом более удобным, особенно для регенеративных процессов, порошок молекулярного сита обычно смешивают с глиняным формуют в экструдат или шарики . связующим материалом и перед активацией [10]
Первоначально смесь молекулярного сита, цеолита и глиняного связующего вещества экструдировали в форме таблеток. Хотя гранулы по-прежнему широко используются, производители со временем начали придавать смеси форму шариков, что обеспечивает более благоприятные адсорбционные характеристики. В зависимости от условий процесса и размера технологической камеры экструдаты и шарики доступны в различных номинальных размерах . Например, в промышленных процессах обезвоживания этанола используются более крупные гранулы размером 4x8, поскольку технологические камеры большие, до 40 футов в высоту и более. [11] С другой стороны, портативный концентратор кислорода использует гранулы меньшего размера, примерно 20x40 меш, что обеспечивает более высокую производительность в сосуде меньшего размера за счет улучшения скорости адсорбции/ десорбции молекулярного сита. [12]
Сферические шарики имеют преимущества перед другими формами, поскольку они обеспечивают меньший перепад давления , устойчивы к истиранию, поскольку не имеют острых краев, и обладают хорошей прочностью, т. е. сила раздавливания, необходимая на единицу площади, выше. Некоторые молекулярные сита с шариками обладают более низкой теплоемкостью , что снижает потребность в энергии во время регенерации. Другим преимуществом использования молекулярных сит с шариками является то, что объемная плотность обычно выше, чем у других форм, поэтому для данной потребности в адсорбции требуемый объем молекулярного сита меньше. При устранении узких мест можно использовать гранулированные молекулярные сита для загрузки большего количества адсорбента в тот же объем, избегая при этом модификаций сосуда. [13]
Одобрение FDA [ править ]
С 1 апреля 2012 г. FDA США одобрило алюмосиликат натрия для прямого контакта с расходными материалами в соответствии с 21 CFR 182.2727. [14] До этого разрешения Европейский Союз использовал молекулярные сита с фармацевтическими препаратами, и независимые испытания показали, что молекулярные сита соответствуют всем государственным требованиям, но промышленность не желала финансировать дорогостоящие испытания, необходимые для получения одобрения правительства. [15]
Регенерация [ править ]
Методы регенерации молекулярных сит включают изменение давления (как в концентраторах кислорода), нагрев и продувку газом-носителем (как при использовании при дегидратации этанола ) или нагрев в высоком вакууме. Температуры регенерации варьируются от 175 °C (350 °F) до 315 °C (600 °F) в зависимости от типа молекулярных сит. [16]
Адсорбционные возможности [ править ]
| Имя | Псевдоним | пора диаметр ( Ангстрем ) | Масса плотность (г/мл) | Адсорбированный вода ( % по весу ) | Потертость или истирание В (% масс.) | Использование [17] |
|---|---|---|---|---|---|---|
| 3А | А-3, Калифорния | 3 | 0.60–0.68 | 19–20 | 0.3–0.6 | Осушка нефтяного газа крекинга и алкенов, селективная адсорбция H 2 O в изоляционном стекле (IG) и полиуретане, сушка этанольного топлива для смешивания с бензином. |
| 4А | А-4, Би-А | 4 | 0.60–0.65 | 20–21 | 0.3–0.6 | Адсорбция воды в алюмосиликате натрия , одобренном FDA (см. ниже ), используемом в качестве молекулярного сита в медицинских контейнерах для сохранения содержимого сухим, а также в качестве пищевой добавки с номером E E-554 (антислеживающий агент); предпочтителен для статической дегидратации в закрытых жидкостных или газовых системах, например, при упаковке лекарств, электрических компонентов и скоропортящихся химикатов; удаление воды в печатных и пластиковых системах и сушка потоков насыщенных углеводородов. Адсорбированные виды включают SO 2 , CO 2 , H 2 S, C 2 H 4 , C 2 H 6 и C 3 H 6 . Обычно считается универсальным осушителем в полярных и неполярных средах; [16] разделение природного газа и алкенов , адсорбция воды в нечувствительном к азоту полиуретане |
| 5А-ДВ | 5 | 0.45–0.50 | 21–22 | 0.3–0.6 | Обезжиривание и снижение температуры застывания авиационного керосина и дизельного топлива , отделение алкенов. | |
| 5А небольшой обогащенный кислородом | 5 | 0.4–0.8 | ≥23 | Специально разработан для медицинского или здорового генератора кислорода. [ нужна ссылка ] | ||
| 5А | А-5, Ка-А | 5 | 0.60–0.65 | 20–21 | 0.3–0.5 | Осушка и очистка воздуха; осушка и десульфурация природного газа и сжиженного нефтяного газа ; кислорода и водорода производство адсорбции при переменном давлении методом |
| 10X | Ф-9, Са-Х | 8 | 0.50–0.60 | 23–24 | 0.3–0.6 | Высокоэффективная сорбция, используемая при сушке, обезуглероживании, обессеривании газа и жидкостей и отделении ароматических углеводородов. |
| 13X | Ф-9, На-Х | 10 | 0.55–0.65 | 23–24 | 0.3–0.5 | Осушка, десульфурация и очистка нефтяного и природного газа |
| 13X-АС | 10 | 0.55–0.65 | 23–24 | 0.3–0.5 | Обезуглероживание и сушка в воздухоразделительной промышленности, отделение азота от кислорода в кислородных концентраторах | |
| Cu-13X | с-х | 10 | 0.50–0.60 | 23–24 | 0.3–0.5 | Подслащивание (удаление тиолов ) авиационного топлива и соответствующих жидких углеводородов. |
Цеолит [ править ]
Цеолиты — это привлекательные минералы , которые могут встречаться в природе или создаваться синтетически для удовлетворения конкретных промышленных потребностей. Естественное образование цеолита представляет собой удивительное сочетание вулканической активности и грунтовых вод . Он возникает в результате взаимодействия вулканического пепла с щелочными грунтовыми водами на протяжении тысячелетий, в результате чего образуются пористые кристаллические структуры, наделяющие этот материал уникальными свойствами, которые делают его ценным в различных промышленных процессах.Вулканический пепел, богатый кремнеземом и глиноземом , действует как строительные блоки для пористых структур молекулярных сит. По мере того, как вода просачивается через эти отложения пепла, она постепенно растворяет некоторые минералы и уносит их с собой. Со временем эти растворенные минералы рекомбинируются при определенных условиях, образуя кристаллический каркас, определяющий структуру цеолита. Этот естественный процесс приводит к замечательным адсорбционным способностям, которыми славится цеолит. Благодаря своей природной структуре цеолит обладает высоким сродством к молекулам воды, что делает его особенно полезным в тех случаях, когда удаление воды имеет важное значение, например, в процессах сушки газа. [18]
3А [ править ]
- Примерная химическая формула: ((K 2 O) 2 ⁄ 3 (Na 2 O) 1 ⁄ 3 ) • Al 2 O 3 • 2 SiO 2 • 9/2 H 2 O
- Алюмосиликатное соотношение: SiO 2 / Al 2 O 3 ≈2
Производство [ править ]
Молекулярные сита 3А производятся путем катионного обмена калия на натрий в молекулярных ситах 4А.
Использование [ править ]
Молекулярные сита 3А не адсорбируют молекулы диаметром более 3 Å. Характеристики этих молекулярных сит включают высокую скорость адсорбции, способность к частой регенерации, хорошую стойкость к раздавливанию и устойчивость к загрязнению . Эти функции могут улучшить как эффективность, так и срок службы сита. Молекулярные сита 3А являются необходимым осушителем в нефтяной и химической промышленности для переработки нефти, полимеризации и химической глубокой сушки газа и жидкости.
Молекулярные сита 3А используются для сушки различных материалов, таких как этанол , воздух, хладагенты , природный газ и ненасыщенные углеводороды . К последним относятся крекинг-газ, ацетилен , этилен , пропилен и бутадиен .
Молекулярное сито 3А используется для удаления воды из этанола, который впоследствии можно использовать непосредственно в качестве биотоплива или косвенно для производства различных продуктов, таких как химикаты, продукты питания, фармацевтические препараты и т. д. Из-за образования азеотропа с концентрацией примерно 95,6 процентов по массе обычная дистилляция сама по себе не может удалить всю воду (нежелательный побочный продукт производства этанола) из технологических потоков этанола. Чтобы разрушить азеотроп, используется молекулярное сито для разделения этанола и воды на молекулярном уровне путем адсорбции воды в кристалле молекулярного сита 3А, позволяя этанолу свободно проходить. Как только молекулярное сито насыщается водой, можно манипулировать температурой или давлением, чтобы позволить воде вытечь из молекулярного сита в процессе, называемом регенерацией. [19]
Молекулярные сита 3А следует хранить при комнатной температуре, относительной влажности не более 90%. Они герметизированы при пониженном давлении, вдали от воды, кислот и щелочей.
4A[edit4А
- Химическая формула: Na 2 O•Al 2 O 3 •2SiO 2 •9/2H 2 O
- Соотношение кремний-алюминий: 1:1 (SiO 2 / Al 2 O 3 ≈2)
Производство [ править ]
Производство сита 4А относительно несложно, поскольку оно не требует ни высокого давления, ни особенно высоких температур. Обычно водные растворы силиката натрия и алюмината натрия объединяют при температуре 80°С. Пропитанный растворителем продукт «активируется» путем «обжига» при 400°C. [20]
Связь с 3А и 5А [ править ]
Сита 4А служат предшественниками сит 3А и 5А посредством катионного обмена натрия калий на (для 5А ) (для 3А) или кальций . [21] [22] Фактически, этот ионный обмен позволяет селективности молекулярного сита различать, где молекулярное сито 3А более селективно, чем молекулярное сито 4А, тогда как молекулярное сито 5А менее селективно, чем молекулярное сито 4А, и может адсорбировать более крупные молекулы. [23]
Использование [ править ]
Высыхающие растворители [ править ]
Молекулярные сита 4А широко используются для сушки лабораторных растворителей. [7] Они могут поглощать воду и другие молекулы с критическим диаметром менее 4 Å, такие как NH 3 , H 2 S, SO 2 , CO 2 , C 2 H 5 OH, C 2 H 6 и C 2 H 4 . Они широко используются при сушке, рафинировании и очистке жидкостей и газов (например, при получении аргона).

Полиэфирные добавки [ править ]
Эти молекулярные сита используются в качестве вспомогательных средств для моющих средств, поскольку они могут производить деминерализованную воду посредством обмена ионов кальция , удалять и предотвращать отложение грязи. Они широко используются для замены фосфора . Молекулярное сито 4А играет важную роль в замене триполифосфата натрия в качестве вспомогательного моющего средства, чтобы смягчить воздействие моющего средства на окружающую среду. Его также можно использовать в качестве агента, образующего мыло , и в зубной пасте .
Обращение с вредными отходами [ править ]
Молекулярные сита 4А могут очищать сточные воды от катионных частиц, таких как ионы аммония , Pb 2+ , С 2+ , Зн 2+ и компакт-диск 2+ . Благодаря высокой селективности по NH 4 + они успешно применяются в полевых условиях для борьбы с эвтрофикацией и другими последствиями на водных путях, вызванными чрезмерным содержанием ионов аммония. Молекулярные сита 4А также использовались для удаления ионов тяжелых металлов, присутствующих в воде в результате промышленной деятельности.
Другие цели [ править ]
- Металлургическая промышленность : разделительный агент, сепарация, извлечение рассолов калия, рубидия , цезия и др.
- Нефтехимическая промышленность, катализатор , осушитель , адсорбент
- Сельское хозяйство: кондиционер для почвы
- Лекарство: загрузите на основе серебряного цеолита . антибактериальное средство
5А [ править ]
- Химическая формула: 0,7CaO•0,30Na 2 O•Al 2 O 3 •2,0SiO 2 •4,5H 2 O
- Алюмосиликатное соотношение: SiO 2 / Al 2 O 3 ≈2
Производство [ править ]
Молекулярные сита 5А производятся путем катионного обмена кальция на натрий в молекулярных ситах 4А.
Использование [ править ]
сита пятиангстрема Молекулярные (5А) часто используются в нефтяной промышленности, особенно для очистки газовых потоков и в химической лаборатории для разделения соединений и сушки исходных материалов реакций. Они содержат крошечные поры точного и одинакового размера и в основном используются в качестве адсорбента для газов и жидкостей.
Молекулярные сита размером пять ангстрем используются для осушки природного газа , а также для обессеривания и декарбонизации газа. Их также можно использовать для разделения смесей кислорода, азота и водорода, а также нефтепарафиновых н-углеводородов от разветвленных и полициклических углеводородов.
Молекулярные сита пятиангстрема хранят при комнатной температуре, относительной влажности воздуха не более 90 % в картонных бочках или картонной упаковке. Молекулярные сита не должны подвергаться прямому воздействию воздуха и воды, следует избегать кислот и щелочей.
Тип 13X [ править ]
- Химическая формула: [(AlO 2 ) a (SiO 2 ) b ]• c H 2 O

Производство [ править ]
Были разработаны специализированные методы синтеза, позволяющие адаптировать свойства цеолита для различных промышленных применений. Тщательно контролируя химический состав и условия реакции, производители могут изменять размер, форму и свойства поверхности цеолита для создания синтетических молекулярных сит 13X, что позволяет оптимизировать их для выполнения конкретных функций. Для процессов разделения воздуха тщательно синтезированное молекулярное сито 13X может быть спроектировано так, чтобы избирательно адсорбировать определенные молекулы газа, пропуская при этом другие, что делает его неоценимым при разделении и очистке газов в промышленном масштабе. [24]
Связь с молекулярным А типа ситом
Кристаллы типа X имеют форму, отличную от формы кристаллов типа A, как правило, имеют гораздо больший размер пор, около 9 ангстрем в диаметре. [25]
Использование [ править ]
В газовой и биогазовой промышленности присутствие примесей, таких как диоксид углерода и сероводород, может существенно повлиять на качество и удобство использования этих ценных ресурсов. Цеолит 13X является ключевым компонентом в удалении этих примесей. Используя свою высокую селективность по диоксиду углерода и сероводороду, 13X эффективно очищает природный газ и биогаз, гарантируя, что эти ресурсы соответствуют строгим стандартам чистоты для безопасного использования. Более того, в системах разделения воздуха вступают в силу способности селективной адсорбции 13X за счет эффективного удаления примесей из воздуха. Это особенно важно в отраслях, где газы высокой чистоты необходимы для различных процессов. Способность цеолита 13X избирательно захватывать молекулы воды и другие примеси способствует достижению желаемого уровня чистоты, необходимого для промышленного применения. Помимо разделения и очистки газов, цеолит 13X также служит бесценным инструментом при осушке различных газов и жидкостей. Его исключительная способность к поглощению воды делает его незаменимым инструментом для удаления влаги в промышленных процессах. Будь то сушка природного газа, биогаза или потоков жидкости, цеолит 13X играет решающую роль в поддержании чистоты и целостности этих важных веществ. [26]
См. также [ править ]
Ссылки [ править ]
- ^ «Определение молекулярного сита - Определение молекулярного сита - Что такое молекулярное сито?» . Химия.about.com. 18 декабря 2013 г. Архивировано из оригинала 21 февраля 2014 г. Проверено 26 февраля 2014 г.
- ^ Ж. Рукерол; и др. (1994). «Рекомендации по характеризации пористых тел (Технический отчет)» (скачать бесплатно в формате pdf) . Чистое приложение. Хим . 66 (8): 1739–1758. дои : 10.1351/pac199466081739 . S2CID 18789898 .
- ^ «Молекулярное сито с покрытием – заявка на патент» . Faqs.org. 18 марта 2010 г. Проверено 26 февраля 2014 г.
- ^ Бриндли, Джордж В. (1952). «Структурная минералогия глин» . Глины и глинистые минералы . 1 (1): 33–43. Бибкод : 1952CCM.....1...33B . дои : 10.1346/CCMN.1952.0010105 .
- ^ «Виды осушителей» . SorbentSystems.com . Проверено 26 февраля 2014 г.
- ^ Манн, Б.Ф.; Манн, ПСР; Скрабалак, ГП; Новотный, М.В. (2013). «Макропористые частицы кремнезема размером менее 2 мкм, полученные для повышения сродства гликопротеинов к лектинам» . Аналитическая химия . 85 (3): 1905–1912. дои : 10.1021/ac303274w . ПМЦ 3586544 . ПМИД 23278114 .
- ↑ Перейти обратно: Перейти обратно: а б Уильямс, Д.Б., Лоутон, М., «Сушка органических растворителей: количественная оценка эффективности некоторых осушителей», Журнал органической химии, 2010, том. 75, 8351. дои : 10.1021/jo101589h
- ^ Пухадо, PR; Рабо, Дж.А.; Антос, Дж.Дж.; Гембицки, С.А. (11 марта 1992 г.). «Промышленное каталитическое применение молекулярных сит». Катализ сегодня . 13 (1): 113–141. дои : 10.1016/0920-5861(92)80191-О .
- ^ [1] Архивировано 16 апреля 2012 г., в Wayback Machine.
- ^ «Регенерирующие адсорбенты» . www.hengyeinc.com . Hengye Inc., 21 января 2020 г. Проверено 23 мая 2024 г.
- ^ Биннс, Марк (12 июня 2017 г.). «Как не убить молекулярное сито» . Журнал производителей этанола . Проверено 23 мая 2024 г.
- ^ «Молекулярное сито для кислородного концентратора» . www.hengyeinc.com . Hengye Inc., 19 февраля 2024 г. Проверено 23 мая 2024 г.
- ^ Беркс, Колтен (28 февраля 2018 г.). «Действительно ли размер имеет значение?» . www.hengyeinc.com . Хенгье Инк . Проверено 23 мая 2024 г.
- ^ «Раздел 182.2727 Алюмосиликат натрия» . Управление по контролю за продуктами и лекарствами США. 1 апреля 2012 года . Проверено 10 декабря 2012 г.
- ^ «Молекулярное сито-осушитель» . DesiccantPacks.net . Проверено 26 февраля 2014 г.
- ↑ Перейти обратно: Перейти обратно: а б «Молекулярные сита» . Сигма-Олдрич . Проверено 26 февраля 2014 г.
- ^ «Молекулярное сито, молекулярные сита Июань» . Chemicalpackingcorp.com . Проверено 26 февраля 2014 г.
- ^ «Цеолит 13X - раскрытие его универсального использования, применения и преимуществ» . www.hengyeinc.com . 30 января 2024 г. Проверено 23 мая 2024 г.
- ^ Биннс, Марк; Беркс, Колтен (сентябрь – октябрь 2017 г.). «Удаление воды из этанола» . Биотопливо Интернэшнл . 11 (5): 38–39 . Проверено 10 июля 2015 г.
- ^ US 3433588 , Макс Мишель и Денис Папи, «Способ получения цеолитов с единицей измерения 4 ангстрема», опубликовано 18 марта 1969 г., выпущено 18 марта 1969 г.
- ^ Зеохем
- ^ Внутриглобальный
- ^ Беркс, Колтен (20 июля 2017 г.). «3А, 4А, 5А, 13Х... Какая разница?» . Хенгье Инк . Проверено 22 мая 2024 г.
- ^ «Цеолит 13X - раскрытие его универсального использования, применения и преимуществ» . www.hengyeinc.com . 30 января 2024 г. Проверено 23 мая 2024 г.
- ^ Беркс, Колтен (20 июля 2017 г.). «3А, 4А, 5А, 13Х... Какая разница» . www.hengyeinc.com . Проверено 23 мая 2024 г.
- ^ «Цеолит 13X - раскрытие его универсального использования, применения и преимуществ» . www.hengyeinc.com . 30 января 2024 г. Проверено 23 мая 2024 г.